ÁREA: Materiais
TÍTULO: COMPORTAMENTO ELETROQUÍMICO DA LIGA Ni-Cr-Mo-Ti EM DIFERENTES ELETRÓLITOS NA AUSÊNCIA E PRESENÇA DE ALBUMINA
AUTORES: VIEIRA, J.C. (IQ-USP) ; AREAS, E.P.G. (IQ-USP) ; AGOSTINHO, S.M.L. (IQ-USP)
RESUMO: Uma liga Ni-Cr-Mo-Ti empregada em próteses odontológicas foi estudada em meios de NaCl, na ausência e presença de albumina e de NaF e de ácido cítrico, empregando medidas de potencial de circuito aberto e curvas de polarização potenciostática anódica, a 36,5 oC. Foi verificado que a albumina favorece a dissolução da liga em todos os meios estudados. Em meios de NaF e de ácido cítrico, a presença da proteína elimina completamente a faixa de potencial em que a liga se mantém passivada.
PALAVRAS CHAVES: oxidação, liga ni-cr-mo-ti, albumina
INTRODUÇÃO: Diversas composições de ligas de base Ni-Cr tem sido utilizadas na odontologia em substituição às ligas áuricas, dado o seu menor custo e boa resistência à oxidação. Trabalhos anteriores têm mostrado que a albumina modifica o comportamento eletroquímico de diferentes materiais metálicos quando expostos a meios que simulam fluidos biológicos [1, 2].
O objetivo desse trabalho é de estudar o efeito da albumina na oxidação anódica de uma liga odontológica de Ni-Cr-Mo-Ti em diferentes meios que podem estar presentes no ambiente bucal.
MATERIAL E MÉTODOS: Utilizou-se um eletrodo de trabalho sólido, obtido pelo embutimento de amostra de Liga Ni-Cr-Mo-Ti Tilite® (Talladium Brasil) em resina inerte aos meios de ensaio. O eletrodo de referência adotado foi o de calomelano saturado (ECS). Foi empregado como eletrodo auxiliar o de platina de grande área. Os meios de ensaio usados foram: (a) NaCl 9 g L-1 para simular o efeito do soro fisiológico presente na saliva; (b) NaF 3,3 g L-1 em NaCl 9 g L-1, para simular o conteúdo de íon fluoreto presente em alguns dentifrícios bucais; (c) ácido cítrico (H3Cit) 11 g L-1 em NaCl 9 g L-1, para simular o efeito do suco de laranja; (d) albumina de soro bovino (BSA), pI=5,5, adicionada aos meios (a) a (c), a 0,20 g L-1. Medidas de potencial de circuito aberto e de polarização potenciostática anódica foram feitas como técnicas de ensaio eletroquímico, com os eletrodos de trabalho, referência e auxiliar imersos primeiramente no meio de NaCl. Posteriormente, as medidas eram repetidas com a adição de BSA ao primeiro meio, ou de NaF e depois BSA, ou de H3Cit e depois BSA.
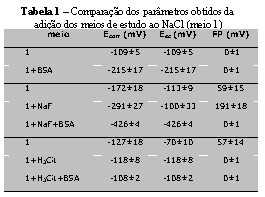
RESULTADOS E DISCUSSÃO: A tabela 1 apresenta uma visão geral dos resultados obtidos.
Observa-se que a liga Ni-Cr-Mo-Ti apresenta uma superfície bem irreprodutível, conforme se comparam os valores de Ecorr, Esc, FP e ipass para o NaCl nas diferentes superfícies ensaiadas. A faixa passiva é muito pequena, no máximo igual a 60 mV, e em outros experimentos mostra-se inexistente.
Nota-se que a adição de NaF ao NaCl torna bem mais negativos os valores de Ecorr, mas não altera os valores de Esc e de ipass, indicando uma modificação na composição da interfase, sem alteração das características do filme passivante.
O ácido cítrico tem o efeito de reduzir a zero a faixa passiva quando adicionado ao NaCl, indicando o rompimento do filme passivo no próprio Ecorr. Atribui-se este efeito ao baixo valor de pH quando da adição do H3Cit, dissolvendo os óxidos. Não se pode descartar, também, a possibilidade de complexação dos íons metálicos pelo ânion citrato.
A albumina bovina torna mais negativos Ecorr e Esc quando adicionada ao NaCl e ao NaCl+NaF, principalmente neste último meio. Observou-se o total desaparecimento do filme passivante, desde o Ecorr, quando da adição da proteína. Nota-se que a adsorção da BSA é maior em meio de NaF (pH≈7). Por se encontrar acima do seu ponto isoelétrico, portanto carregada negativamente, a sua adsorção sobre a liga Ni-Cr-Mo-Ti no Ecorr deve ocorrer em virtude da formação de complexos com metais de transição. O eletrodo, no Ecorr, encontra-se a um potencial bem mais negativo, diferente dos outros materiais estudados, o que torna difícil atribuir este resultado a um efeito puramente eletrostático.
CONCLUSÕES: A BSA favorece a dissolução do filme passivo, mesmo no Ecorr, em todos os meios estudados.
AGRADECIMENTOS:
REFERÊNCIAS BIBLIOGRÁFICA: [1]Vieira, J.C.; Estudo de interfases eletroquímicas envolvendo materiais metálicos de uso odontológico; dissertação de mestrado; IQ-USP; São Paulo; 2006.
[2] Afonso, M.L.C.A.; Caracterização do aço inoxidável austenítico UNS S31254 em meio de NaCl 0,11 mol L-1 visando seu emprego em implantes ortopédicos; tese de doutorado; IQ-USP; São Paulo; 2006.
[3] Huang, H.; Effect of fluoride and albumin concentration on the corrosion behavior of Ti-6Al-4V alloy; Biomaterials 2003; 24: 275-282.
