ISBN 978-85-85905-10-1
Área
Química Orgânica
Autores
Egito, M.S. (UFPE) ; Silva, T.G. (UFPE) ; Militão, G.C.G. (UFPE) ; Albuquerque, J.F.C. (UFPE)
Resumo
O grande desafio imposto aos pesquisadores atuais é a busca por novas moléculas que sejam específicas para determinadas doenças e que causem menos efeitos colaterais. As tiossemicarbazonas são compostos conhecidos por possuírem diversas atividades biológicas. São moléculas versáteis, de fácil obtenção e muito utilizadas como intermediários na produção de compostos heterocíclicos. A fim de encontrar uma molécula eficiente, um novo derivado tiossemicarbazônico foi sintetizado a partir da reação entre a tiossemicarbazida e o 3-Bromo-5- Clorosalicilaldeído. Após isolamento e purificação por cristalização sua estrutura química foi confirmada pelos métodos espectroscópicos convencionais (RMN1H, RMN13C e infravermelho) e as suas constantes físicas foram determinadas.
Palavras chaves
heterocíclico; tiossemicarbazida; tiossemicarbazona
Introdução
Para o desenvolvimento da indústria de medicamentos é preciso levar em conta a síntese e o planejamento de novos fármacos na busca de produtos bioativos por reações orgânicas de substâncias previamente estudadas com potencial atividade biológica. As tiossemicarbazonas são compostos de grande interesse científico devido as suas importantes propriedades químicas e biológicas, e por apresentarem ações como antitumoral, antibacteriana, antiviral, antiprotozoária, citotóxica, etc. (BASU et al., 2010). Tiossemicarbazonas são conhecidas, também, pelas suas excelentes propriedades para formarem complexos organometálicos, comportando-se como agentes quelantes (PAUL et al., 2011). Duas estratégias diferentes podem ser empregadas para a obtenção destes compostos que podem ser obtenção direta, pela reação quimiosseletiva de aldeídos e/ou cetonas com as tiossemicarbazidas, e obtenção indireta, pela preparação prévia das tiossemicarbazidas, utilizando hidrazina (NH2-NH2) e diferentes reagentes, seguida de condensação com o derivado carbonilado específico. Tais moléculas recebem a denominação da classe tiossemicarbazona após o nome do respectivo aldeído ou cetona que foi condensado. Do ponto de vista sintético, apresentam como características principais sua versatilidade de obtenção, assim como vasta aplicação como intermediários de muitos núcleos importantes. Estas moléculas apresentam baixo custo de síntese e grande economia de átomos, uma vez que, com exceção da água que é liberada na sua síntese, todos os outros átomos dos reagentes estarão presentes na molécula final. Essas substâncias são muito utilizadas como intermediários na síntese orgânica de importantes compostos heterocíclicos, como tiazois, tiazolidinonas e aminopirazois (TENÓRIO et al., 2005).
Material e métodos
O composto tiossemicarbazônico foi sintetizado a partir da reação entre a tiossemicarbazida e o 3-Bromo-5-Clorosalicilaldeído em iso-propanol e ácido clorídrico concentrado. Em um balão de fundo redondo foram adicionados cuidadosamente 0,100 g de tiossemicarbazida e 2 mL de iso-propanol como solvente e também para facilitar a cristalização do produto formado. Posteriormente, foi adicionado ácido clorídrico concentrado e a reação permaneceu sob agitação magnética à temperatura ambiente, por quinze minutos para facilitar a formação do ânion e ataque deste ao benzaldeído substituído, adicionado numa segunda etapa da reação. Após este período, foi acrescentado 0,389 g do 3-Bromo-5- Clorosalicilaldeído à mistura reacional (Figura 1). Este reagente foi também previamente solubilizado em iso-propanol e adicionado gota a gota à reação que se encontrava à temperatura ambiente sob agitação contínua. À medida que o benzaldeído foi sendo adicionado cuidadosamente, ainda à temperatura ambiente, foi observada a formação de um precipitado branco. Este precipitado chamou a atenção para a realização de uma cromatografia de camada delgada para verificar se o composto formado naquela ocasião era o produto. Ao se fazer a cromatografia, foi confirmado que se tratava do produto e que os reagentes já tinham sido consumidos ao longo da reação. Após o término de a reação ter sido comprovado, o produto foi vertido para um béquer, filtrado em funil sinterizado e lavado várias vezes com água destilada (com o objetivo de remover resíduos do ácido). Após filtração cuidadosa à vácuo e observado a ausência total de solvente o produto foi isolado e purificado por recristalização em iso-propanol. Os cristais formados foram secos em estufa a 37 ºC e determinadas as suas constantes físicas.
Resultado e discussão
Os resultados apresentados pelo produto reacional puro foram os seguintes: Ponto
de Fusão. 225-226 ºC, Rf. 0,46 no sistema (hexano e acetato de metila
na seguinte proporção 0,60:0,40, respectivamente). O rendimento foi de 76,31 %,
que foi considerado muito bom. Foram utilizadas quantidades equimolares dos
reagentes, que reagiram de imediato à temperatura ambiente, ou seja, não houve
gasto de água (necessária quando a reação se processa sob refluxo) e nem de
energia. A não utilização desses dois itens deixa o processo mais barato, tanto
do ponto de vista econômico como ambiental. Foram realizados os espectros de
Ressonância Magnética Nuclear de Hidrogênio e Carbono treze como também o
espectro de Infravermelho. O espectro de Infravermelho foi responsável pela
identificação da função orgânica por meio das características exatas e de
absorções na faixa responsável por cada pico. Os sinais referentes a cada
hidrogênio e carbono foram identificados por meio dos espectros de Ressonância
Magnética Nuclear de Hidrogênio e de Carbono treze.
Os picos obtidos foram os seguintes: IV., principais sinais (cm –1,
KBr 1%, ) 3149,88 (O–H); 3411,58; 3238,26 (N–H); 1598,82 (C=N); 1287,31 (C-O);
1240,52 (C=S) cm-1. RMN1H (300 MHz, DMSO-d6, δ, ppm),
7.643 (s, 1H, Ar); 8.050 (s, 1H, Ar), 8.247 (s, 2H, NH2); 8.302 (s,
1H, CH); 9.941 (s largo, 1H, O-H); 11.542 (s, 1H, N-H). RMN13C e DEPT
(75.5 MHz, DMSO-d6, δ, ppm), 15,4 (CH3); 71.6 (CH2); 102.8
(S–CH); 114.3 (Ar); 114.8 (Ar), 121.0 (Ar); 127.3 (Ar); 128.9 (Ar); 129,1 (Ar);
132,2 (Ar); 140,8 (CH=C); 154.0(C=N); 158,7 (C–O); 168,1 (S–C=N).
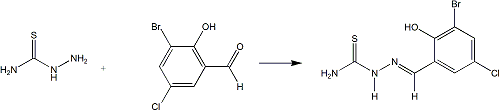
Esquema de síntese do derivado tiossemicarbazônico.
Conclusões
A síntese apresentou um sólido branco cristalizado. A reação foi processada imediatamente a adição dos reagentes. O composto foi sintetizado dentro das normas planejadas, por reação rápida e sem gastos de água e energia. As constantes físicas foram determinadas, incluindo rendimento, Rf e PF. A estrutura química foi comprovada pelos métodos espectroscópicos de RMN1H, RMN13C e Infravermelho. O derivado foi sintetizado com rendimento excelente. O próximo passo será a realização de testes para avaliar a atividade anticâncer deste composto e posteriores reações de ciclização.
Agradecimentos
Ao CNPq pelo financiamento da pesquisa.
Referências
BASU, S.; ACHARYYA, R.; BASULI, F.; PENG, S.; LEE, G.; MOSTAFA, G.; BHATTACHARYA, S. Iridium assisted S–H and C–H activation of benzaldehydethiosemicarbazones. Synthesis, structure and electrochemical properties of the resulting complexes. Inorganica Chimica Acta; v.363, p.62-73, 2010.
PAULA. P; DATTA, S.; HALDER, S.; ACHARYYA, R.; BASULI, F.;BUTCHER, R. J.; PENG, S.; LEE, G.; CASTINEIRAS, A.; DREW, M. G. B.; BATTACHARRYA, S. Syntheses, structures and efficient catalysis for C–C coupling of some benzaldehydethiosemicarbazone complexes of palladium. Journal of Molecular Catalysis A: Chemical; v.344, p.62–73, 2011.
TENÓRIO, R. P.; GÓES, J. S.; LIMA, J. G.; FARIA, A. R.; ALVES, A. J.; AQUINO, T. M. Tiossemicarbazonas: Método de obtenção, aplicações sintéticas e importância biológica. Química Nova; v.28, n.6, p.1030-1037, 2005.










