ISBN 978-85-85905-10-1
Área
Química Orgânica
Autores
Silva, J.F. (UFCG) ; Lima, J.A.C. (UFCG) ; Freitas, J.J.R. (UFPE) ; Silva, C.L.L. (UFPE) ; Freitas, L.P.S.R. (UFCG) ; Freitas, J.C.R. (UFCG) ; de Andrade Vicente, D. (UFRPE)
Resumo
Este trabalho descreve a síntese de alcoóis homoalílicos funcionalizados a partir da reação de alilação de diferentes aldeídos por alil trifluoroborato de potássio utilizando sílica ácida como catalisador. A metodologia mostrou-se eficiente, pois levou aos alcoóis homoalílicos em excelentes rendimentos e em curtos tempos reacionais sob um sistema bifásico.
Palavras chaves
Alcoóis homoalílicos; Sílica ácida; Alil trifluoroborato
Introdução
A alilação de compostos carbonílicos é um dos métodos mais empregados para a formação de novas ligações C-C.1 O produto dessa reação, ou seja, os alcoóis homoalílicos, são importantes blocos de construção na síntese de moléculas biologicamente ativas.2 Assim, a procura de métodos para sintetizar esta classe de compostos é muito interessante em química orgânica e farmacêutica, especificamente para a preparação de novos agentes terapêuticos. Geralmente na reação de alilação são empregadas espécies organometálicas de lítio (RLi) ou Grignard (RMgBr), que são susceptíveis ao ar e água, o que tornam a síntese mais limitada.3 Neste aspecto, os sais de organotrifluoroboratos se destacam, pois são reagentes que podem ser estocados sem cuidados adicionais, podem ser facilmente manipulados, além de serem estáveis sob o ar.4 Assim, este trabalho descreve a síntese de alcoóis homoalílicos funcionalizados a partir da alilação de diversos aldeídos por aliltrifluoroborato de potássio na presença de sílica ácida (SiO2/H2SO4) como catalisador usando um sistema bifásico.
Material e métodos
Material e Instrumentação Em todas as reações foram utilizados solventes e reagentes na sua forma comercial (P.A.). A cromatografia em camada delgada (CCD) foi feita utilizando placas de sílica-gel contendo indicador de fluorescente GF254. Para visualização das CCD, foi utilizada luz ultravioleta, vapor de iodo e solução ácida de vanilina. Os espectros de Ressonância Magnética Nuclear de 1H (300 MHz), 13C (75 MHz), 19F (282 MHz) e 11B (96 MHz) foram obtidos em um espectrofotômetro, utilizando clorofórmio deuterado (CDCl3) ou dimetilsulfóxido deuterado (DMSO-d6) como solventes e os deslocamentos químicos expressos em partes por milhão. Os espectros de infravermelho foram obtidos em espectrofotômetro de IV com Transformada de Fourier, sendo as amostras preparadas como filmes finos ou pastilhas de KBr. Procedimento Experimental Preparação da Sílica Ácida (SiO2/H2SO4) Em um balão de 150 mL foi adicionado sílica gel (5 g, 200-300 mesh) em éter dietílico seco (50 mL). Em seguida, a essa suspensão foi adicionado ácido sulfúrico concentrado (0,25 mL) sob agitação. Após 5 min, o solvente foi evaporado e o sólido resultante foi secado sob 120 oC por 3 h. A capacidade de carga H2SO4 na sílica gel foi de 0,9 mmol de H3O+ por grama. Preparação dos alcoóis homoalílicos Em um tubo de 10 mL contendo o alil trifluoroborato de potássio 2 (89 mg, 0,60 mmol) e o aldeído apropriado 1a-f (0,50 mmol) foi adicionado CH2Cl2 (1,50 mL) e H2O (1,50 mL), seguido da adição da sílica ácida (50% M/M). A mistura bifásica foi agitada durante o tempo indicado no Esquema 1. Após o término da reação a fase orgânica foi separada, extraída com CH2Cl2 (3 x 5 mL) e secada com MgSO4. O solvente foi removido sob pressão reduzida fornecendo os alcoóis homoalílicos (3a-f) em excelentes rendimentos.
Resultado e discussão
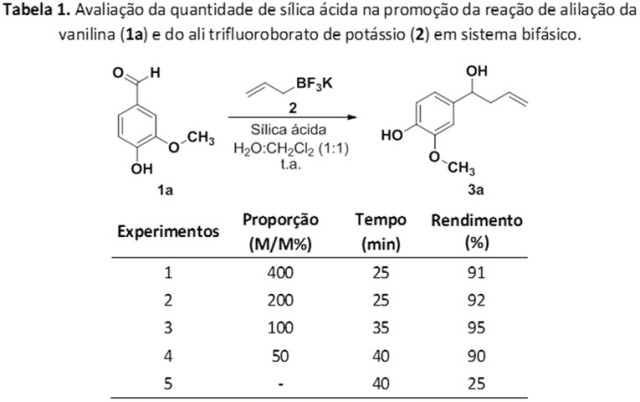
O trabalho foi iniciado com a avaliação da quantidade mínima necessária de
sílica ácida na reação de alilação. Para isso, foram colocados para reagir, a
vanilina (1a) e o alil trifluoroborato de potássio (2) em um sistema bifásico
(H2O:CH2Cl2, na proporção 1:1) utilizando diferentes quantidades de sílica ácida
(Tabela 1).
O estudo demonstrou que a diminuição da quantidade de sílica ácida, levou a um
aumento do tempo reacional (Experimentos 1-4, Tabela 1), sendo isto justificado
devido à diminuição da acidez do meio reacional, o que não favorece a ativação
do grupo carbonila. Adicionalmente, a reação na ausência da sílica ácida levar a
formação do álcool homoalílico correspondente 3a, contudo em baixo rendimento
(Experimento 5, Tabela 1).
A fim de verificar a eficácia e robustez desta alilação utilizando sílica ácida
a metodologia foi então estendida para diferentes aldeídos 1a-f, e em todos as
reações os alcoóis homoalílicos 3a-f foram obtidos em excelentes rendimentos e
baixos tempos reacionais (Esquema 1).
Avaliação da quantidade de sílica ácida na alilação da vanilina (1a) e do ali trifluoroborato de potássio (2) sob sistema bifásico.
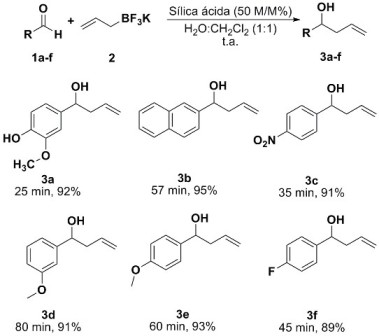
Síntese de diferentes alcoóis homoalílicos funcionalizados.
Conclusões
Neste trabalho, foi descrito uma catálise heterogênea utilizando a sílica ácida como catalisador para a reação de alilação de aldeídos por aliltrifluoroborato de potássio. Está metodologia demonstrou ser eficiente e rápida utilizando um sistema bifásico. Novos estudos estão em andamento, visando ampliar os resultados para outros aldeídos e imidas.
Agradecimentos
Os autores agradecem a CNPq, CAPES, UFCG, UFRPE e UFPE pelas bolsas e auxílio financeiro.
Referências
1. Nowrouzi, F.; Thadani, A. N.; Batey, R. A. Org. Lett. 2009, 11, 2631.
2. (a) Devi, T. J.; Saikia, B.; Barua, N. C. Tetrahedron 2013, 69, 3817. (b) Tietze, L. F.; Wolfram, T.; Holstein, J. J.; Dittrich, B. Org. Lett. 2012, 14, 4035. (c) Yadav, J. S.; Reddy, M. K.; Gupta, M. K.; Reddy, B. V. S. Monotsh. Chem. 2013, 144, 1583. (d) de Fátima, A.; Kohn, L. K.; de Carvalho, J. E.; Pilli, R. A. Bioorg. Med. Chem. 2006, 14, 622. (e) Sang, F.; Feng, P.; Chen, J.; Ding, Y.; Duan, X.; Zhai, J.; Ma, X.; Zhang, B.; Zhang, Q.; Lin, J.; Chen, Y. Eur. J. Med. Chem. 2013, 68, 321. (f) Barbosa, F. C. G.; Freitas, J. C. R. Melo, C. F.; Menezes, P. H.; Oliveira, R. A. Molecules 2012, 17, 14099.
3. (a) Yamamoto, Y.; Asao, N. Chem. Rev. 1993, 93, 2207. (b) Denmark, S. E.; Fu, J. Chem. Rev. 2003, 103, 2763.
4. Thadani, A. N.; Batey, R. A. Org. Lett. 2002, 4, 3827.










