ISBN 978-85-85905-10-1
Área
Química Orgânica
Autores
Moraes, M.I. (UFPI) ; Soares, S.H. (UFPI) ; Viana, C.C. (UFPI) ; Nobre, F.X. (UFPI) ; Matos, J.M.E. (UFPI) ; Vieira, E.C. (UFPI) ; Machado, L.L. (UFOB) ; Santos, A.K.L. (UFCA)
Resumo
A biotranformação surgiu como um processo eficiente para a síntese de compostos orgânicos quirais e pode ser definida como modificações específicas da estrutura molecular de uma substância catalisada por meios biológicos (MACHADO et al, 2009). Utilizamos de uma metodologia eficiente para a redução de aldeídos aos seus álcoois correspondentes, empregando as sementes do amendoim (Arachis hypogaea L) como uma nova fonte de enzimas a serem utilizadas nas biotransformações. O amendoim mostrou-se bastante seletivo, com excelentes conversões tanto ao reagir com o benzaldeído quanto com o 4-metóxibenzaldeído.
Palavras chaves
biorredução; 4-metóxibenzaldeido; amendoim
Introdução
Nos últimos anos, o crescente interesse na preparação de compostos orgânicos ampliou o desenvolvimento de novos procedimentos sustentáveis e amigos do ambiente. Entre todos estes métodos, a biotransformação surgiu como um processo eficiente para a síntese de compostos de elevado valor (MACHADO et al, 2009). A Biocatálise tornou-se uma ferramenta cada vez mais importante para os químicos sintéticos. A biorredução é um método atraente, principalmente devido a uma elevada enantiosseletividade, condições de reação suaves e seguras e menores impactos ambientais em comparação com reações convencionais em química (LOPES et al, 2011). As plantas têm sido consideradas sistemas enzimáticos adequados para serem empregados em biocatálise. A maioria das reações catalisadas por plantas são processos redox (redução de aldeídos e cetonas, oxidação de álcoois racêmicos) (BIZERRA et al, 2010). As reações biocatalíticas pode ser aplicada na fitoterapia de poluentes orgânicos (ANDRADE et al, 2006), lactonização enzimática (ORDEN et al, 2009; ANDRADE et al, 2006), hidrólise de ésteres (ORDEN et al, 2009; BIZERRA et al, 2010), além da glicosilação (GIRI et al, 2001). O amendoim é uma erva que possui um caule encurtado e folhas trifolioladas, raiz aprumada de 1 – 1,5 pés de altura, flores anãs e a noz cresce para o subterrâneo pertencente à família Fabaceae. Devido possuir uma quantidade significativa de lipídeos, é utilizado na fabricação de óleo de cozinha. Portanto, o trabalho tem por objetivo realizar biotransformações, mais especificamente, biorreduções do benzaldeído e do 4-metóxibenzaldeído, através de reações enzimáticas de biocatalisadores vegetais da espécie Arachis hypogaea L.
Material e métodos
As sementes foram lavadas com água destilada, e mantidas em solução aquosa de hipoclorito de sódio a 5% durante 10 minutos, em seguida foram trituradas no liquidificador até a obtenção de pedaços não uniformes de aproximadamente 0,5 cm. Em erlenmeyeres (250 mL) foram adicionados respectivamente, as sementes trituradas (24g), os substratos (200mg) e 150 mL de água destilada. Colocou-se as amostras em um orbital shaker (150 ppm) por 72 horas, de acordo com os procedimentos da literatura (MACHADO et al., 2006). A mistura foi, em seguida, filtrada, e as sementes foram lavadas com água. Os filtrados foram submetidos à extração líquido-líquido com AcOEt (3 x 50mL), que a partir desta obteve-se a fase orgânica. Essa foi seca com sulfato de sódio anidro para a eliminação da água e concentrada em rota-evaporador a 80 rpm, onde a temperatura não excedeu 40 °C, obtendo-se assim o extrato bruto da biorredução. Os produtos finais foram purificados por coluna de gel de sílica, utilizando Hex : AcOEt (8:2, v/v) como eluente, para se obter o produto reduzido. As conversões foram quantificadas por GC-MS.
Resultado e discussão
Para as biorreduções foram utilizados como substratos o benzaldeído (1) e o 4-
metóxibenzaldeído (2), obtendo seus álcoois correspondentes (Esquema 1). Em
todas as reações foram utilizadas células íntegras das sementes de amendoim. A
conversão foi determinada por CG/EM, os resultados são apresentados na Tabela 1.

Tabela 1: Resultados das biotransformações do benzaldeído e 4-metóxibenzaldeído
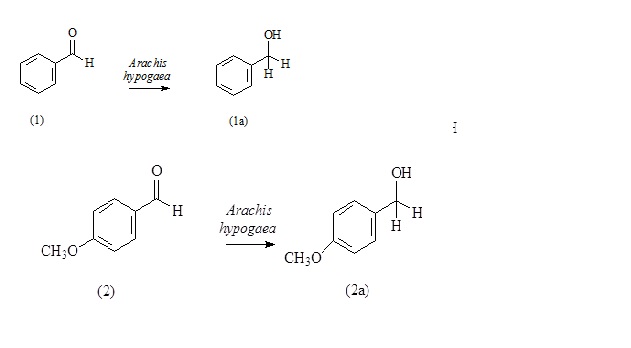
Esquema 1:Esquema das biotransformações utilizando células íntegras de amendoim
Conclusões
As sementes de amendoim (Arachis hypogaea L) apresenta-se como um excelente biocatalisador, cujas enzimas foram capazes de realizar as biorreduções, pois produziu os álcoois 1a com 99% de conversão e 2a com 94,3% de conversão. Dessa forma, o amendoim mostra-se bastante seletivo, e com excelente conversão frente ao benzaldeído e ao 4-metóxibenzaldeído, cujas conversões foram 99 e 94,3%, respectivamente.
Agradecimentos
Referências
ANDRADE, L.H., et al. Edible catalysts for clean chemical reactions: Bioreduction of aromatic ketones and biooxidation of secondary alcohols using plants. Journal of Molecular Catalysis B: Enzymatic, v. 38, p.84-90, 2006.
BIZERRA, A. M. C., et al. Reduction processes biocatalyzed by Vigna unguiculata. Tetrahedron: Asymmetry, v. 21, p. 566-570, 2010.
GIRI, A., et al. Biotransformations using plant cells, organ cultures and enzyme systems: current trends and future prospects. Biotechnology Advances, v. 19, p. 175-199, 2011.
LOPES, R. D. O., et al. Highly enantioselective bioreduction of 4-bromoacetophenone. Tetrahedron: Asymmetry, v. 22, p. 1763-1766, 2011.
MACHADO, L. L. et al. Bioreduction of Aldehydes and Ketones using Manihot species.Phytochemistry, v. 67, p. 1637-1643, 2006.
MACHADO, L. L., et al. Enantioselective acetylation of racemic alcohols by Manihot esculenta and Passiflora edulis preparations. Journal of Molecular Catalysis B: Enzymatic,v. 60, p. 157-162, 2009.
ORDEN, A. A., et al. Anti-Prelog reduction of ketones by hairy root cultures. Journal of Molecular Catalysis B: Enzymatic, v. 61, p. 216-220, 2009.
WIKIPÉDIA.; Amendoim – Wikipédia, a enciclopédia livre. Disponível em: <http://pt.wikipedia.org/wiki/Seriguela>. Acessado em: 20 de março 2014.










