ISBN 978-85-85905-10-1
Área
Bioquímica e Biotecnologia
Autores
Oliveira Silva, W. (UPE) ; Lucas Silva, I. (UFPE) ; Alves O Silva Liveira, L. (UFPE/UFAM)
Resumo
As actinobactérias estão largamente distribuídas no meio ambiente e possuem um alto potencial enzimático, entre estas enzimas estão a L- asparaginase e L- glutaminase.Este trabalho teve como objetivo avaliar qualitativamente e quantitativamente a produção dos complexo enzimático. Apenas a linhagem 8M, mostrou-se como potencial produtora da enzima asparaginase apresentado resultado positivo para ambos os testes qualitativos. A produção enzimática para L- asparaginase foi testada em fermentação semi-sólida e líquida utilizando dois diferentes substratos: farinha de soja e farinha de arroz, com o tempo de crescimento de 8 dias em condições estacionária. A FS, foi condicionada em função da atividade enzimática de fermentação em 120 horas a 180 rpm e 37°C. A FS teve mais eficiência.
Palavras chaves
Actinobactérias; L-asparaginase; L-glutaminase
Introdução
Actinobactérias fazem parte da comunidade microbiana do solo e colaboram no desenvolvimento de plantas, com isso, a presença desses micro-organismos na rizosfera é de extrema importância. As contribuições de actinobactéria do solo à biotecnologia são atribuídas segundo Miao (2010) citado por Silva (2012) na produção de antibióticos, no envolvimento em processos de ciclagem de matéria orgânica, na biorremediação, síntese de enzimas de aplicação industrial e farmacêutica além da participação da conversão e produção de bicombustíveis. São degradadoras da matéria orgânica como celulose, lignina e quitina, gerando biomassa proteica ou mesmo servindo como alimento para outros organismos (AZUMA, 2011). Através do uso da tecnologia enzimática microbiana, pode-se obter uma gama de enzimas, com potencial biotecnológico. Dentre estas se destacam enzimas de grande atrativo industrial e farmacêutico, como L-asparaginase e a L-glutaminase, atualmente aceitas, como agentes antitumorais. A L-asparagina é decomposta para o ácido L-aspártico e amônia por uma enzima exocelular a L-asparaginase. Contudo, a L-glutamina desempenha um papel importante no ciclo do nitrogênio no solo. Esta é decomposta para o ácido L-glutâmico e amônia por uma enzima exocelular a L-glutaminase (BALAGURUNATHAN et al, 2010). Neste contexto o presente trabalho visa contribuir com a busca de novos organismos potenciais que possuem capacidade de produção de L-asparaginase produzidas por actinobactérias isoladas do bioma da Caatinga.
Material e métodos
Foram estudadas 35 linhagens de actinobactérias, isoladas da rizosfera de Catingueira, no período de inverno.Para selecionar a linhagem mais promissora quanto à capacidade em degradar glutamina e asparagina foram realizados ensaios qualitativos. Os ensaios de detecção da enzima L-asparaginase foram realizados utilizando meio de cultura M-9 descrito por Gulati et al,1997. Os ensaios de detecção de L-glutaminase, utilizou-se o meio Minimo Glutamina Agar,descrito por Balagurunathan et al, 2010.A linhagem que se destacou nos ensaios qualitativos, foi avaliada quanto a capacidade de excretar o referido complexos enzimático em diferentes meios líquidos e meio semi-sólidos de fermentação. Foram utilizados dois diferentes substratos: farinha de soja e farinha de arroz como diferentes fontes de carbono indutoras do complexo enzimático.Para extração do complexo enzimático excretado pelas referidas linhagens nas fermentações semi-sólidas, foram adicionado 50 ml de tampão de fosfato de sódio 0,1 M, pH 7,0, seguido por centrifugação a 8000 rpm por 8 minutos e os sobrenadantes obtidos foram posteriormente submetidos a dosagens quantitativas dos referidos complexos enzimáticos (BASHA et al., 2009).No estudo de fermentação líquida foi avaliada a capacidade de produção do referido complexo enzimático em meio líquido de fermentação. A linhagem de actinobacteria foi inoculadas em 100 mL de meio líquido M-9 modificado (GULATI, et al 1997), inoculada com 1mL de pré-inoculo, incubados por até 7 dias a 37 º C, sob agitação de 180 rpm. Posteriormente submetidos a quantitativa conforme descrita por Imada et al. 1973, utilizou o reativo de Nessler (TIZZOT et al.,2005). Foram avaliados a influência dos parâmetros de pH e temperatura na produção do complexo L-asparaginase.
Resultado e discussão
Das 35 linhagens cedidas pelo laboratório de coleção de micro-organismos UFPEDA
isolados da rizosfera da catingueira no período de inverno, apenas uma corres e
designada 8M, apresentou modificação de coloração do meio de cultura M-9 bem
como MGA, formando um halo rosa em torno da colônia. Esta mudança de coloração
ocorre devido a alteração de pH do meio provocado pela atuação da enzima(BASHA
et al 2009. Sabe-se que embora a L-asparaginase seja identificada em muitos
organismos, apenas enzimas de origem bacteriana são usados na terapia do câncer,
e destas, apenas do tipo II de L-asparaginases pode possuir atividade
anticancerígena (GESTO et al., 2013. Neste contexto a linhagem 8-M foi a
selecionada para dar continuidade ao presente trabalho. Quando o isolado foi
submetido à fermentação semi-sólida foram utilizados a farinha de arroz e
farinha de soja, como substratos. Porém apenas com a farinha de arroz foi
constatado o crescimento da linhagem. Com produção enzimática de 0,318 µmol
amônia/mL min após 8 dias de cultivo em condições estacionarias. Na fermentação
líquida realizada com o meio M9 modificado, obteve-se um melhores resultados
detectando um perfil cinético com pico de produção em 48 horas de cultivo, de
0,672 U/mL (Figura 2). Posteriormente foi verificada a influência do pH na
produção do complexo enzimático excretado pela linhagem 8-M, em uma faixa de pH
de 5,0 a 9,0. O pH inicial 6,0 apresentou o melhor valor de atividade enzimática
correspondente a 1,021 U/mL. Resultado que mostrou uma melhora na produção
enzimática. O parâmetro final avaliado no presente trabalho foi a temperatura no
qual observa-se que em uma faixa de 37° a 45 ºC, a temperatura de 37ºC de
incubação continuou apresentando a melhor atividade enzimática correspondente a
1,021 U/mL.
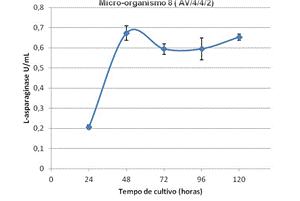
Cinética de produção do complexo L- asparaginase excretado pela linhagem 8-M em fermentação liquida meio M9 sob agitação de 180 rpm a 37°C
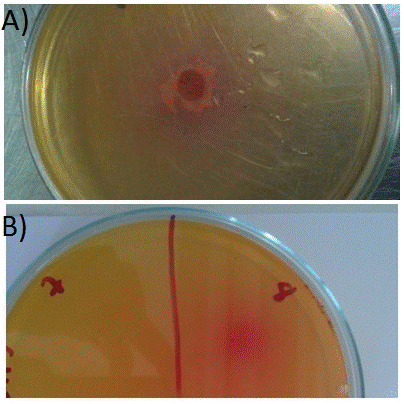
Teste qualitativo, mostrando positividade em A) para L-asparaginase e B) para L- glutaminase.
Conclusões
Apesar das condições físico-químicas do solo não serem favoráveis ao crescimento de uma vasta vegetação, este estudo mostra que a rizosfera da caatinga, possui um gama de micro-organismos com o potencial biotecnológico significativo. A partir deste estudo, observa-se que o micro-organismo analisado oferece potencial de produzir uma quantidade significativa de enzima L-asparaginase e, portanto na produção de fármacos antitumorais, entretanto são necessárias análises adicionais na quantificação e na caracterização físico-química da enzima estudada.
Agradecimentos
Referências
AZUMA, M. V. P. Actinobactérias com potencial biotecnológico. 95 f. Dissertação (Pós- Graduação) - Universidade Federal do Paraná, Curitiba, 2011.
BALAGURUNATHAN, R.; RADHAKRISHNAN, M.; SOMASUNDARAM, S.t.. L-glutaminase Producing Actinomycetes from Marine Sediments – Selective Isolation,. Australian Journal of Basic And Applied Sciences, Tamilnadu, p. 698-705. 2010.
BASHA, N Saleem et al. Production of Extracellular Anti-leukaemic Enzyme Lasparaginase. Tropical Journal Of Pharmaceutical Research, Benin City, p. 353-360. ago. 2009.
GESTO, D. S. et al. Unraveling the Enigmatic Mechanism of L Asparaginase II with QM/ QM Calculations. Journal Of The American Chemical Society. Porto, p. 7146-7158. abr. 2013.
GULATI, R.; SAXENA, R. K.; GUPTA, R. A rapid plate assay for screening L- asparaginase producing microorganisms. Letters in Applied Microbiology. 24, 23–26. 1997.
SILVA, Monique Suela et al. Brazilian Cerrado Soil Actinobacteria Ecology. Biomed Research International, Lavras, n. , p.1-10, dez. 2012.
TIZZOT, Maria Regina P. A. et al. Asparaginase [EC 3.5.1.1] de. Tuiuti: Ciência e Cultura, Curitiba, n. , p.53-72, 2005










