ISBN 978-85-85905-10-1
Área
Química Inorgânica
Autores
Medina, A.C.Q.D. (UFRN) ; Cavalcante, N.G.S. (UFRN) ; Pontes, D.L. (UFRN) ; Brito, A.C.F. (UFRN)
Resumo
A quitosana, proveniente da desacetilação da quitina, é um polímero muito utilizado em pesquisas por possuir aplicações em diversos âmbitos. Este trabalho busca purificar a quitosana comercial, produzir esferas com o polímero purificado, modificar suas estruturas químicas utilizando a vanilina e analisar sua capacidade de adsorção do complexo de cobre(II). As esferas mostraram-se solúveis apenas em meio ácido, os resultados de adsorção do complexo diclorofenantrolinacobre(II) nas esferas modificadas indicam que o sistema atinge o equilíbrio em 40 minutos.
Palavras chaves
Esferas de quitosana; Base de Schiff; Adsorção
Introdução
A quitina é facilmente encontrada na natureza, sendo constituinte do exoesqueleto de insetos e crustáceos. Após sofrer o processo de desacetilação em meio alcalino a quitina passa a ser denominada de quitosana, ambos os polímeros são atóxicos e biodegradáveis, mas possuem diferenças nas suas estruturas, no carbono dois do anel glicosídico da quitina há um grupo acetil, já na quitosana observa-se a presença do grupamento amino(BORGOGNONI,C.F. et al.,2006; SILVA, R. S. et al., 2010). A quitosana tem sido muito estudada devido às suas diversas aplicações em indústrias de cosméticos, alimentícias e farmacêuticas, na agricultura, no tratamento de água, como biocombustível, bem como sua atividade antifúngica(LIMA, I. S. et al., 2006). A quitosana pode sofrer modificações através dos grupamentos aminos livres, formando uma base de Schiff a qual é caracterizada por ser um grupo funcional no qual exista ao menos uma ligação dupla carbono-nitrogênio, onde o nitrogênio deve estar ligado a grupos arilas ou aquilas(GUO, Z. et al., 2007). A vanilina é um composto orgânico que pode ser encontrado na vagem de uma orquídea tropical denominada Vanilla planifólia, em sua estrutura existem três grupos funcionais: fenol, éter e aldeído. Essa substância tem sido objeto de estudo por possuir propriedades antimicrobianas e antioxidantes, além de atribuir aroma aos alimentos, bebidas e perfumes(PACHECO, S.M.V. et al., 2010). O objetivo desse trabalho é produzir esferas de quitosana modificada com vanilina, com posterior incorporação do cobre como centro metálico.
Material e métodos
A purificação da quitosana comercial foi feita na forma de acetato, na qual o polímero foi dissolvido em acetato de sódio e ácido acético, em seguida, a solução foi filtrada e precipitada em etanol, obtendo-se assim a quitosana purificada. As esferas foram produzidas através da dissolução da quitosana purificada em ácido acético sob agitação de 24 horas, a solução foi gotejada em solução de hidróxido de sódio e ao final as esferas formadas foram lavadas até pH neutro. A base de Schiff foi formada pelo contato das esferas com solução de vanilina durante 24 horas, posteriormente, elas foram lavadas para que o excesso de vanilina fosse retirado. A adição do diclorofenantrolinacobre(II) foi realizada por meio de um acompanhamento cinético com duração de 4 horas onde as esferas de quitosana modificadas ficaram em contato com a solução do complexo de cobre, ao total foram retiradas dezesseis alíquotas da solução e obtidos os espectros eletrônicos na região do ultravioleta e visível utilizando o espectrofotômetro Uv-visível Agilent, modelo 8453.
Resultado e discussão
O rendimento do processo da purificação da quitosana comercial foi de 85% e o
rendimento da produção das esferas foi de 76%. Um indício de que a base de
Schiff foi formada é a mudança de coloração das esferas de marrom claro para
marrom escuro ao final da modificação. O teste de solubilidade feito mostrou que
as esferas são insolúveis em água, DMSO, acetonitrila, metanol e em solução
diluída de hidróxido de sódio, nesta última observou-se que as esferas
entumeceram e ficaram com uma coloração esbranquiçada, porém, as esferas se
mostraram solúveis em solução diluída de ácido clorídrico. Na figura 2, a curva
de calibração feita com oito concentrações diferentes da solução do complexo
apresentou uma linearidade satisfatória e o gráfico concentração x tempo obtido
através do estudo cinético das esferas quitosana modificada em contato com
solução de diclorofenantrolinacobre(II) mostra que 194,1 mg de esferas de
quitosana modificada adsorveram uma concentração do complexo de 38,49mg/L e que
a adsorção tornou-se constante após 40 minutos do início.

Esferas de quitosana modificadas.
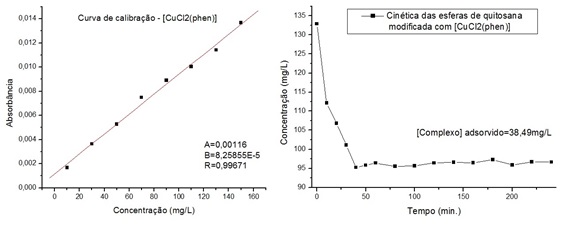
Curva de calibração do [CuCl2(phen)] e estudo cinético das esferas de quitosana modificadas.
Conclusões
Os rendimentos da purificação da quitosana comercial e da produção das esferas assemelham-se aos resultados da literatura. A mudança de cor nas esferas modificadas podem indicar uma mudança na sua estrutura. A formação da base de Schiff pode ocorrer entre o grupamento amino da quitosana com o grupamento aldeído da vanilina. Já a incorporação do complexo diclorofenantrolinacobre(II) deve ocorrer nos grupamentos metóxi. Os estudos cinéticos indicam que ocorre a incorporação do complexo com um tempo de 40 minutos.
Agradecimentos
Ao LQCPol, à UFRN e à CNPq.
Referências
BORGOGNONI, C.F.; POLAKIEWICZ, B.; PITOMBO, R.N.M.; Estabilidade de emulsões de D-Limoneno em quitosana modificada. Ciênc. Tecnol. Aliment. 26(3), 502-508, 2006.
GUO, Z.; XING, R.; LIU, S.; ZHONG, Z.; JI, X.; WANG, L.; LI, P.; Antifungal properties of Schiff bases of chitosan, N-substituted chitosan and quaternized chitosan. Carbohydr. Res. 342, 1329-1332, 2007.
LIMA, I. S.; RIBEIRO, E. S.; AIROLDI, C.; O emprego de quitosana quimicamente modificada com anidrido succínico na adsorção de azul de metileno. Quím. Nova 29(3), 501-506, 2006.
PACHECO, S.M.V.; DAMASIO, F.; Vanilina: Origem, propriedades e produção. Quím. Nova 32(4), 2010.
SILVA, R. S.; ANDRADE JR., M. A. S.; CESTARIA, A. R.; Adsorção de Cr(VI) em esferas reticuladas de quitosana – Novas correlações cinéticas e termodinâmicas utilizando microcalorimetria isotérmica contínua. Quím. Nova 33(4), 880-884, 2010.










