ISBN 978-85-85905-10-1
Área
Química Inorgânica
Autores
Paiva, A.S. (UFRN) ; Pontes, A.C.F.B. (UFRN) ; Pontes, D.L. (UFRN)
Resumo
No presente trabalho foram obtidos novos nitro complexos com Fe (III) e Cu (II) com a base de Schiff 3-MeOsalen com potencial aplicação na área biológica. Os complexos [Fe(3-MeOsalen)NO2] (1) e Na[Cu(3-MeOsalen)NO2] (2) foram caracterizados através de técnicas espectroscópicas. O espectro eletrônico do complexo 1 não apresentou a banda LMCT sugerindo a substituição do ligante cloreto presente no complexo de partida [Fe(3-MeOsalen)Cl] pelo íon nitrito. Já o composto 2 apresentou banda d-d em 532 nm, com uma variação de 30 nm para maiores energias em relação ao precursor [Cu(3-MeOsalen)H2O]. Os espectros de IV de 1 e 2 apresentaram ν assimétrico NO2 em torno de 1300 cm-1 e ν simétrico NO2 por volta de 1270 cm-1 comprovando a coordenação do íon nitrito na isomeria nitro.
Palavras chaves
complexos; base de Schiff; nitrito
Introdução
As bases de Schiff são obtidas a partir da condensação de uma amina primária com uma carbonila, a qual pode ser proveniente de cetona ou de aldeído. Uma das principais classes de base Schiff é o salen, que desempenha papéis importantes, por exemplo, na catálise e área biológica (GALIC et al, 2008). A coordenação de ligantes biologicamente ativos a centros metálicos fazem com que sua atividade seja intensificada (DEHKORDI et al, 2013), desse modo complexos com base de Schiff apresentam relevância científica e social por estarem envolvidos em pesquisa sobre intervenções terapêuticas como no tratamento de câncer e nas atividades antibacterianas (WOLDEMARIAM et al, 2008). O ligante nitrito (NO2-) é um oxiânion de nitrogênio, considerado como uma importante fonte de óxido nítrico a partir de sua conversão biológica a NO em certas condições (ZAHRAN et al, 2008). Neste contexto, compostos de coordenação com íon nitrito podem atuar como pró-droga para liberação de NO em meio biológico (BRYAN, 2006). Assim, este trabalho tem como objetivo sintetizar novos complexos de Fe (III) e Cu (II) com a base de Schiff 3-MeOsalen e o íon nitrito e caracterizá-los através de espectroscopia de absorção na região do ultravioleta e visível (Uv-Vis) e vibracional na região do infravermelho (IV).
Material e métodos
A síntese do ligante 3-MeOsalen foi realizada a partir de procedimentos similares aos descritos na literatura para o salen, a partir da orto-vanilina e etilenodiamina (ARANHA et al, 2007). As sínteses dos complexos precursores [Fe(3- MeOsalen)Cl] e [Cu(3-MeOsalen)H2O] foram realizadas a partir de 1 mmol de 3- MeOsalen solubilizados em metanol ao qual foram adicionados 1 mmol do sal do metal de interesse (FeCl3.6H2O e CuCl2.4H2O) previamente solubilizados em metanol. A solução foi mantida sob agitação constante e sob refluxo durante 2 horas. As sínteses dos complexos 1 e 2 foram realizadas em refluxo com metanol a partir de 1 mmol dos complexos precursores e de 2 mmol de NaNO2.
Resultado e discussão
O ligante 3-MeOsalen, os complexos precursores e complexos de interesse 1 e 2
foram caracterizados por Uv-Vis em metanol e IV em KBr. No espectro eletrônico
do ligante foram observadas às bandas referentes às transições do grupo imina em
324 nm (π→π*) e 421 nm (n→π*). O espectro de IV deste composto apresenta o
estiramento C=N, característico da base de Schiff, em 1632 cm-1. Para o composto
1 observou-se pequenos deslocamentos de energia nas transições intraligantes em
230, 271, 306, 352 e 428 nm, além da ausência da banda LMCT do ligante cloreto
para o metal ferro (III) em 533 nm, característica do complexo de partida. Já
no espectro eletrônico do composto 2 observou-se bandas intraligantes da base de
Schiff em 233, 279, 368 nm além de uma banda d-d em 542 nm, para a qual foi
evidenciada um deslocamento de 30 nm para menores comprimento de onda em relação
ao complexo precursor de cobre. Nos espectros de IV dos complexos 1 e 2
observaram-se bandas referentes aos estiramentos assimétricos do íon nitrito
coordenado em 1317 e 1333 cm-1 e estiramentos simétricos em 1271 e 1270 cm-1,
respectivamente. No complexo de ferro foi ainda visualizada a banda de
deformação angular ONO em 833 cm-1. A presença destas bandas no espectro de IV
do complexo indicou que a coordenação do íon nitrito ocorreu através do átomo de
nitrogênio, pois a diferença entre o estiramento assimétrico e simétrico está
abaixo de 100 cm-1.
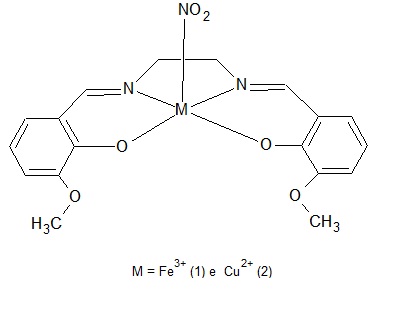
Estrutura proposta para os complexos nitros.
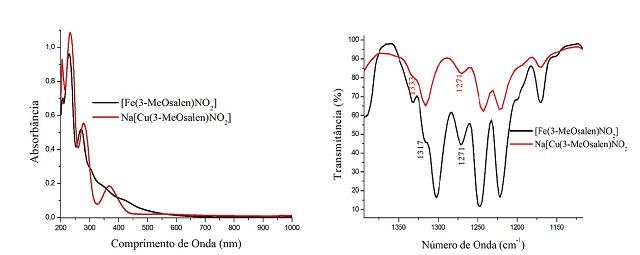
Sobreposição dos espectros eletrônicos no Uv-Vis e IV dos compostos 1 e 2 respectivamente nas cores preta e vermelha.
Conclusões
Através das técnicas espectroscópicas empregadas foi possível comprovar a obtenção dos novos complexos de Fe e Cu coordenados à base de Schiff 3-MeOsalen e ao ligante nitro. Constatou-se a coordenação dos ligantes nitros aos complexos de base de Schiff via átomo de nitrogênio devido à variação entre os estiramentos do nitrito está inferior a 100 cm-1 e ao contrapor os espectros eletrônicos dos precursores com 1 e 2 foram detectadas a ausência da banda de transferência de carga LMCT no complexo de Fe bem como o acentuado deslocamento da banda d-d no complexo de Cu.
Agradecimentos
UFRN, Instituto de Química, PPGQ-UFRN, CNPq, LQCPol.
Referências
ARANHA, P. E.; SANTOS, M. P.; ROMERA, S.; DOCKAL, Edward R. Synthesis, characterization, and spectroscopic studies of tetradentate Schiff base chromium(III) complexes Polyhedron, v. 26, p. 1373 - 1382, 2007.
BRYAN, N. S. Nitrite in nitric oxide biology: Cause or consequence? A systems-based review. Free Radical Biology & Medicine, v. 41, p. 691-701, 2006.
DEHKORDI, M. N.; LINCOLN, P. Comprehensive study on the binding of iron Schiff base complex with DNA and determining the binding mode. Journal of Fluorescence, v. 23, p. 813-821, 2013.
GALIC, N.; CIMERMAN, Z.; TOMISIC, V. Spectrometric study of tautomeric and protonation equilibria of o-vanillin Schiff base derivatives and their complexes with Cu (II). Spectrochimica Acta Part A: Molecular and Biomolecular Spectroscopy, v. 71, p. 1274-1280, 2008.
WOLDEMARIAM, G. A.; MANDAL, S. S. Iron(III)-salen damages DNA and induces apoptosis in human cell via mitochondrial pathway. Journal of Inorganic Biochemistry, v. 102, p. 740-747, 2008.
ZAHRAN, Z. N.; CHOOBACK, L.; COPELAND, D.M., West, A. N.; RICHTER-ADDO, G. B. Crystal structures of manganese- and cobalt-substituted myoglobin
in complex with NO and nitrite reveal unusual ligand conformations. Journal of Inorganic Biochemistry, v. 102, p. 216-233, 2008.










