ISBN 978-85-85905-10-1
Área
Físico-Química
Autores
Costa, A. (UFMA) ; Gomes Varela Júnior, J.J. (UFMA) ; Pereira Silva, A.L. (UFMA) ; Ramos de Macedo, E. (UFMA) ; Matos Mourão Neto, I. (UFMA)
Resumo
No presente trabalho estudaram-se os efeitos do substituinte do grupo hidroxila nas moléculas de naftaleno e azuleno. Todos os cálculos de otimização de geometria e freqüência vibracional foram realizados com o auxílio do programa Gaussian 09 utilizando a Teoria do Funcional da Densidade (DFT) com o funcional híbrido B3LYP e o conjunto de base 6-311G(d) para as moléculas naftaleno (1), mono-hidroxi-naftaleno (2), azuleno (3) e mono-hidroxi-azuleno (4). A energia total do naftaleno e azuleno tem uma relação direta com o a adição dos radicais sendo assim as moléculas 2 e 4 apresentaram uma menor energia total apresentando dessa forma os menores gap com valores muito próximos (3.579 eV) e (3.578) indicando uma instabilidade e alta reatividade.
Palavras chaves
Naftaleno; Azuleno; Energia total
Introdução
Os compostos aromáticos são importantes na indústria e desempenham papéis fundamentais na bioquímica de todos os seres vivos (K. J. DENNISTON et al, 2007). Os materiais semicondutores orgânicos, tais como, moléculas orgânicas conjugadas têm sido amplamente utilizados como materiais ativos para dispositivos óptico eletrônicos, como fotovoltaicos e células solares (G. YU, J. WANG et al, 1998) e (C. J. BRABEC et al, 2001). O naftaleno é o mais simples dos compostos da classe que chamamos de hidrocarbonetos aromáticos condensados. Considera-se esse composto como um híbrido de ressonância de três estruturas canônicas apresentando uma baixa energia de ressonância quando comparada com o benzeno. Além disso, o naftaleno apresenta uma tendência a reagir através de reações de substituição apresentando resistência às reações por adição manifestando, mais uma vez, a estabilidade aromática em relação ao benzeno (SOLOMONS, T.W.G 2003). Por outro a molécula de azuleno é estruturalmente similar á do naftaleno, porém é compreendida por 11 átomos de carbono e 9 de hidrogênios, o que confere ao azuleno propriedades físicos-químicas diferentes das observadas no naftaleno como, por exemplo, a região de emissão no espectro de UV (MILIAN TRSIC et al, 2009). No presente trabalho estudaram-se os efeitos do substituinte do grupo hidroxila nas moléculas de naftaleno e azuleno e seus derivados.
Material e métodos
Todos os cálculos de otimização de geometria e freqüência vibracional foram realizados com o auxílio do programa Gaussian 09 utilizando a Teoria do Funcional da Densidade (DFT) com o funcional híbrido B3LYP e o conjunto de base 6-311G(d) para as moléculas naftaleno (1), mono-hidroxi-naftaleno (2), azuleno (3) e mono- hidroxi-azuleno(4).
Resultado e discussão
Na Tabela 1 são mostradas as estruturas otimizadas e os parâmetros estruturais
comprimento de ligação e ângulo de ligação. A partir dos valores teóricos,
podemos constatar que os comprimentos de ligação das moléculas 1,2,3 e 4 são
ligeiramente próximos dos valores experimentais C-C (1.39 Å) C-H (1.09 Å) (Nidia
França Roque, p.74.2011) se comparados com compostos aromáticos. Enquanto que os
ângulos de ligação das moléculas 1 e 2 se aproximam dos valores calculados por
(CRUICKSHANK, 1975), em contrapartida as moléculas 3 e 4 apresentam ângulos
superiores a 120º.
A tabela 2 mostra que a energia total do naftaleno e azuleno tem uma relação
direta com o a adição dos radicais sendo assim as moléculas 2 e 4 apresentaram
uma menor energia total. Outro ponto importante corresponde às mudanças de
simetria das moléculas estudadas, sendo a molécula 3 planar com o centro de
inversão e simetria C2v (alta simetria), enquanto que molécula 4 tem simetria
CS (baixo simetria). A substituição dos grupos laterais reduziu a população dos
orbitais moleculares ocupados, isso levou a uma diminuição do gap de energia
para as moléculas com o grupo hidroxila, sendo que a molécula 1 apresentou um
maior gap (4.778 eV) mostrando-se altamente estável e com baixa reatividade
outro efeito contrário foi observado para as moléculas 2 e 4 que apresentaram
os menores gap com valores muito próximos (3.579 eV) e (3.578) indicando uma
instabilidade e alta reatividade.
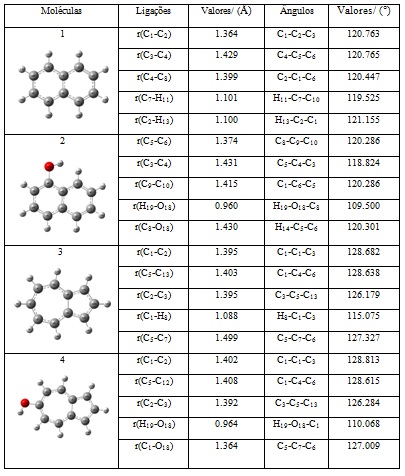
Estruturas otimizadas e os parâmetros estruturais comprimento de ligação e ângulo de ligação com funcional B3LYP e o conjunto de base 6-311G(d).
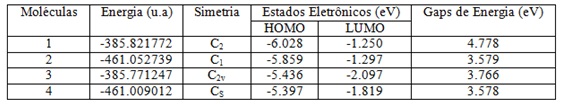
Energia total,simetria, estados eletrônicos e os gaps de energia (eV)com o funcional híbrido B3LYP e o conjunto de base 6-311G(d).
Conclusões
A metodologia empregada nos cálculos, B3LYP/6-311G(d) em nível de DFT, descreve satisfatoriamente o comportamento dos compostos de naftaleno e azuleno substituídos pela hidroxila.A energia total do naftaleno e azuleno tem uma relação direta com o a adição dos radicais sendo assim as moléculas 2 e 4 apresentaram uma menor energia total apresentando dessa forma os menores gap com valores muito próximos (3.579 eV) e (3.578) indicando uma instabilidade e alta reatividade.
Agradecimentos
A Universidade Federal do Maranhão
Referências
BY D. W. J. CRUICKSHANK.; A Detailed Refinement of the Crystal and Molecular Structure of Naphthalene . Acta Cryst. (1957). 10, 504.
C. J. BRABEC, N. S. SARICIFTCI, J. C. HUMMELEN, Adv. Funct. Mater, 11, 15, 2001.
G. YU, J. WANG, J. MC ELVAIN, A. HEEGER, Adv. Mater, 10, 1431, 1998.
NIDIA FRANÇA ROQUE.; Substâncias Orgânicas: Estruturas e Propriedades. São Paulo: Editora da Universidade de São Paulo, p.74.2011.
MILIAN TRSIC, MELISSA F. SIQUEIRA PINTO.; Química quântica:fundamentos e aplicações. Barueri, SP: Manole, p.119.2009.
K. J. DENNISTON, J.TOPPING AND T. M. DWYER, "General Organic and Biochemistry", 5th Edition, Towson University, 2007.
SOLOMONS, T.W.G; FRYHLE, C.B.; Organic Chemistry, 8th ed. John Wiley & Sons, 2003.










