ISBN 978-85-85905-10-1
Área
Físico-Química
Autores
Siara, L.R. (UEMS) ; Alves, T.S. (UEMS) ; Maximiano, E.M. (UEMS) ; Arruda, G.J. (UEMS)
Resumo
Nesse trabalho foi modificada a superfície do eletrodo de carbono vítreo com filme de nafion, para avaliar a resposta eletroquímica da oxidação do herbicida linuron sobre a superfície do eletrodo de trabalho, utilizando voltametria de varredura linear (VVL) e espectroscopia de impedância eletroquímica (EIE). Os resultados apresentaram um aumento sobre a corrente de pico, indicando uma maior sensibilidade do eletrodo com modificação, uma vez que houve a diminuição a resistência da transferência de carga e um aumento para a constante de velocidade heterogênea da reação.
Palavras chaves
IMPEDÂNCIA ELETROQUÍMICA; LINURON; NAFION
Introdução
Herbicidas representam um grande grupo de produtos químicos, uma classe de herbicidas utilizados em pré e pós-emergência é representada pelas fenilureias, em altas taxas de aplicação são úteis para matar plantas daninhas, mas a preços baixos, muitos deles podem ser utilizados para controle seletivo de ervas daninhas numa larga variedade de culturas. O linuron, 3 [3,4-(diclorofenil) -1- metoxi-1-metil-ureia], é uma das mais importantes ureias comerciais (USEPA, 1995). Devido à ausência de atividade microbiana, os processos de degradação são muito lentos e sua acumulação pode facilmente levar a níveis tóxicos (GROVER et al, 1980). A capacidade de pré-concentração dos eletrodos modificados com filmes finos de polímeros de troca iônica foi descrita em estudos do começo da década de 80 (OYAMA et al, 1980). Nesta técnica usam-se eletrodos sólidos, coberto com um filme fino do polímero trocador de íon, o qual permite uma, detecção voltamétrica simultânea e rápida do íon analito eletroativo (WANG,1992). O nafion consiste de um polímero perfluorado com unidades de tetrafluorpolietileno (n = 5 a 13), ligado a um éter, que por sua vez está ligado a um ácido sulfônico. É um ionômero perfluoro-sulfonatado polianionico, que tem a capacidade de acumular cátions (ESPENSCHEID et al,1986). A permeabilidade seletiva do nafion também resulta da natureza polianiônica do filme, a qual faz uma barreira para ânions e de sua estrutura microscópica de canais estreitos que evita a penetração de moléculas volumosas (HSU et al, 1983). Esse trabalho tem como objetivo estudar a resposta eletroquímica do herbicida linuron, sob a superfície do eletrodo de carbono vítreo como eletrodo de trabalho modificando a superfície com filme de nafion.
Material e métodos
Para as medidas eletroquímicas, utilizou-se uma célula eletroquímica com 3 eletrodos e capacidade de 25 mL. Os eletrodos de fio de platina, (Ag/AgCl) e eletrodo de carbono vítreo com área geométrica de 0,190 cm2, foram utilizados como eletrodo auxiliar, referência e de trabalho, respectivamente. O eletrodo de carbono vítreo foi previamente limpo em feltro umedecido com solução de alumina 0,3 µm numa politriz e levado em banho ultrassônico em álcool etílico absoluto (99,8%), água destilada e ácido nítrico (0,1%) respectivamente, durante 3 minutos em cada etapa. O filme de nafion na superfície do eletrodo de carbono vítreo foi obtido adicionando 20µL da solução de nafion (0,1%), na superfície do eletrodo já limpo secando a temperatura ambiente, representando a quantidade de nafion de 221 µg cm-2 na superfície do eletrodo. A solução de estoque de linuron (Riedel-deHaën®),com pureza de 99,7%, foi preparada pela dissolução do padrão em 70:30% (água:acetonitrila). Para as medidas eletroquímicas em VVL foi utilizada uma solução de linuron com concentração de 62 ppm na célula. As medidas em EIE foram utilizadas uma solução de ferricianeto de potássio K3[Fe(CN)6] a uma concentração de 1 mM, e como eletrólito de suporte foi utilizado H2SO4 (0,02 M).As medidas eletroquímicas foram obtidas após 10 minutos de purga de nitrogênio com pureza de 99,999%, em um Potenciostato/Galvanostato AUTOLAB PGSTAT 128N interfaciado a um computador e gerenciado pelo software NOVA 1.10 para aquisição e tratamento dos dados.
Resultado e discussão
A figura 1A mostra os voltamogramas obtidos em VVL, realizados em uma solução de
linuron de 62 ppm, utilizando eletrodos de carbono vítreo sem modificação (CV-
SM) e com modificação (CV-CM). Observa-se a presença de
um pico de oxidação em ambos os voltamogramas, esse pico pode ser atribuído à
oxidação eletroquímica do linuron através da perda de grupos metoxi e metila.
Este inicialmente envolve a eliminação do grupo metoxi (substituído por um átomo
de hidrogênio), através da formação de 3-(3,4-diclorofenil)-1-metilureia e ácido
fórmico (DORDEVIC et al., 2012). Os resultados obtidos em VVL apresentam um
aumento acima de 500% na intensidade do pico (Tabela 1). A Figura 1B representa
o diagrama de Nyquist e o circuito [Rs(Cdc[RtcW])], onde Rs resistência da
solução, Cdc capacitância da dupla camada e Rtc resistência de transferência de
carga. Os valores de Rtc foram de 788.81Ω para CV-SM e 422.17Ω para CV-CM. A
constante de velocidade heterogênea padrão foi estimada através da equação:
k0 =
(RT)/(n2F2 A Rtc C), onde R constante universal dos gases,
T temperatura em K, F
constante de Faraday, A área do eletrodo, e C concentração de K3
[Fe(CN)6] na
célula, obtendo valores de 1,776 e 3,319 μcm s-1 em CV-SM e CV-CM
respectivamente. A presença do filme de nafion na interface eletrodo/solução
provoca uma diminuição da resistência à transferência eletrônica, favorecendo a
mesma, entre o linuron e eletrodo de trabalho.
(A) VVL CV-SM e CV-CM, concentração linuron 62 ppm. (B) EIE obtidos de uma solução de K3[Fe(CN)6] 1 mM em H2SO4.
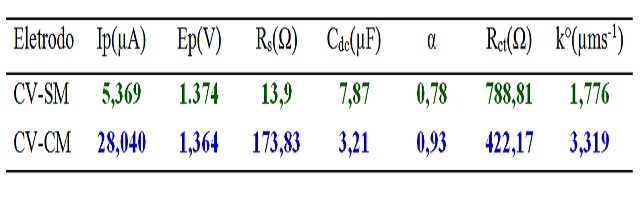
Tabela de valores de Ip, Ep, Rs, Cdc, Rct e k°, extraidos das figuras 1A e 1B.
Conclusões
Os resultados obtidos mostraram que a presença do filme de nafion na superfície do eletrodo de carbono vítreo provoca uma diminuição a resistência da transferência de carga, o que acarretou no aumento de 187% para a constante de velocidade heterogênea da reação e o aumento superior a 500% sobre a corrente de pico. Mostrando assim uma resposta positiva para a utilização da metodologia de modificação da superfície do eletrodo de carbono vítreo para estudos eletroquímicos do linuron.
Agradecimentos
UEMS (Universidade Estadual de Mato Grosso do Sul)
Referências
DORDEVIC, J. PAPP, Z. GUZSVÁNY, V. SVANCARA, I. Sensors 12 (2012) 148-161.
ESPENSCHEID, T.M.; CHATAK ROY, A.R.; MOORE III, R.B.; PENNER R.M.; SZENTIRMAY, M.N.; MARTIN, C.R. J. Chem. Soc. Faraday Trans I. 1986, (82), 1051.
GROVER, R.; SMITH, A.E.; KORVEN. H.V.; Can. J. Plant Sci. 60 (1980) 185.
HOYER, B.; FLORENCE, T. M.; Anal. Chem. 1987, 59, 2839.
HSU, W.Y.; GIERKE,T.D. J. Membr. Sct., 1983, (13), 307.
OYAMA, N.; ANSON, F. C.; J. Electrochem. Soc. 1980,127, 247.
USEPA, Reregistration Eligibility Decision (RED), Linuron, 1995 (EPA/NCEPI).
WANG, J. In Electroanalytical Chemistry; Bard, A. J., Ed.;Marcell Dekker; New York, 1992; v. 16, p1.










