ISBN 978-85-85905-10-1
Área
Química Analítica
Autores
Cabral, A.M. (UNIVERSIDADE FEDERAL DO RIO GRANDE DO NORTE) ; Moura, M.F.V. (UNIVERSIDADE FEDERAL DO RIO GRANDE DO NORTE) ; Silva, D.R. (UNIVERSIDADE FEDERAL DO RIO GRANDE DO NORTE)
Resumo
Este trabalho desenvolve um método para identificação de Tetraciclina (TC) e epi – tetraciclina (epi-TC) em medicamentos veterinários a base de ácido ascórbico (AA) e ácido ascórbico (AA), L-ascórbico (LAA) e D-iso-ascórbico (DIAA), utilizando cromatografia líquida de ultra eficiência com arranjo de fotodiodos (UFLC-DAD). A separação cromatográfica foi realizada em modo gradiente utilizando coluna de fase reversa de C8 (4,6 mm x 25 cm, 5 μm). A composição da fase móvel de Água: Acetonitrila foi 80:20 (v/v) e fluxo de 1 mLmin-1. Considerando, resolução de (0,80 – 0,96) e seletividade de (2 – 2,44) em nível de confiança de 95 %, os resultados mostraram que o método é adequado para identificação de TC em 1,6 min, epi-TC (1,5 min), LAA (1,38 min) e DIAA (1,45 min).
Palavras chaves
UFLC-DAD; Ácido Ascórbico; Tetraciclina
Introdução
O controle de qualidade dos fármacos de uso veterinário é essencial para garantia da sua eficiência terapêutica, estabilidade e garantia da ausência de resíduos em alimentos expostos ao consumo humano. Os fatores que alteram a qualidade dos medicamentos são: temperatura de armazenagem, luz, umidade, radiações ionizantes e os tipos de embalagens (EUROPEAN COMMISSION, 2006; MINISTÉRIO DA AGRICULTURA PECUÁRIA E ABASTECIMENTO, 2012). A associação de antioxidantes a fórmulas contendo tetraciclinas é comum, quando deseja-se prevenir reações que ocorrem em medicamentos deste grupo. Na indústria farmacêutica existem muitas aplicações técnicas prevenir mecanismos oxidativos uma delas é a adição do ácido ascórbico, principalmente quando é utilizado para compensar perdas no armazenamento, aumentando a data de validade e também para preservar a integridade do produto refletindo na sua qualidade (BAJAJ., SINGLA., SAKHUJA, 2012). A tetraciclina como base livre é insolúvel em água, para ser dissolvida e formar uma solução é necessário deve ser convertida em sal do seu ácido (cloridrato de tetraciclina), porém a solução não é considerada estável durante um determinado tempo, desta maneira o ajuste de pH é necessário (J. H. BOOTHE., A. GREEN., J. P. PETISI., 1953; RITTER LAWRENCE., 1957). As indústrias farmacêuticas adicionam ácido ascórbico para conferir estabilidade biológica e torna-la apta a ser administrada ao organismo. Este trabalho desenvolve um método para identificação de Tetraciclina (TC) e epímero da tetraciclina (epi-TC) em medicamentos veterinários a base de ácido ascórbico e isômeros ácido L-ascórbico (LAA) e ácido D-iso-ascórbico (DIAA) utilizando cromatografia líquida de rápida eficiência com arranjo de fotodiodos (UFLC-DAD).
Material e métodos
1. Reagentes e Soluções Todos os reagentes utilizados foram grau HPLC acetonitrila fabricado por Merck (). Soluções injetáveis de medicamentos antimicrobianos foram filtradas em nylon (13 mm x 0,45 μm). Os procedimentos de preparo estão descritos em Farmacopeia Americana. A concentração da solução trabalho TC é 50 µgmL e AA de 30 µgmL. As faixas de concentrações das soluções são descritas Sequência 1 e 2, respectivamente. AA (0,3 e 0,15 µgmL) e TC (0,5 e 0,25 µgmL). As soluções têm sido preparadas por adição de padrão externo solução e diluído em água (resistividade > 16 MΩ). 1.2 Condições do Sistema Cromatográfico As análises foram realizadas em sistema cromatográfico UFLC-DAD modelo LC-20 ® e coluna de fase reversa de C8 (4,6 mm x 25 cm, 5 μm) e de injeção por loop. Os Parâmetros cromatográficos foram testados para composição da fase móvel e água e acetonitrila (50:50), (70:30), (80:20) e (90:10) e fluxo (0,1 – 1 mLmin-1), respectivamente. O gradiente binário constitui-se de água e acetonitrila 80:20 (v/v). A melhor condição para fluxo é de 1 mLmin a temperatura constante de 25 °C. O detector utilizado foi com arranjo de fotodiodos, o comprimento de onda foi selecionado de acordo com o máximo de absorbância para cada família de beta-lactâmicos de 220, 370 e 450 nm.
Resultado e discussão
O planejamento das condições cromatográficas foi realizado para aumentar a resolução dos picos investigados e evitar interferentes e sobreposição. Os melhores resultados foram obtidos utilizando a fase móvel de água: acetonitrila 80:20 (v/v) e fluxo de 1 mLmin. Os comprimentos de onda de detecção de foram estudados no intervalo entre 190 e 800 nm. A intensidade máxima TC foi trabalhado em 220, 370 e 450 nm. Andersen et al., 2005 enfatizam que tetraciclinas são susceptíveis a formar quatro epímeros em função do pH e da temperatura. Fox, Smith, Bitler, Reichenthal, & Origoni, 1954 mostram que TCs podem sofrer uma epimerização reversível em quatro de carbono para formar uma nova série de compostos, as 4-epi-tetraciclinas. Desta forma, o cromatograma da Figura 1 mostra picos menos intensos de epi – TC em 1,5 min. A seletividade foi confirmada pela ausência de interferentes de picos sobrepostos. O procedimento utilizando coluna em fase reversa C8 e eluição por gradiente é satisfatório oferece um bom desempenho. A Resolução adequada entre todos os picos TC é alcançado dentro do tempo de análise relativamente curto entre (1,55 – 1,7 min), para os agentes antioxidantes LAA e DIIA o tempo de retenção de 1,38 e 1,45 min, respectivamente. Considerando, a resolução de (0,80 – 0,96) e seletividade de (2 – 2,44), os procedimentos em limite de confiança de 95 % têm sido adequados para identificação de TC, epi – TC em presença de LAA e DIAA.
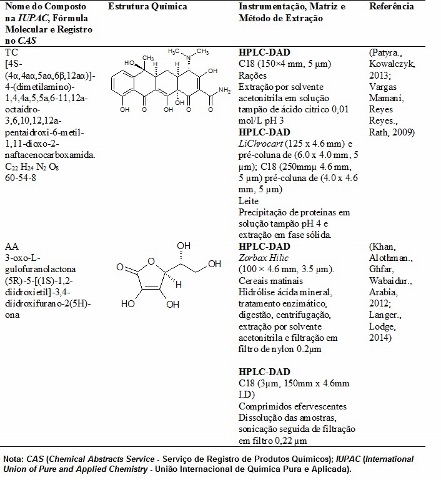
A Tabela 1 mostra um estudo das principais condições para identificação dos compostos analisados.
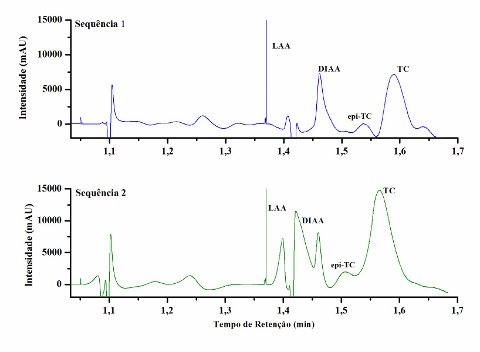
A Figura 1 mostra a separação em tempos de retenção curtos para LAA (1,38 min) DIIA (1,45 min), epi – TC (1,55 min) e TC (1,6 min).
Conclusões
A qualidade dos medicamentos veterinários usados em animais produtores de alimentos reflete na valorização da matéria-prima, toxidade e principalmente na segurança dos alimentos. O método desenvolvido tem demostrado ser apto para identificação de Tetraciclina e epímeros, presentes em soluções injetáveis a base de ácido ascórbico. Os resultados mostraram que o método alia a especificidade, com sensibilidade, reprodutibilidade, custo-efetividade e rápida obtenção do sinal analítico da substância em estudo, após planejamento das condições cromatográficas.
Agradecimentos
Os autores agradecem CAPES,PPGQ, IQ e UFRN, pelo suporte.
Referências
W. C., Andersen, J. E., Roybal, S.A., Gonzales., S.B., Turnipseed, A. P., fenning, L.R., Kuck, L. R. Determination of tetracycline residues in shrimp and whole milk using liquid chromatography with ultraviolet detection and residue confirmation by mass spectrometry. Analytica Chimica Acta, nº 529, 1-2, 145–150, 2005.
S.C., Bajaj, D., Singla, N., Sakhuja. Stability Testing of Pharmaceutical Products, nº 02, 129–138, 2012.
European Commission. Commission Directive 2006/130/EC of 11 December 2006 implementing. Official Journal of the European Union, 15–16, 2006.
M., Fox, L., Smith, A., Bitler, J., Reichenthal,V., Origoni. Studies of the Reversible Epimerization Occurring in the Tetracycline Family. The Preparation, Properties and Proof of Structure of Some 4-epi-Tetracyclines, nº 4981, 9, 1954.
J. H., Boothe, A., Green, J. P., R.G., Petisi. Demethyltetracyclines Synthesis of a degradation product. Journal American Chemical Society, nº 1710, 1, 11952, 1953.
M.R., Khan,Z.A., Alothman, A.A., Ghfar, S.M., Wabaidur, S., Arabia. Simultaneous analysis of vitamin c and aspirin in aspirin c effervescent tablets by high performance liquid chromatography–photodiode array detector, 2454–2461, 2012.
S., Langer, J.K, Lodge. Determination of selected water-soluble vitamins using hydrophilic chromatography : A comparison of photodiode array, fluorescence , and coulometric detection , and validation in a breakfast cereal matrix. Journal of Chromatography B, nº 960, 73–81, 2014.
Ministério da Agricultura Pecuária e Abastecimento. (2012). Legislação relacionada aos produtos de uso veterinário.
E., Patyra, E., Kowalczyk Development and validation method for the determination of selected tetracyclines in animal medicated feedingstuffs with the use of micellar liquid chromatography, 6799–6806, 2013.
R.B., Polec., S.D., Yell, A.E., Sells, A. E. Divwion of Medwal Research, Sloan-Kettering Institute for Cancer Research and Departments of Medkine, Memorial Hospital and Cornell University, 1969.
Ritter Lawrence. United. States Patent (2803657) Acid Stabilized Tetracycline Salts, 1957.
M.C., Vargas Mamani, F.G., Reyes Reyes, S., Rath. Multiresidue determination of tetracyclines, sulphonamides and chloramphenicol in bovine milk using HPLC-DAD. Food Chemistry, nº 117, 3, 545–552, 2009.










