ISBN 978-85-85905-10-1
Área
Química Analítica
Autores
Sousa, F.W.N. (CESC/UEMA) ; Sousa, M.S. (CESC/UEMA) ; Neto, J.P.C. (CESC/UEMA) ; Nunes, P.M. (CESC/UEMA) ; Oliveira, S.S. (CESC/UEMA) ; Soares, A.C.F. (CESC/UEMA) ; Freire, J.S. (CESC/UEMA)
Resumo
A água oxigenada comercializada contém determinada quantidade de peróxido de hidrogênio. Apesar das concentrações virem expressas nos produtos, onde a amostra selecionada expressava um valor de 3% e 10 volumes respectivamente, isso não nos permite confirmar se a % em volume de peróxido de hidrogênio e o número de volumes indicados no rótulo correspondem ao valor real. O presente estudo foi realizado para desenvolver uma nova metodologia com utilização da técnica de Quimiluminescência adaptada a um dispositivo portátil inibidor da passagem de luz que qualifica ainda mais esse novo método. Conclui-se que o método quimiluminescente além de ser um método prático, rápido e versátil também demonstrou a sua excelente eficácia quando posto em prática.
Palavras chaves
Peróxido de hidrogênio; Metodologia; Quimiluminescência.
Introdução
O peróxido de hidrogênio que se decompõe sob ação da luz e do calor necessita de uma determinação do seu teor real de peróxido de hidrogênio em uma amostra de água oxigenada. Podendo estes ser determinados por volumetria, espectrofotometria, quimiluminescência, algumas vezes com o emprego de fibra óptica, cromatografia e por métodos eletroquímicos. (MATTOS, 2003). Sabe-se que o peróxido de hidrogênio é um agente oxidante, onde, quando utilizado para uma análise volumétrica, tem-se uma reação de oxidação e redução. Os agentes oxidantes e redutores devem ser estáveis no solvente usado – geralmente água – e a substância que se deseja determinar deve estar em um estado de oxidação definido e estável, antes de se iniciar a titulação. Para se ter sucesso em um método volumétrico, é necessário também que os métodos de preparação de soluções padrão sejam disponíveis e que exista um meio adequado de se detectar o ponto final da reação (BACCAN, 1979). Baseado nos resultados obtidos em uma determinação volumétrica (permaganimetria), o presente trabalho visa elaborar uma nova metodologia para determinar o teor de peróxido de hidrogênio em água oxigenada utilizadas em formulações farmacêuticas a partir do desenvolvimento de um novo método onde haverá a reação entre o peróxido de hidrogênio e um reagente quimiluminescente que irá produzir luminosidade onde será captada por um dispositivo luxímetro que medirá as quantidades em lux (unidade de medida do luxímetro) advindas de cada concentração de peróxido de hidrogênio. O método proposto será uma forma fácil e prática para a determinação de peróxido de hidrogênio em formulações farmacêutica, onde o mesmo pelo fato de não consumir muito tempo até o término da determinação, diminui as possibilidades de decomposição da amostra.
Material e métodos
As coletas das águas oxigenadas foram adquiridas no comércio farmacêutico de Caxias-MA, sob a forma de solução de 100ml. Optou-se pela coleta de três amostras de água oxigenadas 10V que possuíam marcas distintas, onde ficarão acondicionadas à temperatura baixas para que não haja decomposição. Fez-se o uso das seguintes soluções para realização do trabalho; solução de oxalato de sódio 0,02 M; solução de permanganato de potássio 0,02 mol/ (onde se fez a padronização da solução de permanganato de potássio KMnO4 por permanganimetria na qual verificou-se a determinação do teor de H2O2 na amostra); a solução de hidróxido de sódio foi preparada da seguinte forma pesou-se cerca de 4,0 g de hidróxido de sódio puro em balança analítica de precisão e adicionou-se em água e completou-se para um balão volumétrico de 1 litro. A quimiluminescência consiste num método prático e rápido de análises de amostras, na qual foi montado um sistema composto das seguintes instrumentações analíticas e materiais: caixa isoladora de luminosidade e espelhada de 20 cm x 10 cm, onde foi feita adaptação do luxímetro para caixa plástica com o tubo de ensaio para análise do sistema, agitador de tubos de ensaio. O sistema será basicamente assim: serão inseridos no tubo de ensaio a amostra contendo peróxido de hidrogênio e o reagente quimiluminescente onde os mesmo são agitados para homogeneizar-se e reagirem. Em seguida mediu-se a quantidade de lux produzida no luxímetro, e subsequentemente será adicionado o catalisador e novamente agitaram-se e mediram a quantidade de lux produzida no luxímetro. Assim será proposto a serem realizadas os mesmos procedimentos em todas as amostras com diferentes concentrações.
Resultado e discussão
A curva de calibração foi elaborada a partir de um software denominado ORIGIN
PRO 8 que estabelece os valores no eixo x correspondente a concentração de
peróxido em porcentagem e no eixo y a quantidade de lux capitada pelo luxímetro.
Baseado no gráfico anterior verifica-se uma boa linearidade desse método devido
ao valor do R, mostrando que o método utilizado é bem satisfatório. À medida que
o coeficiente de correlação obtido aproxima-se da unidade, mais o método
tornando-se confiável.
Peróxido de hidrogênio nas amostras farmacêuticas
As análises tiveram início com o recolhimento das amostras, que ao total foram 3
(três) de diferentes marcas de águas oxigenadas que continham peróxido de
hidrogênio com concentração aproximada a 3%. Na qual foram rotuladas
aleatoriamente como MARCA A, MARCA B, MARCA C. Desse momento em diante deu-se
início de fato aos procedimentos analíticos a fim de verificar se são ou não
verdadeiras as informações apresentadas nas embalagens destes produtos a
respeito da presença de peróxido de hidrogênio. As análises da amostra A foram
descritas anteriormente e utilizadas para a construção da curva de calibração.
Amostra B: foi retida uma alíquota de 2µL da amostra de peróxido de hidrogênio e
sujeitou-a a determinação quimiluminescente onde obteve um resultado em lux
igual a 248 lux e de acordo com a equação da reta Lux = 87,36228. C +
(-4,90873) obtivemos a concentração de acordo com os parâmetros desejados.
Amostra C: foi retida uma alíquota de 2µL da amostra de peróxido de hidrogênio e
sujeitou-a a determinação quimiluminescente onde obteve um resultado em lux
igual a 245 lux e de acordo com a equação da reta Lux = 87,36228.C +
(-4,90873) obtivemos a concentração de acordo com os parâmetros desejados.
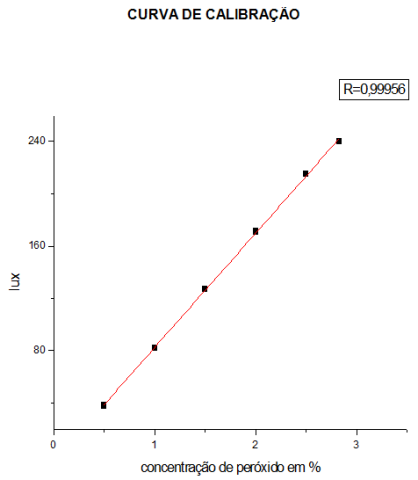
Gráfico 1 - Curva de calibração do luxímetro com o lux em função da concentração de peróxido em %.
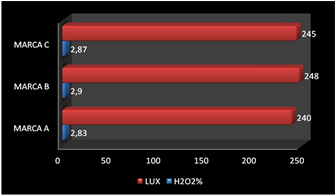
Gráfico 2: quantidades de peróxido com relação ao lux nas amostras analisadas.
Conclusões
Pôde-se observar com os resultados que a marca B continha a maior quantidade de peróxido e a marca A com menor concentração, isso devidamente visto com a quantidade de lux produzido por cada uma. O que demonstrou que quanto maior a concentração de peróxido maior seria a quantidade lux produzido caracterizando um paralelo entre lux e concentração de peróxido. A técnica teve uma maior confiabilidade, pois foi baseado de acordo com uma determinação titulométrica e a mesma se comportou de forma excelente em amostras ainda não determinadas.
Agradecimentos
CESC-UEMA
Referências
BACCAN, N. Química Analítica Quantitativa Elementar. 1. ed. São Paulo: Edgard Blücher, p. 191-192, 1979
MATTOS,Ivanildo Luiz; SHIRAISHI,Karina Antonelli; BRAZ,Alexandre Delfhini;FERNANDES,João Roberto.Peróxido de hidrogênio:Importância e determinação.Quim.Nova,vol.26,No.3,2003.










