ISBN 978-85-85905-10-1
Área
Química Analítica
Autores
Oliveira, S.D.S. (UFRN) ; Martinez-huitle, C.A. (UFRN)
Resumo
A tuberculose (TB) continua sendo um grave problema de saúde publica, especialmente em países em desenvolvimento. O tratamento da TB consiste na administração de uma combinação de fármacos: isoniazida, etambutol, rifampicina e pirazinamida. A isoniazida (INH), quando convertida, torna-se um metabólito ativo que inibe a síntese do ácido micólico. Neste trabalho, utiliza-se a voltametria de pulso diferencial (DPV), usando o diamante dopado com boro (BDD), para a obtenção do perfil eletroquímico da INH. Em pH 4 e pH 8, as curvas analíticas para a INH apresentaram boa linearidade, tendo os limites de quantificação de 6,15 μM (0,844 ppm) e 4,08 μM (0,560 ppm), para os respectivos pH. Com os resultados, o método proposto pode ser usado para a determinação de INH em combinações farmacêuticas.
Palavras chaves
Isoniazida; Diamante Dopado com Boro; DPV
Introdução
A tuberculose (TB) é uma doença infecciosa causada pelo Mycobacterium tuberculosis ou bacilo de Koch, em homenagem ao bacteriologista alemão Robert Koch, descobridor da bactéria [1]. A grave situação mundial da tuberculose está intimamente ligada ao aumento da pobreza, à má distribuição de renda e à urbanização acelerada [2]. No Brasil, a TB afeta principalmente as periferias urbanas e está associada, geralmente, às más condições de moradia e alimentação, à falta de saneamento básico e outros. A isoniazida (INH) é um pró-farmaco que continua sendo o principal agente para a quimioterapia da TB. A enzima catalase- peroxidase micobacteriana converte a isoniazida em um metabólito ativo que age inibindo a síntese do ácido micólico, peculiar na formação da parede celular do bacilo [3]. A INH é bacteriostática para os bacilos “em repouso”, mas tem atividade bactericida para os microrganismos em rápida divisão [4]. Vários trabalhos foram realizados para determinação da isoniazida utilizando técnicas eletroquímicas, porém nenhum estudo foi feito utilizando o eletrodo de diamante dopado com boro (BDD, do inglês Boron-Doped Diamond) como eletrodo de trabalho. O diamante é um material muito promissor devido à janela de potencial desse material é incomparavelmente maior do que a de qualquer outro material, podendo atingir valores próximos a 3 volts ou ainda maiores [5]. Neste trabalho foi utilizado um eletrodo de diamante dopado com boro como eletrodo de trabalho, a técnica de voltametria cíclica para estudo do perfil eletroquímico e o uso da voltametria de pulso diferencial para analisar a possibilidade de utilização desse método para quantificar o fármaco isoniazida em formulações farmacêuticas, como também comparar os resultados obtidos nos pH 4 e 8.
Material e métodos
Aparelhos: As medidas voltamétricas foram realizadas em uma cela eletroquímica com capacidade total de 100 mL conectado ao Potenciostato/Galvanostato Autolab PGSTAT 302 (Eco Chimie), constituído por três eletrodos: eletrodo de diamante dopado com boro (A = 1,54 cm2), como eletrodo de trabalho; Ag/AgCl, como eletrodo de referência e platina como eletrodo auxiliar. O potenciostato é gerenciado pelo programa computacional GPES 4.9. O eletrólito de suporte utilizado foi KCl 0,1 mol L-1 e ajustado para os pH 4 e 8. Ativação do Eletrodo: foi realizado um pré-tratamento catódico do eletrodo de diamante, aplicando-se o potencial de -3000 mV durante 1800 segundos. Procedimento Analítico: a) Preparação da Solução de INH: A solução padrão de INH 0,05 mol L-1 foi preparada com 0,0686 g (50 mmol) dissolvidos em 10 mL de KCl 0,1 mol L-1. c) Determinação da Faixa Linear da Resposta do Eletrodo com a Concentração de INH: As medidas eletroquímicas foram feitas depois do pré-tratamento catódico do eletrodo de diamante e sua limpeza. As determinações realizadas através de voltametria de pulso diferencial foram realizadas considerando os seguintes parâmetros experimentais: faixa de -250 a 1700 mV; modulação de amplitude, 50 mV. Para a voltametria cíclica utilizou-se os seguintes parâmetros experimentais: faixa de -250 a 1700 mV; velocidade de varredura, 100 mV s-1 para o eletrodo de diamante. Foram colocados 20 mL do eletrólito suporte na cela eletroquímica e determinados volumes da solução padrão de isoniazida foram adicionados posteriormente. A determinação da faixa linear de trabalho e das curvas analíticas para os pH 4 e 8, foram obtidas com adições da solução padrão de isoniazida 0,05 mol L-1 ao eletrólito suporte com o auxílio de uma micropipeta de volume variável de 10-100 μL.
Resultado e discussão
Para o estudo da relação corrente vs concentração de analito foi utilizado a
DPV, devido a maior sensibilidade desta técnica e por permitir uma melhor
determinação dos valores de corrente de pico. O voltamograma da INH, obtido
através da DPV e utilizando eletrodo de BDD, apresentou apenas um pico
irreversível com potencial próximo à 1,16 V. Comparando os voltamogramas obtidos
em pH 4 e 8, apresentados na Figura 01, observa-se um deslocamento de 0,143 V
para regiões de corrente mais positivas devido a forma protonada presente no pH
4 ou da forma não protonada presente no pH 8 da isoniazida em solução, mostrando
maior eletroatividade para a superfície do eletrodo. As curvas analíticas em pH
4 e 8 foram obtidas através da adição de padrão de 100 a 800 μL (0,249 a 1,92 M)
utilizando a DPV em KCl 0,1 M. A Figura 02 apresenta os voltamogramas de DPV
para a INH em pH 4. Observa-se um incremento da corrente na medida em que a
concentração de isoniazida aumenta. Observou-se uma boa linearidade para a curva
analítica, pois o fator de correlação linear (R2) foi próximo de 1. Enquanto que
para as curvas analíticas para pH 8 foi observado que a INH não mantêm a relação
de linearidade nas duas últimas adições. Foi observado que com o aumento da
concentração aumenta a corrente do pico, mantendo uma boa dependência linear, em
ambos os valores de pH, gerando as seguintes equações de reta das curvas
analíticas:
pH 4 = i (μA)=4,73+75,4 C_isoniazida (r = 0,998);
pH 8 = i (μA)=4,46+66,9 C_isoniazida (r = 0,993);
Os limites de detecção obtidos para o pH 4 e pH 8 foram 1,85 M (0,253
ppm) e 1,23 M (0,169 ppm), respectivamente. Enquanto que os limites de
quantificação obtidos para o pH 4 e pH 8 foram 0,00615 mM (0,844 ppm) e 0,00408
mM (0,560 ppm), respectivamente.
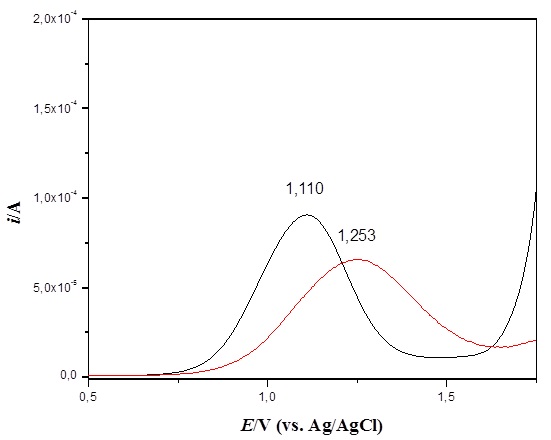
Voltamogramas de pulso diferencial da solução padrão de INH 0,0980 M em 0,1M KCl: linha preta: pH 4;linha vermelha: pH 8.Modulação de amplitude:0,050
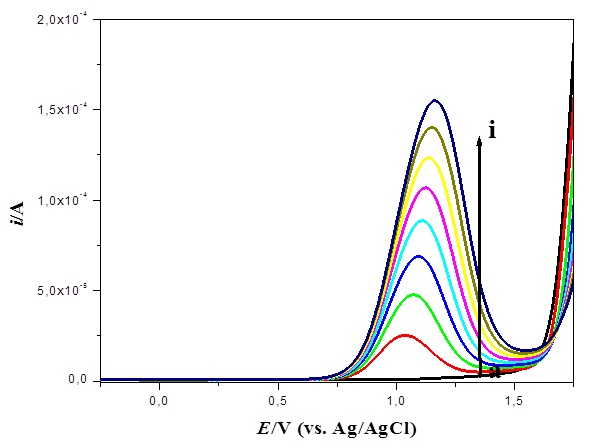
Voltamogramas de INH em 0,1M KCl pH 4, adição:(a)0 M;(b)0,249 mM;(c)0,495 M;(d)0,739 mM;(e)0,980mM;(f)1,22 mM;(g)1,46 mM;(h)1,69 mM;(i)1,92 mM
Conclusões
Com a técnica VDP é possível observar o perfil do fármaco INH.A INH apresenta um deslocamento de 0,143 V para regiões de corrente de pico mais positivas quando comparado os voltamogramas dos pH de 4 e 8.Em pH 4, a curva analítica apresentou boa linearidade, enquanto que em pH 8, a INH não mantêm a linearidade em altas concentrações (> 0,169 M. Os limites de quantificação obtidos para o pH 4 e pH 8 foram 0,00615 mM (0,844 ppm) e 0,00408 mM (0,560 ppm), respectivamente. Dessa forma, essa técnica apresentou-se como um potencial método para a determinação de INH em formulações farmacêuticas
Agradecimentos
À Capes pela bolsa concedida.
Referências
[1] ARAGUAIA, M. Tuberculose. Brasil Escola.
Disponível em: <http://www.brasilescola.com/doencas/tuberculose.htm> Acesso em: 06 abr. 2013.
[2] HIJJAR, M. A.; OLIVEIRA, M. J. P. R.; TEIXEIRA, G. M. A Tuberculose no Brasil e no mundo. Boletim de Pneumologia Sanitária, v. 9, n. 2, p. 9-16, 2001.
[3] JUNIOR, S.V.C. Técnicas de caracterização de polímeros. Editora Artiliber, p.17-261, 2004.
[4] BLANCHARD, J. S. Molecular mechanisms of drug resistance in mycobacterium tuberculosis. Annual Review of Biochemistry, v. 65, p. 215-239, 1996.
[5] PLESKOV, Y. Electrochemistry of diamond. In: BRILLAS, E.; MARTÍNEZ-HUITLE, C. A. Synthetic Diamond Films: Preparation, Electrochemistry, Characterization and Applications. p. 79-108. New Jersey: John Wiley e Sons, 2011.










