ISBN 978-85-85905-10-1
Área
Química Tecnológica
Autores
Vieira, M.L.G. (FURG) ; Gonçalves, J.O. (FURG) ; Piva, T. (FURG) ; Oppelt, A.P. (FURG) ; Vieira, V.A. (FURG) ; Pinto, L.A.A. (FURG)
Resumo
O corante amarelo crepúsculo é um aditivo muito utilizado na indústria de alimentos. Este é responsável por melhorar a aparência dos produtos, no entanto, pode estar contido nos efluentes destas indústrias e necessita de um tratamento específico. Neste caso, pode-se citar a adsorção em colunas de leito fixo, as quais se destacam pelo tratamento destes efluentes de forma contínua e por serem de simples operação. O objetivo deste trabalho foi utilizar esferas recobertas com quitosana como preenchimento de coluna de leito fixo para a adsorção do corante amarelo crepúsculo. O comportamento da adsorção do corante amarelo crepúsculo foi avaliado através da obtenção de curvas de ruptura experimentais. O efeito da vazão de alimentação sobre a capacidade máxima de adsorção da coluna foi analisado.
Palavras chaves
adsorção; corante alimentício; curva de ruptura
Introdução
A quitosana tem sido aplicada em diversas áreas, como biomédica, farmacêutica, ambiental, indústria química e alimentícia. Em relação a sua utilização como adsorvente no tratamento de águas residuais, a quitosana mostra-se adequada devido aos elevados percentuais de remoção e afinidade com diversos corantes (CRINI; BADOT, 2008). Devido às baixas taxas de fixação, corantes estão contidos em efluentes industriais, dentre eles pode-se citar o amarelo crepúsculo que é um dos mais utilizados no processamento de alimentos, tais como gelatinas, sorvetes, balas e sucos (AMIN; ABDEL HAMEID; ELSTTAR, 2010). Para o tratamento desses efluentes em colunas de leito fixo é necessário uma modificação da quitosana a fim de melhorar os aspectos hidrodinâmicos do sistema de adsorção (CRINI; BADOT, 2008). O recobrimento das esferas com quitosana para aplicação como adsorvente de corantes em leito fixo mostrou-se promissor, e este fato deve-se a união das propriedades da quitosana e das esferas. A quitosana com sua alta capacidade de adsorção e versatilidade para o recobrimento, e as esferas por sua vez, podem ser utilizadas para o empacotamento do leito sem afetar a hidrodinâmica do sistema (VIEIRA et al., 2014). Desta forma, as esferas recobertas com quitosana permitem a viabilização do uso da quitosana no processo de adsorção em leito fixo. Neste contexto, o objetivo deste trabalho foi utilizar esferas recobertas com quitosana como preenchimento de coluna de leito fixo para a adsorção do corante amarelo crepúsculo. O comportamento da adsorção do corante amarelo crepúsculo foi avaliado através da obtenção de curvas de ruptura experimentais, e a capacidade máxima de adsorção da coluna foi determinada para as vazões de alimentação utilizadas.
Material e métodos
A coluna foi composta por esferas recobertas por quitosana através da técnica dip coating (VIJAYA et al., 2008; VIEIRA et al., 2014). A massa de quitosana presente nas esferas foi de 2,3 mg quitosana/ g esfera. A quitosana utilizada (massa molar de 146±5 kDa e grau de desacetilação de 85±1%) foi obtida de resíduos de camarão (Penaeus brasiliensis) conforme descrito por Weska et al. (2007). As esferas de vidro (diâmetro de partícula de 1 mm, massa específica de 2300 kg m-3 e esfericidade de 0,99) foram adquiridas da Nacional Esferas Ltda., Brasil. O corante utilizado foi o amarelo crepúsculo (massa molar de 452,4 g mol -1, pureza de 90% e comprimento de onda de máxima absorção de 480 nm), e foi fornecido pela indústria Duas Rodas, Brasil. A adsorção foi realizada em coluna de leito fixo (3,4 cm de diâmetro interno e 20 cm de altura) acoplada a uma bomba peristáltica (Master Flex, 07553–75, Canadá). A solução de corante (100 mg L-1) foi bombeada em fluxo ascendente na vazão de 5 mL min-1, pH 3 e temperatura ambiente (25 ± 2°C). No topo da coluna foram retiradas amostras em tempos pré-estabelecidos até a completa saturação do sistema. A concentração remanescente do corante foi determinada por espectrofotometria (Quimis, modelo Q108 DRM, Brasil).
Resultado e discussão
As curvas de ruptura foram expressas em termos de concentração normalizada (Ct /C0) como uma função de tempo. Os parâmetros foram calculados de acordo com as Equações de 1 a 5 expressas no Quadro 1 (CHEN et al., 2012; AHMAD e HAMEED, 2010; HAN et al., 2009).
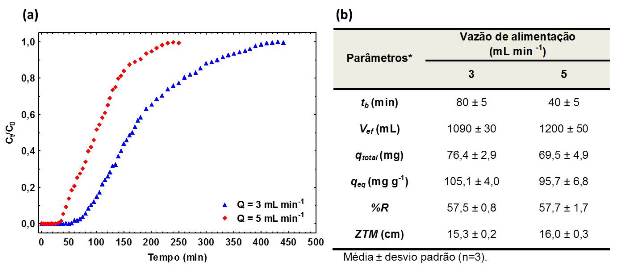
A Figura 1 apresenta as curvas de ruptura para a adsorção do corante amarelo crepúsculo nas vazões de 3 e 5 mL min -1 e os resultados obtidos pelas curvas de ruptura.
Podemos observar na Figura 1((a) e (b)) que a alteração da vazão de alimentação teve uma maior influência sobre o tempo de ruptura, este dobrou na menor vazão de alimentação. Além disso, na vazão de 3 mL min-1 observa-se que o leito levou cerca de 340 min para que ocorresse a exaustão, enquanto que, na vazão de 5 mL min -1 o tempo de exaustão foi atingido mais rapidamente, aos 200 min. Este fato pode ser explicado, pois na menor vazão, o adsorvato tem um maior tempo de residência no leito propiciando a ocorrência do equilíbrio de adsorção entre os solutos contidos na coluna e o adsorvente. Comportamento similar foi encontrado por Elwakeel (2009) na remoção do preto reativo 5 em leito fixo composto por resinas de quitosana.

Conclusões
Esferas recobertas com quitosana foram utilizadas com preenchimento da coluna de leito fixo na adsorção do corante amarelo crepúsculo. Pode-se verificar através das curvas de ruptura que o parâmetro de maior influencia foi o tempo de ruptura, que dobrou com o aumento da vazão de 3 para 5 mL min-1. A capacidade máxima de adsorção da coluna chegou a 105 mg g-1.
Agradecimentos
os autores agradecem a CAPES e ao CNPq.
Referências
AHMAD, A. A.; HAMEED, B. H. Fixed-bed adsorption of reactive azo dye onto granular activated carbon prepared from waste. Journal of Hazardous Materials, v.75, p. 298–303, 2010.
AMIN, K.A.; ABDEL HAMEID II; ELSTTAR, A.H. Effect of food azo dyes tartrazine and carmoisine on biochemical parameters related to renal, hepatic function and oxidative stress biomarkers in young male rats. Food and Chemical Toxicology, v.48, p. 2994–2999, 2010.
CHEN, S.; YUE, Q.; GAO, B.; LI, Q.; XU, X.; FU, K. Adsorption of hexavalent chromium from aqueous solution by modified corn stalk: A fixed-bed column study. Bioresource Technology, v.113, p. 114 –120, 2012.
CRINI, G.; BADOT, P.M. Application of chitosan, a natural aminopolysaccharide, for dye removal from aqueous solutions by adsorption processes using batch studies: A review. Progress in Polymer Science, v. 33, n. 4, p. 399 – 447, 2008.
ELWAKEEL, K.Z. Removal of reactive black 5 from aqueous solutions using magnetic chitosan resins. Journal of Hazardous Materials.v.167, p. 383–392, 2009.
HAN, R.; YU, W.; XIN, Z.; YUANFENG, W.; FULING, X.; JUNMEI, C.; NGSHENG, T. Adsorption of methylene blue by phoenix tree leaf powder in a fixed–bed column: experiments and prediction of breakthrough curves. Desalination, v.245, p. 284 – 287, 2009.
WESKA, R. F.; MOURA, J. M.; BATISTA, L. M.; RIZZI, J.; PINTO L. A. A. Optimization of deacetylation in the production of chitosan from shrimp wastes: Use of response surface methodology. Journal of Food Engineering, v. 80, p. 749–753, 2007.
VIEIRA,M.L.G.; ESQUERDO,V.M.; NOBRE,L.R.; DOTTO, G.L.; PINTO, L.A.A. Glass beads coated with chitosan for the food azo dyes adsorption in a fixed bed column. Journal of Industrial and Engineering Chemistry, v. 20, p. 3387– 3393, 2014.
VIJAYA, Y.;POPURI, S. R.; BODDU, V. M.; KRISHNAIAH, A. Modified chitosan and calcium alginate biopolymer sorbents for removal of nickel (II) through adsorption. Carbohydrate Polymers. v. 72, p. 261 – 271, 2008.










