ISBN 978-85-85905-15-6
Área
Química Orgânica
Autores
Souza, A.M.M. (UFPE) ; Santiago, P.B.G.S. (DEPARTAMENTO DE ANTIBIÓTICOS DA UFPE) ; Albuquerque, J.F.C. (DEPARTAMENTO DE ANTIBIÓTICOS DA UFPE)
Resumo
As tiazolidinas são importantes substâncias heterocíclicas com anéis pentagonais contendo no seu núcleo enxofre e nitrogênio. Os seus compostos derivados apresentam importantes propriedades farmacológicas bem conhecidas, despertando o interesse de vários pesquisadores na síntese de seus análogos. Este fato implica na minimização de riscos à saúde no que diz respeito aos efeitos adversos sobre o sistema biológico humano. O objetivo deste trabalho foi a síntese e a determinação estrutural do composto 5-(2-Bromo-5-metoxibenzilideno)- tiazolidina- 2,4-diona (Ju-625). O composto sintetizado teve todos os seus dados químicos determinados e também sua estrutura por métodos físicos convencionais de espectrometria de infravermelho, ressonância magnética nuclear de hidrogênio, carbono treze e massa.
Palavras chaves
Tiazolidina; Tiazolidina-2,4-diona; Tiazolidinadiona
Introdução
A Química Farmacêutica e Medicinal é uma área de pesquisa que envolve em especial a química orgânica e farmacologia, visando à síntese de novos fármacos, bem como, seu planejamento e avaliação de segurança (Korolkovas, 1986; Thomas, 2003). A necessidade de modificação molecular implica em produzir moléculas mais promissoras como forma de ampliar a terapêutica com baixos efeitos colaterais. Isto leva em conta seu mecanismo de ação, biodisponibilidade, biotransformação e resposta farmacológica. As tiazolidinas são moléculas versáteis que vem sendo estudadas e costumam apresentar importantes propriedades farmacológicas, despertando o interesse da indústria para produção de novos medicamentos. Várias propriedades farmacológicas são atribuídas aos derivados tiazolidínicos como, anticâncer, anestésica, anti-inflamatória, antimicrobianas e outras. (Ottana, 2005, Verma, 2008). Estes estudos são apresentados na literatura como necessários e de grande relevância para determinar várias atividades biológicas. A 4-tiazolidinona é um derivado muito versátil que é responsável por grande número de drogas usadas clinicamente na medicina. O Uso deste derivado é muito importante na cura de diversas doenças principalmente aquelas produzidas por bactérias e por agentes antivirais principalmente contra HIV. A literatura mostra que substituintes arilazo, sulfamoilfenilazo or fenilhidrazona em diferentes posições do anel aumentam a atividade antimicrobiana (Jain, 2012). A mudança da carbonila do posição 4 do anel tiazolidínico por enxofre formando a tiocarbonila, também é um fator para aumentar a atividade microbiológica de seus derivados (Gouveia, 2009). Com estas informações foi sintetizado o composto 5- (2-Bromo-5-metoxibenzilideno)-tiazolidina-2,4-diona e determinado sua estrutura química.
Material e métodos
Em um balão de fundo redondo foram adicionados 0,200g (1,7x10-3 moles) da tiazolidina-2,4-diona (Ju-32) e 3 mL de etanol em agitação magnética até total solubilização da substância. Em seguida foi adicionada três gotas de piperidina, utilizada como catalisador. A reação permaneceu na bancada sob agitação magnética durante dez minutos. Em um Becker foram adicionados 0,3671g (1,7x10-3 moles) do 2-Bromo-5-metóxibenzaldeído e 2 mL de etanol e mantidos sob agitação a quente até completa dissolução. Este material foi vertido para o balão, juntamente com a solução já presente de tiazolidina-2,4-diona. Este foi transferido para o banho de óleo estabilizado a 75 ºC. O balão foi mantido no banho de óleo sob refluxo e agitação magnética. O avanço da reação foi acompanhado por cromatografia em camada delgada, com visualização em luz UV 254 nm, havendo ajuste no sistema de eluição, até o término da reação. A reação permaneceu na capela com exaustão permanentemente ligada durante 5 horas. Após constatar o fim da reação, a mistura contida no balão foi vertida para um béquer, imerso em banho de gelo, ocorrendo resfriamento e posterior cristalização do produto. O produto foi filtrado usando bomba de vácuo e lavado três vezes consecutivas com água destilada seguido de etanol gelado, para retirada de alguma impureza. Após este procedimento os cristais foram recristalizados e novamente filtrados e levados à estufa estabilizada a 37º C para secagem. Os cristais totalmente secos foram submetidos à cromatografia de camada fina para verificar se existia uma só mancha ou se haviam algumas impurezas. Os cristais foram pesados e determinados o rendimento, ponto de fusão e fator de retenção (Rf) sendo enviados para a determinação dos espectros convenientes para a determinação da estrutura química.
Resultado e discussão
O derivado em questão 5-(2-Bromo-5-metoxibenzilideno)-tiazolidina-2,4-diona
(Ju-
625) Fig.1 mostrou os dados a seguir: rendimento 31 %, PF 212–213 °C e Rf
0,53
no sistema (Clorofórmio/Metanol (0,94:0,06). As reações seguiram metodologia
apresentada na literatura. A estrutura foi realizada pelos espectros de
Infravermelho (IV), Ressonância Magnética Nuclear de Hidrogênio e Carbono
treze
(RMN1H; RMN13C) e Massas. Os principais deslocamentos foram: (IV) em (KBr,
cm-1)
3163 referente ao (N-H), (amida). As carbonilas apresentaram picos em 1768
(C=O(4)), e 1702 (C=O(2)), e 1613 referente a dupla ligação exocíclica
(CH=C). O
espectro de RMN1H (300 MHz, DMSO-d6) apresentou sinais característicos de
cada
hidrogênio. Os hidrogênios do substituinte (CH3) em 3,87 ppm, apresentados
como
singleto (s). Além disso, os hidrogênios aromáticos benzílicos foram
apresentados como singlete (s), dublete (d) ou duplo dublete (dd) com
constante
de acoplamento (J). Os resultados estão mostrados a seguir: 7,38 (d 1H(3),
J=6,35 Hz) e 6,83; (dd 1 H(4) J=6,91 e 1,20 Hz); 6,91 (s 1 H(6)). Para o
hidrogênio ligado a posição 6 do anel aromático foi apresentado um singlete
em
6,91 ppm. O hidrogênio da ligação N-H apresentou um singlete em 11,8 ppm. O
Hidrogênio da dupla ligação exocíclica CH=C apresentou um pico referente a
um
singlete em 8,12 ppm. O RMN13C (75.5 MHz, DMSO-d6), mostrou as carbonilas
(C=O2
e C=O4) em 167,49 e 166,85 ppm respectivamente, a CH=C em 142,28 ppm, o
grupo
CH3 em 55,63 ppm. Os carbonos aromáticos foram apresentados em 136,81,
115,89,
136,57, 117,53, 160,71, 137,83 ppm. O carbono quaternário em 158,81 ppm é
próprio do carbono 5 do anel tiazolidínico após a condensação. Massa alta
resolução-ionização por eletron spray- MAR(ESI) mostrou o PM, calculado
315.983;
encontrado 314.1551.
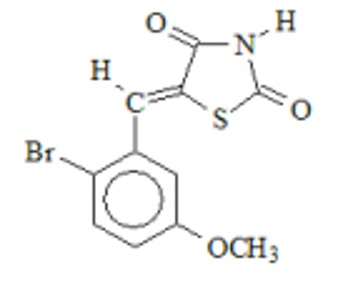
Estrutura química do composto 5-(2-Bromo-5- metoxibenzilideno)-tiazolidina-2,4-diona (Ju-625).
Conclusões
O composto sintetizado 5-(2-Bromo-5-metoxibenzilideno)-tiazolidina-2,4-diona (Ju 625), foi obtido seguindo as indicações da literatura pela reação da tiazolidina-2,4-diona (Ju-32) com 2-Bromo-5-metóxibenzaldeído. O produto foi cristalizado e sua estrutura química foi identificada sendo determinada por espectrometria de Infravermelho, Ressonância Magnética Nuclear de Hidrogênio, de Carbono treze e massa. Os picos de RMN1H; RMN13C mostraram absorções para todos os hidrogênios e carbonos existentes na molécula. O espectrômetro de massa apresentou o peso molecular para o novo composto sintetizado.
Agradecimentos
Pro reitoria de assistência estudantil (CNPq/PROAES) pela aprovação da bolsa de Iniciação científica. Ao CNPq pelo financiamento do projeto de pesquisa aprovado.
Referências
1 Gouveia, F. L.; Oliveira, R. M. B.; Oliveira, T. B.; Silva, I. M.; Nascimento, S. C.; Sena, K. X. F. R.; Albuquerque, J. F. C. Synthesis, antimicrobial and cytotoxic activities of some 5-arylidene-4-thioxo-thiazolidine-2-ones, Eur J Med Chem. 2009, 44, 2038-2043.
2 Jain, A.K; Vaidya , A; Ravichandran, V., Sushil Kumar Kashaw ,A. K.; Agrawal, R.K..Recent developments and biological activities of thiazolidinone
derivatives: A review. Bioorganic & Medicinal Chemistry v.20 p. 3378–3395, 2012.
3 KOROLKOVAS, A.L. E BURCKHALTER, J.H. Química Farmacêutica, Rio de
Janeiro, Ed. Guanabara Dois, 1982, 783 p.
4 Ottana, R.; Maccari, R.; Barreca, M.L.; Bruno, G.; Rotondo, A.; Rossi, A.; Chiricosta, G.; Di Paola, R.; Sautebin, L.; Cuzzocread, S.; Vigorita, M.G. 5-Arylidene-2-imino-4-thiazolidinones: design and synthesis of novel anti-inflammatory agents, Bioorg. Med. Chem. 2005, 13, 4243-4252.
5 THOMAS, G. Química Medicinal: Uma Introdução. ed. Guanabara Koogan, Rio de Janeiro, 2003, p.36-37.
6 Verma, A.; Saraf, S. K. Eur. J. Med. Chem. v. 43, p. 897, 2008.