ISBN 978-85-85905-15-6
Área
Alimentos
Autores
Junqueira Pinto Brito, M. (UESB) ; Martins Veloso, C. (UESB) ; Cristina Ferreira Bonomo, R. (UESB) ; da Costa Ilhéu Fontan, R. (UESB) ; Ferreira Alves, M. (UESB) ; Pereira Flores Santos, M. (UESB)
Resumo
Este trabalho teve como objetivo produzir carvão ativado utilizando como precursor de carbono o caroço do cajá e avaliar sua capacidade em adsorver a α-lactoalbumina do soro do leite. O carvão foi obtido por meio da ativação química, utilizando ácido fosfórico como agente de ativação. A eficiência do processo de adsorção da α-lactoalbumina em carvão ativado, foi determinada através do estudo do pH e da influência da massa de adsorvente utilizada. No estudo verificou-se que em pH = 5,0 ocorreu o melhor desempenho na adsorção e que o aumento a massa do adsorvente promoveu um aumento na capacidade adsortiva da proteína, atingindo uma eficiência máxima de 44,73% com uma massa de 0,075 g do adsorvente.
Palavras chaves
acido fosfórico; ativação quimica; resíduos de biomassa
Introdução
O soro do leite, subproduto resultante da fabricação de queijos, contém uma mistura de proteínas com numerosas e diversas propriedades funcionais, possuindo vários usos em potencial. As principais proteínas no soro de leite são a α-lactoalbumina (α-La) e a β-lactoglobulina (β-Lg), que representam aproximadamente 70% do total proteico contido nele. A α-La é a segunda proteína mais abundante no soro, correspondendo a 20-25% das proteínas do soro e 2% do leite, numa concentração 1,0 a 1,5 g.L-1. É uma proteína globular, pequena, possui massa molecular de 14 kDa e apresenta ponto isoelétrico na faixa de 4,7 a 4,9 (SGARBIERI, p.43, 2005). Diversas técnicas têm sido desenvolvidas visando à recuperação das proteínas do soro de leite (CHEANG; ZYDNEY, p.201, 2003; DE LAMOTTE, p 29, 2005) e entre elas tem-se o método de adsorção, que pode ser definido como um fenômeno físico- químico em que substâncias presentes em uma fase fluida são transferidas para a superfície de uma fase sólida (MASEL, p.112, 1996). Apesar de ser um método eficiente as matrizes adsorventes comerciais utilizadas apresentam alto custo, despertando o interesse para a aplicação de adsorventes alternativos como o carvão ativado, que é um material altamente poroso com elevada área superficial (KEQIANG QIU, p.148, 2011). Os precursores utilizados em sua produção são substâncias com alto valor de carbono e baixo teor de inorgânicos, como por exemplo, resíduos de biomassa oriundos de atividades da agroindústria (CHEN et al, p.5109, 2012). Diante do exposto, o objetivo deste trabalho foi produzir carvão ativado utilizando como precursor de carbono o caroço do cajá, e determinar a influência da variação do pH e da massa na eficiência do processo de adsorção da α-lactoalbumina do soro do leite.
Material e métodos
Na síntese do carvão ativado foi utilizado o caroço do cajá como precursor de carbono. O mesmo foi seco naturalmente, triturado em moinho e peneirado. O resíduo foi impregnado com ácido fosfórico na razão de impregnação 1:1 (massa do agente ativante/massa do caroço do cajá) e seco em estufa a 110°C por 24 h. O material foi carbonizado em forno mufla, sob fluxo de nitrogênio (50 ml.min-1), durante 60 min a 450°C. O carvão obtido foi lavado com água quente até que o pH neutro fosse alcançado e seco em estufa a 105 °C durante 24 h. O rendimento do processo de síntese do carvão (%) foi obtido dividindo-se a massa do carvão obtido (g) pela massa do precursor (g). O pH do ponto de carga zero do adsorvente, foi determinada de acordo com metodologia descrita por Babic et al. (p.477, 2004). Para avaliar o efeito do pH no processo de adsorção da α-lactoalbumina, foram adicionados 0,025 g de carvão em tubos de ensaio contendo 5 mL da solução de proteína (α-lactoalbumina), na concentração de 500 mg.L-1. O ajuste do pH foi realizado com adição de solução tampão fosfato de potássio (20 mM) para pH 7,0 e 5,0, exceto para o pH 3,0 que foi utilizado fosfato de potássio monobásico e ácido fosfórico. Os tubos permaneceram sobre agitação constante à 20 ºC por 24 h, em seguida foram centrifugados sendo o sobrenadante filtrado. A quantificação das proteínas foi realizada por leitura direta em espectrofotômetro no comprimento de onda de 280 nm. Para avaliar a influência da massa de adsorvente na eficiência de adsorção, diferentes massas do carvão (0,025 g; 0,050 g; 0,075 g) foram adicionadas em tubos contendo 5 mL da solução de proteína com concentração inicial de 500 mg.L-1 no pH escolhido, seguindo a mesma metodologia descrita no estudo do pH.
Resultado e discussão
O rendimento do carvão ativado obtido foi de 24,02%, estando de acordo com
valores encontrados na literatura para carvões produzidos de outros
precursores como 13 a 24% para o endocarpo de café (NABAIS et al, p.236,
2008) e 20,1% para semente de uva (OKMAN et al, p.140, 2014). De acordo com
análise do gráfico (Figura 1), foi observado que o ponto de carga zero
(pHPCZ) do carvão ativado esta na região de pH ≅ 5,7. Neste
valor considera-se que o material atua como uma solução tampão, em soluções
com pH abaixo do ponto de carga zero a superfície do carvão ativado é
protonada, favorecendo a adsorção de compostos com carga negativa, e
consequentemente é desprotonada em pH acima, favorecendo o comportamento
oposto (VIEIRA et al, p. 103, 2010). Através do estudo de pH verificou-se
que nos três valores de pH avaliados houve adsorção da proteína, entretanto
no pH = 5,0 foram obtidos os maiores valores de capacidade adsortiva (32,6
mg.g) e eficiência (32,7%), indicando que esse pH é ideal para a
realização dos testes posteriores. Esse valor de pH é o mais próximo do
ponto isoelétrico da proteína e do pHPCZ do carvão, evidenciando
que as interações proteína-adsorvente além de serem influenciadas por forças
eletrostáticas, são também determinadas por interações hidrofóbicas e de Van
der Waals. Em relação ao estudo da massa do adsorvente (Tabela 1) foi
possível verificar que o aumento da massa do carvão promoveu um aumento na
eficiência de adsorção da proteína, tendo sido observado que uma eficiência
máxima (44,73%) foi alcançada, utilizando uma massa de 0,075 g. Este
comportamento se deve ao aumento nos sítios adsortivos proporcionado pelas
massas maiores do adsorvente (HEIBATI et al, p.99, 2015).
Figura 1. Valores de pH inicial e final no experimento de medida do ponto de carga zero do carvão ativado.
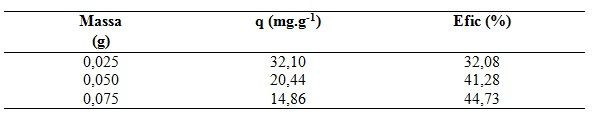
Tabela 1. Capacidade adsortiva (q) e eficiência de adsorção (Efic) da proteína α-lactoalbumina, com variação da massa do adsorvente.
Conclusões
Os testes adsortivos realizados demostraram que o carvão obtido possui uma eficiência considerável na adsorção da α-lactoalbumina, com o emprego de uma massa relativamente pequena e que as interações proteína-adsorvente além de serem influenciadas por forças eletrostáticas, são também determinadas por interações hidrofóbicas e de Van der Waals. Diante disso, é possível concluir que o carvão ativado produzido a partir do caroço de cajá possui potencial para ser empregado na separação da proteína α-La do soro do leite tornando o seu uso como material adsorvente uma alternativa promissora.
Agradecimentos
Referências
BABIC, B.M.; MILONJIC, S.K.; POLOVINA, M.J.; KALUDIEROVIC, B.V. Point of zero charge and intrinsic equilibrium constants of activated carbon cloth. Carbon, v.37, p.477–481, 1999.
CHEANG, B.. ZYDNEY, A.L. Separation of alpha-lactalbumin and beta-lactoglobulin using membrane ultrafiltration, Biotechnol. Bioeng. 83, p.201–209, 2003.
CHEN, C.X.; HUANG, B.; LI, T.; WU, G.F. Preparation of phosphoric acid activated carbon from sugarcane bagasse by mechanochemical processing. Bio Resources, v.7, p.5109–5116, 2012.
DE LAMOTTE, F. Single step pirification of a series of wheat recombinant pro expanded bed absorption chromatography. Journal of Chromatography B, v. 808, p 29-33, 2005.
HEIBATI, B.;COUTO, S.R.; AL-GHOUTI, M.A.; ASIF, M.; TYAGI, I.; AGARWAL, S.; GUPTA, V.K. Kinetics and thermodynamics of enhanced adsorption of the dye AR 18 using activated carbons prepared from walnut and poplar woods. Journal of Molecular Liquids, v.208, p. 99–105, 2015.
KEQIANG QIU, J.Y. Development of high surface area mesoporous activated carbons from herb residues. Chemical Engineering Journal, v.167, p.148–154, 2011.
MASEL, R. I. Principles of Adsorption and reaction on solid surfaces, John Wiley e Sons Inc., p.112, 1996.
NABAIS, J. M. V.; LAGINHAS, C. E,; CARROTT, P. J. M.; CARROTT, M. M. L. R. Production of activated carbons from almond Shell. Fuel Processing Technology, v.92, p. 234-240, 2011.
OKMAN, I.; KARAGÖZ, S.; TAY, T.; ERDEM, M. Activated Carbons From Grape Seeds By Chemical Activation With Potassium Carbonate And Potassium Hydroxide. Applied Surface Science, v.293, p.138– 142, 2014.
SGARBIERI, V.C. Revisão: Propriedades Estruturais e Físico-Químicas das Proteínas do Leite. Brazilian Journal of Food Technology, v.8, n.1, p.43-56, 2005.
VIEIRA, A. P., SANTANA, S. A., BEZERRA, C. W., SILVA, H. A., DE MELO, J. C., DA SILVA FILHO, E. C., & AIROLDI, C. Copper sorption from aqueous solutions and sugar cane spirits by chemically modified babassu coconut (Orbignya speciosa) mesocarp. Chemical Engineering Journal, v.161, p. 99-105, 2010.