ISBN 978-85-85905-15-6
Área
Materiais
Autores
Paiva, M.F. (UNIVERSIDADE DE BRASÍLIA) ; Freitas, E.F. (UNIVERSIDADE DE BRASÍLIA) ; Araújo, A.A.L. (UNIVERSIDADE DE BRASÍLIA) ; Dias, S.C.L. (UNIVERSIDADE DE BRASÍLIA) ; Dias, J.A. (UNIVERISDADE DE BRASÍLIA)
Resumo
A inserção dos heteropoliácidos (HPW e HSiW) na zeólita BEA foi realizada por impregnação aquosa. Os novos materiais foram caracterizados pelas técnicas: DRX, FT-IR, MAS-RMN de 27Al, análise textural por fisissorção de N2 e adsorção gasosa de piridina. Para verificar a estabilidade química foi realizado o teste de lixiviação. Os resultados indicaram a manutenção da estrutura da zeólita observada pela presença das reflexões características nos difratogramas e pela elevada cristalinidade obtida pelo volume total de N2 adsorvido nas amostras. Os materiais com HPW suportado apresentaram maiores valores de área específica e as amostras de 16, 23 e 29% HPW/BEA apresentaram-se promissoras para aplicação em catálise heterogênea devido à maior estabilidade em relação à lixiviação (máximo 7,4%).
Palavras chaves
Heteropoliácidos; Zeólita BEA; Impregnação Aquosa
Introdução
A preocupação com o desenvolvimento de processos sustentáveis vem sendo objeto de interesse de pesquisa em química, buscando-se o aperfeiçoamento e a renovação de processos clássicos baseados nos princípios da química verde. A síntese de catalisadores heterogêneos representa um dos pilares da química verde em virtude da facilidade de remoção desses sólidos do sistema reacional, possibilidade de recuperação, reutilização e por eles serem menos agressivos ao ambiente em relação a catalisadores convencionais. Dessa forma, materiais como zeólitas e heteropoliácidos atraem a atenção de pesquisadores devido a suas propriedades ácidas, possibilitando novas rotas para processos convencionais, promovendo a redução de resíduos tóxicos liberados no ambiente, tornando os processos mais econômicos, rápidos e sustentáveis (YADAV; MORE, 2011). Heteropoliácidos (HPAs) são óxidos iônicos de fácil manuseio e menos corrosivos do que catalisadores homogêneos. Os ácidos 12-tungstofosfórico (HPW) e 12-tungstosilícico (HSiW) são os HPAs com estrutura de Keggin mais conhecidos (KOZHEVNIKOV, 1998). Embora eles apresentem extraordinária acidez de Brønsted, eles possuem baixa área superficial (<10 m2g-1) e alta solubilidade em solventes polares (KOZHEVNIKOV, 1998; KUMAR et al., 2006). A fim de contornar esses inconvenientes à catálise heterogênea, é comum suportá-los em silicatos e aluminossilicatos de elevada área específica (HABER et al., 2003; KUMAR et al., 2006). Dessa forma, é possível preparar catalisadores que apresentem uma adequada força e distribuição de sítios ácidos, e que possam ser utilizados em catálise heterogênea, mesmo na presença de reagentes e solventes polares. A zeólita beta protônica (HBEA) é um dos materiais zeóliticos mais estudadas devido suas propriedades ácidas, elevada área específica de microporos, mesoporos e externa, podendo assim ser utilizada como suporte de metais, óxidos e também de heteropoliácidos. A HBEA possui área específica de aproximadamente 600 m2g-1, elevada capacidade adsortiva e excelente estabilidade térmica, quando comparada a outras zeólitas. Possui propriedades ácidas únicas relacionadas à sua estrutura que a tornam um importante catalisador na conversão de produtos químicos orgânicos, contribuindo para tecnologias de baixo desperdício (JANSEN et al., 1997). O ajuste da acidez e de aspectos morfológicos de sítios ácidos presente em sólidos são fundamentais na catálise. A força e o número de sítios ácidos pode determinar sua capacidade em atuar em reações específicas e a estrutura do suporte pode determinar o acesso dos reagentes aos sítios. O estudo das propriedades do suporte e da impregnação permite o controle das condições ótimas de preparação visando à aplicação mais promissora desses catalisadores suportados, uma vez que as melhores condições são imperativas para sua utilização em processos reacionais de interesse ambiental (RAHIMIZADEH et al., 2010). Diante do exposto, o objetivo do presente trabalho foi o preparo de duas séries de catalisadores heterogêneos baseados na inserção de HPW ou HSiW em diferentes proporções na HBEA. Após o preparo dos materiais, técnicas de caracterização foram utilizadas para determinar a manutenção da estrutura dos HPAs e da HBEA, propriedades texturais, quantificação de sítios ácidos e estabilidade química.
Material e métodos
A zeólita protônica HBEA obtida a partir da calcinação a 550 ºC/8 h da zeólita BEA amoniacal (razão molar SiO2/Al2O3 = 25 - CP814E, Zeolyst), foi adicionada em um balão de fundo redondo e misturada com uma solução de HCl 0,1 mol L-1 contendo a quantidade desejada de H3PW12O40 (HPW) ou H4SiW12O40 (HSiW). O volume da solução aquosa foi de 10 mL por grama de zeólita e a mistura foi mantida sob agitação magnética a 80 ºC até a completa evaporação do solvente. Materiais com os teores de 16, 23, 29 e 50% (m/m) de HPW ou HSiW suportados foram preparados e tratados em forno mufla a 300 ºC/4h (DIAS; OSEGOVIC; DRAGO, 1999; DIAS et al., 2003), sendo nomeados de X%HPA/BEA. Amostras de misturas mecânicas 50% HPW/BEA e 50% HSiW/BEA foram preparadas por maceração e calcinadas a 300 ºC (10 ºC min-1) por 4h para efeito de comparação com as amostras por impregnação aquosa. Para observar a incorporação dos HPAs no suporte, foi feita análise de FT-IR (Varian, 640-IR). Para caracterização de aspectos estruturais foram realizadas análises por: (i) difração de raios X (Bruker, D8 Focus, radiação Cu-Kα de 1,5418 Å); (ii) MAS-RMN de 27Al(Bruker, 600 MHz, Avance) para o estudo dos ambientes de Al presentes na zeólita; (iii) adsorção física de N2 gasoso à -196 ºC (Micromeritics, ASAP 2020C) para obtenção da área específica e diâmetro de poros, sendo que as amostras foram submetidas a um tratamento térmico prévio através da desgaseificação (20 µmHg) à temperatura de 200ºC/12 h. Para o cálculo do número de sítios ácidos nos materiais foram realizados experimentos de adsorção gasosa de piridina e posteriormente análise termogravimétrica (TG), utilizada para detectar a dessorção térmica programada (TPD) de piridina – em um equipamento da TA Instruments, SDT 2960. Para verificar a força da interação entre os HPAs e a zeólita foi realizado teste de lixiviação, de modo a obter informações sobre a estabilidade do catalisador na presença de solventes polares. Quantidade conhecida de catalisador foi adicionada em um balão contendo butanol e alíquotas da solução foram analisadas por espectrofotometria UV-Vis (Beckman, DU 650) para verificar a quantidade de HPA solubilizado.
Resultado e discussão
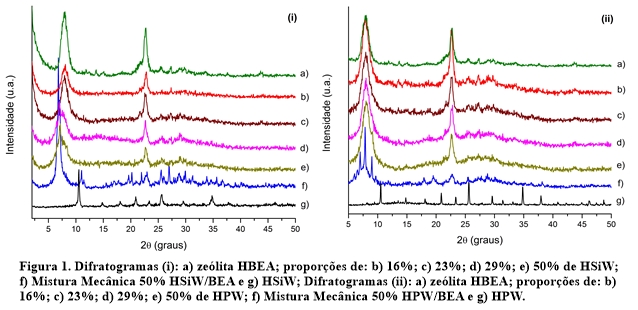
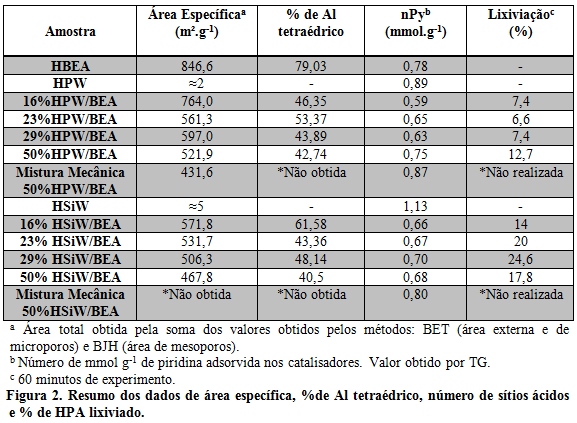
Resultados de FT-IR indicaram para as amostras impregnadas, bandas em torno de 1627 e 1250-950 cm-1 referentes a estiramento assimétrico de tetraedros (vibrações internas) da zeólita, além de duas bandas em 575 e 525 cm-1, que são características para BEA devido a presença de anéis de tetraedros de cinco membros, indicando que a estrutura zeolítica foi mantida após a impregnação o que proporcionou elevada cristalinidade para todas as amostras preparadas (ARMENGOL et al., 1997). Pode-se observar ainda que as bandas dos HPW se sobrepuseram as da BEA, com exceção da banda de baixa intensidade em torno de 880 cm-1 que apresentou um pequeno crescimento com o aumento da proporção do HPA. As mesmas observações podem ser verificadas para a impregnação do HSiW. Os difratogramas de raios X dos catalisadores sintetizados confirmaram que a estrutura cristalina do suporte foi mantida após a impregnação dos HPAs. As amostras permaneceram com picos de difração característicos da zéolita Hβ em 2θ = 7,8º e 22,5° (XU et al., 2013) e cristalinidade elevada (valores entre 92 e 100%). Nenhuma característica de reflexões típicas relacionados com o HPW foi detectada nas amostras HPW/BEA mesmo quando a quantidade suportada foi de 50% (Figura 1-(ii)). Isso demonstra que o HPW foi bem disperso sobre a superfície (BAI et al., 2014). No entanto, para o sistema do HSiW (Figura 1-(i)) é possível observar um desdobramento do pico em torno de 2θ = 6,5º, nas proporções de 29 e 50% de HSiW impregnado. Este desdobramento indica um maior espaçamento entre planos cristalinos resultante da hidratação do próton do heteropoliácido, que modifica sua estrutura secundária, alterando assim os parâmetros de rede do cristal (CALIMAN et al., 2005; ESSAYEM et al., 1995; HOULD et al., 2012).Uma comparação dos difratogramas das amostras impregnadas com as amostras preparadas por uma simples mistura mecânica ((Figura 1-(i-f) e (ii-f)) indica a preservação dos picos do HPA na mistura mecânica e um deslocamento ou alteração da intensidade de seus picos. Os espectros de MAS-RMN de 27Al indicaram um sinal em torno 55 ppm referente à sítios de Al tetraédricos da rede zeolítica e um sinal em torno de 0 ppm devido a Al octaédrico [Al(H2O)6]3+ que pode ser endereçado como espécies de Al fora da rede (KUNKELER et al., 1998). A Figura 2 indica a proporção de Al tetraédrico em relação à quantidade total de Al presente em cada amostra. Observa-se uma redução da quantidade de Al tetraédrico (de 79 para cerca de 40-50% para a impregnação com HPW e para cerca de 40-60% para HSiW) após a impregnação das amostras com o HPA, provavelmente devido à desaluminização da BEA durante a impregnação e posterior evaporação do solvente. O percentual de Al tetraédrico (sítios de Brønsted) que saiu da rede da BEA pode ter gerado sítios de Lewis (HOULD et al., 2012; KIRICSI et al., 1994). A IUPAC classifica as isotermas de adsorção e dessorção de N2 em 6 diferentes tipos e tanto para a zeólita pura como aquela contendo HPA suportado, apresentaram formato do tipo II, assim como obtido por (TOSHEVA et al., 2001). Os valores de área específica total (Figura 2) correspondem a soma da área de microporos e área externa obtidas por BET e área de mesoporos obtidos pelo método BJH. Com o aumento gradual da quantidade de HPA suportado observa-se uma diminuição linear da área total. Isso é condizente com a diminuição gradativa da quantidade da zeólita (espécie que contribui com a área específica) com o aumento da quantidade de HPA suportado. Pelo volume de N2 total adsorvido pela amostra é possível calcular a cristalinidade da amostra (GIANNETTO P., 1990). Os valores de cristalinidade apresentaram-se superiores a 90%, indicando que a estrutura da zeólita BEA é resistente ao tratamento de impregnação e que houve pouca modificação na estrutura inicial do suporte. A elevada área específica dos materiais suportados confirma o preparo de materiais promissores para aplicação em reações de catálise ácida. Uma propriedade importante para a catálise representa a quantificação dos sítios ácidos presentes, pois eles irão atuar efetivamente nas reações. Nas zeólitas podem existir sítios ácidos de Lewis e Brønsted, sendo o último mais importante na catálise ácida. Ao adsorver piridina nos catalisadores observou-se um menor número total de sítios ácidos das amostras impregnadas frente à BEA pura (Figura 2), evidenciando que os HPAs podem estar bloqueando os sítios ácidos da zeólita provocado pela obstrução de seus poros. Esta hipótese é validada pela verificação via FT-IR de que ocorreu uma diminuição nas bandas associadas à acidez do material com o aumento da quantidade suportada do ácido (NANDHINI et al., 2006). Para a maioria dos materiais preparados, aqueles contendo HSiW mostraram maior número de sítios ácidos que aqueles contendo HPW. Isso provavelmente ocorre devido a que cada HSiW possui 4 prótons, enquanto cada HPW possui apenas 3 prótons, isto é, há um maior número de sítios ácidos no HSiW. O teste de lixiviação foi realizado para verificar o grau de interação existente entre os HPAs e o suporte na presença de um solvente polar. Na figura 2 são mostrados esses resultados. Os valores de lixiviação obtidos foram geralmente baixos, sendo o valor mais alto de 24,6%. Isso mostra a boa interação entre os HPAs e a zeólita BEA. Em geral, há um aumento da força de interação de HPAs em suportes contendo alumínio (CALIMAN et al., 2005). Como esperado, com o aumento do teor de HPA suportado é notado o aumento do grau de lixiviação.
Conclusões
Os catalisadores de HPAs suportados em zeólita HBEA foram sintetizados e caracterizados com sucesso. Os resultados indicaram a manutenção da estrutura da zeólita observada pelas bandas nos espectros de FT-IR, pela presença das reflexões características nos difratogramas e pela elevada cristalinidade obtida pelo volume total de N2 adsorvido nas amostras. Os materiais com HPW suportado apresentaram maiores valores de área específica e as amostras de 16, 23 e 29% HPW/BEA se apresentaram mais promissoras devido a maior estabilidade, com valores de lixiviação de no máximo 7,4%. Os catalisadores formados são sólidos ácidos promissores para aplicação em reações como alquilação, esterificação e desidratação.
Agradecimentos
DPP/IQ/UnB, CAPES, MCT/CNPq, FAPDF, FINEP-CTInfra, FINEP-CTPetro, FINATEC e Petrobras.
Referências
ARMENGOL, E. et al. Acid zeolites as catalysts in organic reactions. Acetylation of cyclohexene and 1 -methylcyclohexene. 1997. BAI, G. et al. Friedel–Crafts acylation of anisole with hexanoic acid catalyzed by Hβ zeolite-supported tungstophosphoric acid. Research on Chemical Intermediates, v. 41, n. 8, p. 5041–5048, 25 mar. 2014. CALIMAN, E. et al. Solvent effect on the preparation of H3PW12O40 supported on alumina. Catalysis Today, v. 107-108, p. 816–825, out. 2005. DIAS, J. A et al. Preparation and characterization of supported H3PW12O40 on silica gel: a potential catalyst for green chemistry processes. Catalysis Today, v. 85, n. 1, p. 39–48, set. 2003. DIAS, J. A.; OSEGOVIC, J. P.; DRAGO, R. S. The Solid Acidity of 12-Tungstophosphoric Acid. Journal of Catalysis, v. 183, n. 1, p. 83–90, abr. 1999. ESSAYEM, N. et al. Acidic and catalytic properties of CsxH3−xPW12O40 heteropolyacid compounds. Catalysis Letters, v. 34, n. 1-2, p. 223–235, mar. 1995. GIANNETTO P., G. Zeolitas: Caracteristicas, propiedades y aplicaciones industriales. 1a. ed. Caracas: EdIT - Editorial Innovación, 1990. p. 170. HABER, J. et al. Catalytic performance of the dodecatungstophosphoric acid on different supports. Applied Catalysis A: General, v. 256, n. 1-2, p. 141–152, dez. 2003. HOULD, N. D. et al. Effect of Al on Zeolite Beta Solid State Chemistry. Topics in Catalysis, v. 55, n. 19-20, p. 1332–1343, 6 out. 2012. JANSEN, J. C. et al. On the remarkable behaviour of zeolite Beta in acid catalysis. Catalysis Today, v. 38, n. 2, p. 205–212, out. 1997. KIRICSI, I. et al. Progress toward Understanding Zeolite Beta Acidity: An IR and 27Al NMR Spectroscopic Study. The Journal of Physical Chemistry, v. 98, n. 17, p. 4627–4634, abr. 1994. KOZHEVNIKOV, I. V. Catalysis by Heteropoly Acids and Multicomponent Polyoxometalates in Liquid-Phase Reactions. Chemical Reviews, v. 98, n. 1, p. 171–198, fev. 1998. KUMAR, G. S. et al. SBA-15 supported HPW: Effective catalytic performance in the alkylation of phenol. Journal of Molecular Catalysis A: Chemical, v. 260, n. 1-2, p. 49–55, dez. 2006. KUNKELER, P. J. et al. Zeolite Beta: The Relationship between Calcination Procedure, Aluminum Configuration, and Lewis Acidity. Journal of Catalysis, v. 180, n. 2, p. 234–244, dez. 1998. NANDHINI, K. U. et al. Al-MCM-41 supported phosphotungstic acid: Application to symmetrical and unsymmetrical ring opening of succinic anhydride. Journal of Molecular Catalysis A: Chemical, v. 243, n. 2, p. 183–193, jan. 2006. RAHIMIZADEH, M. et al. TiO2 nanoparticles and Preyssler-type heteropoly acid modified nano-sized TiO2: A facile and efficient catalyst for the selective oxidation of sulfides to sulfones and sulfoxides. Journal of Molecular Catalysis A: Chemical, v. 323, n. 1-2, p. 59–64, 17 maio 2010. TOSHEVA, L. et al. Zeolite beta spheres. Microporous and Mesoporous Materials, v. 48, n. 1-3, p. 31–37, nov. 2001. XU, J. et al. The acid treatments of the Hß zeolite as the catalyst in the synthesis of ethyl tertiary butyl ether antiknock additive. v. 2, n. 12, p. 9–17, 2013. YADAV, G. D.; MORE, S. R. Green alkylation of anisole with cyclohexene over 20% cesium modified heteropoly acid on K-10 acidic montmorillonite clay. Applied Clay Science, v. 53, n. 2, p. 254–262, ago. 2011.