ISBN 978-85-85905-15-6
Área
Iniciação Científica
Autores
Souza, L. (UNIANCHIETA) ; Teixeira de Toledo, A.C. (USP) ; Ros de Almeida, J.F. (USP)
Resumo
O presente trabalho tem por objetivo testar o uso de Nanopartículas de Prata em substituição aos produtos clorados comumente utilizados em Estações de Tratamento de Águas e Efluentes, com a finalidade de desinfecção e menor probabilidade de geração de THM's (Trihalometanos), subprodutos comprovadamente tóxicos e carcinogênicos. A fim de avaliar a eficácia da solução nanoparticulada de prata foram realizados testes bacteriológicos e físico-químicos. Os resultados foram satisfatórios quando comparados a ação do Hipoclorito de Sódio. O uso da solução nanoparticulada em ETA's e ETE's torna-se viável técnica e economicamente pela facilidade do uso, não formação de THM's e menor potencial corrosivo em tubulações quando comparado ao cloro inorgânico.
Palavras chaves
Nanopartículas de Prata; Trihalometanos; Tratamento de Água
Introdução
A Nanotecnologia, assunto do presente trabalho, se insere em uma linha de pesquisa ainda pouco explorada no Brasil, portanto o estudo desse tema com foco em tratamento de água, pode ser interessante ao meio científico, social e econômico [17,21]. No início do século XX a prata foi aprovada como agente antimicrobiano e a partir de 1940 a sua utilização caiu com a alta do uso dos antibióticos [10,15]. Os íons de prata (Ag+) também podem interagir com o DNA, impedindo a reprodução celular [12]. As Nanopartículas de Prata (NPP) em dimensões de inferiores a 200 nanômetros no estado coloidal ou sólido resultam em um maior efeito antimicrobiano quando comparadas aos sais de prata [2]. Partículas de prata em dimensões nanométricas encontram-se tão finamente dispersas que podem circular pelas membranas celulares sem ocasionar danos aos organismos superiores, visto que a concentração efetiva para a atuação contra microrganismos é de 0,1 microgramas por litro (0,1μg/L) e a concentração tóxica para os seres humanos é de 10 microgramas por litro (10μg/L) [20]. A partir de 1974, quando nos EUA estudos mostraram pela primeira vez a correlação positiva entre águas de abastecimento público e câncer, várias pesquisas foram desenvolvidas, entre as quais se destaca a realizada pela U.S. Environmental Protection Agency (EPA) em 113 estações de tratamento de água [13,16]. THM’s foram encontrados em todas as ETA’s que utilizavam derivados clorados nos processos de desinfecção [4,5,3,18,19,14]. Vislumbrando um cenário em que as NPP possam contribuir para a melhoria na eficiência nos sistemas de tratamentos de água, fundamentalmente no que se refere ao combate aos agentes patogênicos, presumidamente é possível imaginar águas com maior qualidade do ponto de vista de saúde pública [16].
Material e métodos
Foram preparadas soluções de prata nanoparticulada em concentrações de 60 ppm utilizando método eletrolítico cujo detalhamento é reservado à empresa Khemia Equipamentos Tecnológicos de Efluentes. Para início dos testes, realizou-se a coleta de águas antes e após o processo de cloração da ETA e da ETE na empresa SABESP nos municípios de Campo Limpo Paulista-SP e Várzea Paulista-SP, com objetivo de comparar águas em diferentes condições sem adição de agente desinfectante clorado. Para as análises foram utilizados os seguintes equipamentos: peagâmetro (ORION 720A); termômetro (MINIPA MT-320); turbidímetro (HANNA HI-98703); Analisador de cloro (POLICONTROL AP-2000); condutivímetro (POLICONTROL 3200); Jar Test (FLOCCONTROL); contador de colônias (Phoemix) e Espectrometro de Emissão Óptica (ICP-OES VARIAN 720-ES). Para os testes microbiológicos foram realizadas diluições da solução de prata na proporção (1:10.000) em água ultra pura, e as dosagens feitas foram de 3,5 mL para 2000 mL das amostras em Jar Test com velocidade de 40 rpm. A análise microbiológica foi feita pelo método Pour Plate, conforme a Norma Técnica da CETESB [7,8,9], que baseia-se no desenvolvimento de bactérias heterotróficas em meio de cultura (Plate Count Agar), com valores conhecidos do produto sob condições de tempo e temperatura controlados. Após o período de incubação fez- se a contagem das unidades formadoras de colônia por mililitro (UFC/mL) [1,22]. As análises de pH, turbidez, condutividade, concentração de cloro residual e prata residual foram realizadas nas amostras imediatamente após os ensaios de bancada com o produto em teste. O ensaio de determinação de prata presente na amostra, posterior ao tratamento, foi realizado em equipamento ICP-OES pertencente à empresa SABESP.
Resultado e discussão
Os resultados das análises físico-químicas antes e após adição do produto nas
amostras de água da ETA e ETE são apresentados na tabela 1. Vale destacar que
houve diminuição dos valores de turbidez após a adição do produto, em que
observamos uma significativa melhoria no aspecto das águas, pois quando há
excesso de cloro observa-se uma leve turvação na água, que tende a diminuir
com aumento da temperatura e consequente dispersão do cloro. Os testes
microbiológicos realizados em Placas de Petri são ilustrados na figura 1. Para
a amostra proveniente da ETA observou-se uma total eliminação de atividade
bacteriana, com redução de 1.200 UFC/mL para 0 UFC/mL após adição de solução
de prata (60 ppm). O mesmo ocorreu com a amostra da ETE após exposição à
solução de prata, e neste caso a redução foi de 1.180 UFC/mL para 0 UFC/mL. Os
resultados presuntivamente da ação antimicrobiana avaliadas na forma
vegetativa em tratamentos de águas demonstraram-se satisfatórios, visto que
houve eliminação total das bactérias heterotróficas. Sendo assim, torna-se
plausível a veracidade de teorias decorrentes à mortandade celular, acredita-
se que as NPP são capazes de interagir com elementos da membrana celular das
bactérias causando danos estruturais, forçando a dissipação de prótons, e
finalmente a morte celular [6]. O resultado de prata residual realizada em
ICP-OES apontou um valor de 0,015 ppm (Ag total) na amostra de ETA tratada
com solução de prata. A legislação estabelece um limite de 0,010 mg/L de (Ag
total), portanto entendemos nesses testes preliminares que seria necessária
uma diminuição na dosagem de prata a fim de enquadrar esse parâmetro à lei
[11]. Acreditamos ser possível diminuir as concentrações de prata e ainda
obter um melhor resultado quando comparado ao Hipoclorito.
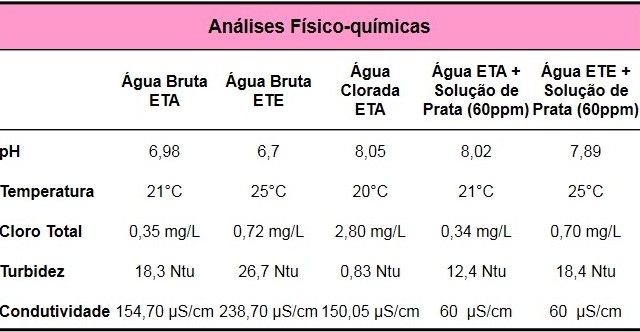
Resultados de Análises Físico-químicas realizadas em águas da ETA e ETE.
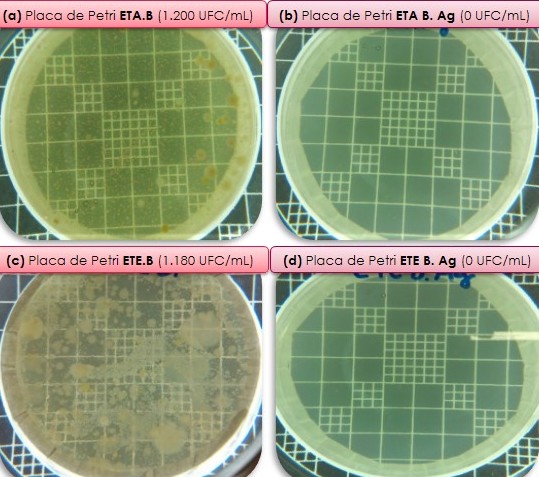
(a) Placa de Petri com Água ETA (b) Placa de Petri com Água ETA + Prata (c) Placa de Petri com Água ETE (d) Placa de Petri com Água ETE + Prata.
Conclusões
Os testes apontaram uma redução completa para atividades bacterianas nas mostras águas de ETA e ETE, portanto conclui-se que o produto em estudo é eficiente para fins de desinfecção ao substituir o Hipoclorito, com as seguintes vantagens: i) diminui a geração de THM’s; ii) menor custo comparado aos produtos clorados; iii) não corrosivo às tubulações; iv) reduz a turbidez da água ao substituir produtos clorados; vi) pode-se testar menores dosagens de prata (piloto e grande escala) a fim de garantir um enquadramento mais seguro do ponto de vista toxicológico, e com eficiência aceitável.
Agradecimentos
Agradecemos às Empresas Khemia e SABESP e ao Centro Universitário Padre Anchieta pela bolsa concedida.
Referências
[1] ALLEN, M. J.; EDBERG, S. C.; REASONER, D.J. Heterotrophic plate count bacteria – what is their significance in drinking water? Int. J. Food Microbiol. v.92, p.265-274, 2004.
[2] ATIYEH, B. S.; COSTAGLIOLA, M.; HAYEK, S. N.; DIBO, S. A. Effect of silver on burn wound infection control and healing: review of the literature. Burns, v. 33, p. 139-148, 2007.
[3] BALSTER, R. L., BORZELLECA. J. F. Behavioral toxicity of trihalomethane contaminants of drinking water in mice.Environmental Health Perspectives, v.46, p.127-136, 1982.
[4] BELLAR, T.A., LICHTENBERG, J. J., KRONER, R. C.Theocurrence of organohalides in chlorinated drinking waters.Journal American Water Works Association, v.66, n.12; p.703-706, Dec. 1974.
[5] BUN, W. W., HAAS, B. B., DEANE, E. R. et al. Formation of trihalomethanes by chlorination of surface water, Environmental Letters, v.10, n.3, p.205-213, 1975.
[6] CARREIRA, C. M.; PEREIRA, C. A.; BOMBANA, A. C.; JORGE, A. O. C. Eficácia antimicrobiana das nanopartículas de prata sobre esporos, leveduras e bactérias. XIII Encontro Latino Americano de Iniciação Científica e IX Encontro Latino Americano de Pós-Graduação – Universidade do Vale do Paraíba, 2009.
[7] CETESB (São Paulo). Guia de coleta e preservação de amostras de água. São Paulo, 1988. 150 p.
[8] _______. 21L5.216: controle de qualidade de meios de cultura: método de ensaio. São Paulo, 1987. 36 p. Norma técnica.
[9] _______. 22M1.001: lavagem, preparo e esterilização de materiais em laboratórios de microbiologia: procedimento. São Paulo, 1986. 34 p. Norma técnica.
[10] CHOPRA, I.The increasing use of silver-based products as antimicrobial agents: a useful development or a cause for concern? Journal Antimicrobial Chemostherapy. v.59, n.4, p. 587-590, 2007.
[11] CONAMA - Conselho Nacional do Meio Ambiente. Resolução n° 357/05. Estabelece a classificação das águas doces, salobras e salinas do Território Nacional. Brasília, SEMA, 2005.
[12] DAMM, C.; MUNSTEDT, H.; ROCH, A. Long-term antimicrobial polyamide 6/silver-nanocomposites.Journal of Materials Science, v. 42, p. 6067-6073, 2007.
[13] DROSTE, R. L. Theory and practice of water and wastewater treatment. New York, Wiley, 1997.
[14] GRAY, N. F. Calidad del agua potable. Zaragoza, Acribia. p. 365, 1994.
[15] KLASEN, H.J. Historical review of the use of silver in the treatment of burns. I. Early uses. Burns.V.26, p. 117-130, 2000.
[16] MACÊDO, J. A. B.; BARRA, M.M. Derivados Clorados de origem orgânica uma solução para o processo de desinfecção de água potável e para desinfecção de industrias. VI Simpósio Ítalo Brasileiro de Engenharia Sanitária e Ambiental. Vitória, 2002.
[17] MCTI. MINISTÉRIO DA CIÊNCIA, TECNOLOGIA E INOVAÇÃO. MCTI, Brasil e Canadá abrem primeira edição de workshop de nanotecnologia. Disponível em: <http://www.mct.gov.br/index.php/content/view/344484/Brasil_e_Canada_abrem_primeira_edicao_de_workshop_de_nanotecnologia.html>. Acesso em: 12 de Julho 2015.
[18] MELNICK, R. L. Toxicology and Carcinogenesis studies or Bromodicholoromethane.Washington, D.C.: US. Departament of Health and Human services, p. 182, 1987.
[19] MELNICK, R. L. Toxicology and carcinogenesis studies or tribromethane (bromofórmio). Washington, D.C.: U.S. Departament of Health and Human Services, p. 194, 1989.
[20] OLIVEIRA, E.M.N. Trabalho de Conclusão de curso. Departamento de Química. UFSC, 2006.
[21] RIBOLDI, B. M. Nanotecnologia: fundamentos e aplicções. Instituto de Geociências e Ciências Exatas. Campus de Rio Claro (UNESP), 2009. Disponível em: <http://unesp.br/proex/congressos/5congresso/fscommand/web/docs/215.pdf> Acesso em: 08 de Julho 2015.
[22] SILVA, N.; NETO, R. C.; JUNQUEIRA, V. C. A.; SILVEIRA, N. F. de A. Manual de métodos de análise microbiológica de água. São Paulo: Livraria Varela, 2005.