ISBN 978-85-85905-15-6
Área
Química Inorgânica
Autores
Salles, P.H.L. (IF SUDESTE MG) ; Vieira, B.L.M. (IF SUDESTE MG) ; Nascimento, J.C. (IF SUDESTE MG) ; Dias, F.A.C. (IF SUDESTE MG) ; Toledo, T.A. (IF SUDESTE MG) ; Barbosa, D.B.A. (IF SUDESTE MG)
Resumo
Foi realizado o estudo espectrofotométrico de soluções comerciais de dipirona sódica monoidratada para investigar a absorção na região UV dos grupos cromóforos presentes na molécula. As análises espectrofotométricas juntamente com os cálculos teóricos para a molécula de dipirona forneceram o perfil da transição eletrônica presente. Foi possível identificar os picos de absorvância e seus respectivos comprimentos de onda, tanto no medicamento de referência, quanto nos medicamentos similar e genérico, mostrando que ambos apresentam a mesma composição esperada do princípio ativo no fármaco. Com este estudo pode-se estabelecer uma boa conformidade entre os dados experimentais e teóricos propostos servindo de base para estudos futuros de propriedades eletrônicas com outros fármacos.
Palavras chaves
dipirona sódica; espectroscopia UV; estudo teórico e experime
Introdução
A dipirona sódica monoidratada, de fórmula molecular C13H16N3NaO4S.H2O, pertence à classe dos antiinflamatórios não esteroidais e possui efeito analgésico e antitérmico, sendo muito utilizada no tratamento de dores e febre. Por não requerer a prescrição médica para sua comercialização, possui taxa abusiva de consumo e uma de suas principais reações adversas é a agranulocitose. Devido a essa reação indesejada, muitos países proibiram sua comercialização, todavia, no Brasil possui venda livre, pois a porcentagem de pessoas atingidas é considerada mínima1,2. A técnica analítica de espectrofotometria, que permite a determinação de compostos pela absorção relativa da luz, pode ser empregada com sucesso para identificação de dipirona sódica em soluções através do espectro na região do ultravioleta2. Foi realizado o estudo espectrofotométrico de soluções comerciais de dipirona sódica monoidratada com o intuito de investigar a absorção na região ultravioleta dos grupos cromóforos presentes na molécula de dipirona.
Material e métodos
Foram adquiridos no comércio local, 3 amostras distintas de dipirona sódica monoidratada em gotas (soluções de 500 mg/mL), sendo um medicamento de referência (Novalgina®), um similar (Anador®) e um genérico (Germed). O ácido clorídrico P.A. adquiridos da Vetec®. Inicialmente foram preparadas soluções de concentração 6,0.10-4 mol/L em ácido clorídrico 0,5 mol/L, e posteriormente foram realizadas diluições das amostras em água destilada para atingir a concentração de 6,0.10-5 mol/L. As análises foram realizadas no espectrofotômetro Lambda 25, Perkin Elmer, na região de absorção ultravioleta, com caminho óptico de 1cm. Realizaram-se cálculos ab initio no método CIS com base 3-21G utilizando o programa GAMESS para o cálculo do espectro eletrônico UV-vis. A partir dos dados obtidos dos comprimentos de onda (λ) absorvidos e a contribuição dos orbitais moleculares que participam da excitação eletrônica pode-se fazer a comparação dos resultados teóricos com os resultados experimentais com o auxílio do programa Chemissian.
Resultado e discussão
A dipirona (ácido [(2,3-diidro-1,5-dimetil-3-oxo-2-fenil-1H-pirazol-4-
il)metilamino] metanosulfônico) é um ácido fraco com um pKa de 3,77 que
apresenta um aumento da intensidade da absorção a medida que o pH diminui.3
Não obstante, a dipirona sódica é classificada com um caráter neutro4 e
apresenta absorbância máxima nos comprimentos de onda no ultravioleta entre
207,8 e 266,7 nm.5
As varreduras espectrofotométricas para verificação das melhores absorções
na faixa de comprimento de onda entre 200 e 300 nm, para as amostras de
dipirona sódica, Novalgina® e Anador®, demonstraram a presença de uma banda
em 239 nm com absorvância de 0,57 ( = 8906(mol-1. L. cm-1)) e outra banda
em 258 nm com absorvância de 0,64 ( = 10.000(mol-1. L. cm-1) utilizando
como solvente o HCl. Também é possível observar um alargamento da banda no
espectro quando o solvente é a água e um deslocamento batocrômico (para o
vermelho) de 7 nm (265 nm) associado as transições →* devido a polarização
do solvente.
Para fazer a atribuição das transições eletrônicas presentes no espectro de
absorção da dipirona, foram comparados os resultados experimentais obtidos
com os resultados dos cálculos ab initio realizados com o programa GAMESS
para a forma protonada e desprotonada presentes em meio ácido (Tabela 1).
A comparação dos dados calculados com os dados experimentais mostra a
presença das bandas B características de transições dos sistemas aromáticos
e heteroaromáticos presentes na molécula. Muitos estudos de referência para
fármacos6 identificam apenas a banda presente em 258 nm como característica
da dipirona em meio ácido, mas os cálculos demonstram a presença de uma
outra espécie presente no meio, a espécie desprotonada, que absorve em 240
nm.

Comprimentos de onda experimentais e teóricos.
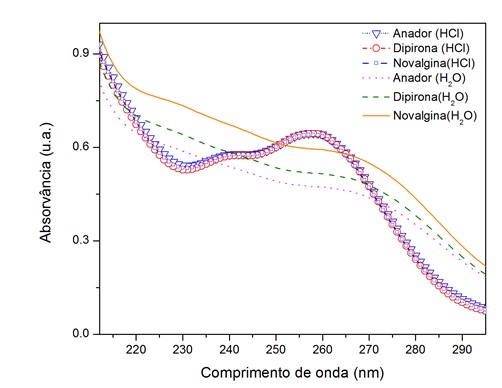
Espectro UV de absorção das amostras de dipirona sódica, Novalgina® e Anador® em H2O e HCl.
Conclusões
As análises espectrofotométricas juntamente com os cálculos teóricos para a molécula de dipirona forneceram o perfil da transição eletrônica presente. Foi possível identificar os picos de absorvância e seus respectivos comprimentos de onda, tanto no medicamento de referência, quanto nos medicamentos similar e genérico mostrando que ambos apresentam a mesma composição esperada do princípio ativo. Com este estudo pode-se estabelecer uma boa conformidade entre os dados experimentais e teóricos propostos servindo de base para estudos futuros de propriedades eletrônicas com outros fármacos.
Agradecimentos
Ao Instituto Federal do Sudeste de Minas Gerais - Campus Juiz de Fora e à Fundação de Amparo a Pesquisa do Estado de Minas Gerais.
Referências
1. IZOLANI, A.O,; MORAES, M.T.; TÉLLEZ, C.A. Fourier transform Raman spectroscopy of drugs: quantitative analysis of 1-phenyl-2,3-dimethyl-5-pyrazolone-4-methylaminomethane sodium sulfonate: (dipyrone). Journal of Raman Spectroscopy, vol. 34, issue 10, pages 837–843, October 2003.
2. NASCIMENTO, A. P. Desenvolvimento e validação de metodologia para medicamentos contendo dipirona sódica e cloridrato de papaverina isolados e em associação. 2006. Tese (Doutorado em Produção e Controle Farmacêuticos) - Faculdade de Ciências Farmacêuticas, Universidade de São Paulo, São Paulo, 2006.
3. PITARELLO, A. P.; LINDINO, C. A.; SILVA, C.; FERRI, E. A. V.; SOUZA, M. L.; BARICCATTI, R. A. Estudo fotoquímico da dipirona na presença de β e γ ciclodextrina. Acta Scientiarum. Health Science, v. 27, n. 2, p. 171-175, 2005.
4. MORAES, E. C.; SZNELWAR, R. B.; FERNICOLA, N. A. G. G. – Manual de Toxicologia analítica, 1ª ed. São Paulo: Roca Ltda, 1991, 229 p.
5. AMÉRICO, M. A., GALERANI, S.A., NISHIYAMA, P.. RBAC, vol. 40(4): 257-259, 2008.
6. CLARKE, E.C.G. Clarke’s isolation and identification of drugs in pharmaceutical body fluids and post-mortem material. 2 ed. London: Pharmaceutical Press, 1986. p.563.