ISBN 978-85-85905-15-6
Área
Físico-Química
Autores
Vicente, M.M.F. (UEMS) ; José Arruda, G. (UEMS)
Resumo
A vitamina E têm sido frequentemente associado à prevenção doenças neurodegenerativas, ateroscleroses, inflamações crônicas, cancerígenas e envelhecimento precoce. Neste trabalho foram realizados estudos eletroquímicos da vitamina E, com o objetivo de comparar a resposta eletroquímica utilizando eletrodos de pasta de carbono e eletrodo de pasta de nanotubos de carbono. Os resultados obtidos mostraram que eletrodo de pasta de nanotubos de carbono apresentou corrente de pico de 267% maior que a corrente de pico obtida com o eletrodo de pasta de carbono.
Palavras chaves
Vitamina E; Voltametria; Nanotubos de carbono
Introdução
Os tocoferóis e tocotrienóis possuem ação sinérgica em mecanismo protetor à oxidação de alimentos e organismos biológicos, isso é divido as suas propriedades químicas é a sua ação antioxidante. A ação antioxidante ocorre pela proteção de ácidos graxos poli-insaturados, evitando, assim, a formação de peróxidos que desencadeiam ação lesiva em tecidos, conhecidos como estresse oxidativo (Fonseca, L. G. et al; 2015). A vitamina E, ou α-tocoferol, é apontado como sendo o mais potente em sua ação antioxidante natural (Yoshida et al., 2003). As moléculas de vitamina E tem um grupo hidroxila que pode reagir com o oxigênio, por isso todos estes tocoferóis são eletroquimicamente oxidados (M. F. Marcus, M. D. Hawley, 1970). Este trabalho tem como objetivo caracterizar eletroquimicamente a vitamina E utilizando os eletrodos de pasta de carbono (EPC) e eletrodo de pasta de nanotubos de carbono de paredes múltiplas (EPNC).
Material e métodos
As medidas eletroquímicas foram realizadas em um Potenciostato/Galvanostato AUTOLAB PGSTAT 12 interfaciado a um computador e gerenciado pelo software NOVA 1.10 para aquisição e tratamento dos dados. Foi utilizada uma célula de vidro de compartimento único com três eletrodos: eletrodo de prata/cloreto de prata (Ag/AgCl) como referência; eletrodo de fio de platina como eletrodo auxiliar e como eletrodos de trabalho foram utilizados EPC (75% de grafite e 25% de Nujol) e EPNC (75% de nanotubo e 25% de nujol), utilizando Na2 SO4 como eletrólito suporte 0,2 mol/L. Na preparação dos eletrodos de pasta de carbono com e sem modificação, foram utilizados grafite em pó (ALDRICH) sintético com tamanho de partícula menor que 20μ, nanotubos de carbono de paredes multiplas em pó(ALDRICH) com teor de pureza de 98% e nujol (ALDRICH) como aglutinante. As análises voltamétricas, utilizando a voltametria de varredura linear (LSV), na janela de potencial de -0,2 a 0,8 V, ν= 100 mVs-1. A solução estoque de vitamina E foi preparada em acetonitrila a partir de um padrão de Sigma-Aldrich com pureza de 99%, concentração de 4,46x10-3 mol/L.
Resultado e discussão
A Figura 1 apresenta os voltamogramas em LSV com sulfato de sódio como
eletrólito de suporte (Curva 1) e para uma solução de vitamina E
4,46x10-3 mol/L utilizando EPC (Curva 2) e EPNC (Curva 3). Pode-
se observar a ausência de pico de oxidação e redução no primeiro
voltamograma caracterizando que nessa janela de varredura de potencial não
existe interferência do tampão. A eletroatividade da vitamina E é comprovada
com a presença de 1 pico de oxidação (Ip 1,03μA/Ep 0,16V) utilizando-se EPC,
já para o eletrodo de EPNC o pico de oxidação é deslocado para um potencial
mais positivo, observa-se um aumento na corrente de pico (Ip 2,75μA/Ep
0,53V) . O pico de oxidação ocorre quando em meio de ácido ou de base
adicionada, a oxidação do tocoferol (α-TOH) produz os radicais de cátions
(α-TOH+), que perdem prótons formando radicais (Burton, G.
W.; Ingold, K. U., 1986). A literatura descreve que na reação de
oxidação da vitamina E, esta envolvido um elétron (Lee., et al, 2005). A
detecção eletroquímica de tocoferóis baseia-se no pico de oxidação dos
radicais de α-TOH+. O ENPC apresenta eletroatividade maior
quando comparado ao EPC, o que pode ser comprovado pelo aumento na
intensidade da corrente de pico de oxidação, apresentado pelos voltamogramas
da vitamina E.
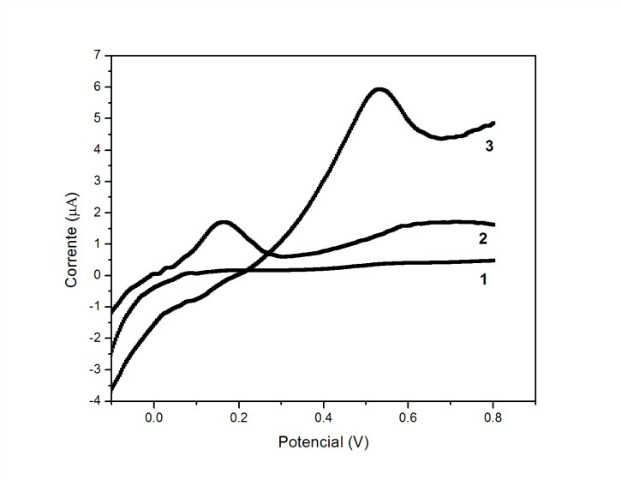
Voltamogramas em LSV obtidos para: Curva 1) Tampão Na2SO4 0,2 mol/L. Curva 2) EPC. Curva 3) EPNC. Vitamina E = 4,46x10-3 mol/L
Conclusões
Através dos resultados que foram obtidos pode-se concluir que o ENPC influencia positivamente na resposta eletroquímica do a-tocoferol. Isso foi comprovado por LSV onde o aumento da corrente de pico observado no EPNC é superior ao eletrodo de EPC. Indicando que os eletrodos de nanotubos de carbono, poderão apresentar maior sensibilidade na determinação eletroquímica da vitamina E.
Agradecimentos
UEMS, CNPq e FUNDECT
Referências
ANÁLISE DA VARIAÇÃO DA SOLUBILIDADE DE ALFA-TOCOFEROL COM A TEMPERATURA EM MISTURA ETANOL+ÁGUA; FONSECA, L. G.; RODRIGUES, J. B.; SILVA, C. V. da; MALAGONI, R. A. fevereiro 2015 vol. 1 num. 2 - XX Congresso Brasileiro de Engenharia Química.
Electrochemistry and environmental chemistry, Lee, S. B.; Lin, C. Y.; Gill, P. M. W.; Webster, R. D., J.Org.Chem. 2005, 70, 10466-10473.
M. F. Marcus, M. D. Hawley, Biochim. Biophys. Acta. 1970, 201, 1.
Vitamin E: application of the principles of physical organic chemistry to the exploration of its structure and function, Burton, G. W.; Ingold, K. U., Acc. Chem. Res. 1986, 19, 194-201.
Yoshida, Y.; Niki, E.; Noguchi, N. Comparative study on the action of tocopherols and tocotrienols as antioxidante: chemical and physical effects. Chemistry na Physics of Lipids, v. 1, p. 1-13, 2003.