ISBN 978-85-85905-15-6
Área
Química Analítica
Autores
Shimizu, L.C.B. (UFG/REGIONAL JATAÍ) ; de Oliveira, G.M. (UFG/REGIONAL JATAI)
Resumo
Os eletrodos de pasta de carbono (EPC) têm despertado grande interesse para o desenvolvimento de métodos quantitativos para análises de fármacos, por apresentarem inúmeras vantagens, como: facilidade no preparo, possibilidade de modificação e elevada seletividade. Neste trabalho foi proposto o uso de um eletrodo de pasta de carbono modificado com nanopartículas de prata eletrodepositada in situ para a determinação eletroanalítica de dopamina (DA) em fármaco. O estudo foi realizado por voltametria cíclica(CV) e por voltametria linear (LV). Verificou-se que apesar das curvas voltamétricas apresentarem diferenças em correntes/cargas anódicas em soluções sem e com DA, e ter sido possível obter uma região de linearidade para a curva analítica, esta não apresentou boa reprodutibilidade.
Palavras chaves
eletrodo pasta carbono; nanopartículas de prata; dopamina
Introdução
A dopamina (DA) é um importante neurotransmissor catecolaminérgico que atua na regulação de áreas motoras, aprendizagem e alimentação, sendo que distúrbios do sistema dopaminérgico podem estar associados a condições patológicas como o Mal de Parkinson e a esquizofrenia (MAHANTHESHA, p. 1, 2013). A DA está presente em pequenas quantidades (0,01–1,0 μM) no fluido extracelular do cérebro (THIAGARAJAN et al, p.212, 2007) o que representa um grande desafio para a proposição de métodos analíticos capazes de quantificar este neurotransmissor. Alguns métodos de análise química são usados para detecção e quantificação de dopamina, tais como: a espectrofotometria na região do UV- visível (PALOMAR-PARDAVÉ, p. 92, 2011), a cromatografia líquida (NIKOLAJSEN, et al, p. 1, 2001) e a eletroforese capilar (ZHAO, et al, p. 2652, 2011). Entretanto, o desenvolvimento de métodos eletroanalíticos tem despertado interesse dado a sua elevada seletividade, baixo custo de instrumentação e dos materiais utilizados, rapidez na análise quando comparados aos outros métodos e facilidade de transporte e montagem do equipamento (portáteis). Ademais, outra grande vantagem das técnicas eletroanalíticas está na possibilidade da análise ser realizada sem necessidade de etapas de pré-purificações ou de separações prévias (SATHISHA et al, p. 4, 2014). Vários métodos eletroanalíticos têm sido propostos para a determinação de dopamina em amostras biológicas e farmacêutica, destacando-se o uso de eletrodos de pasta de carbono modificados (MOZLOUM-ARDAKANI et al, p. 148, 2010; TASHKHOURIAN, et al, p. 85, 2009). Os eletrodos de pasta de carbono (EPC) foram primeiramente descritos por Adams (ADAMS, p. 1576, 1958) e pertencem a um grupo especial de eletrodos compósitos de carbono, sendo que algumas razões contribuem para que este eletrodo seja largamente utilizado, como: facilidade de obtenção da pasta de carbono (PC), à elevada seletividade e as múltiplas possibilidades de modificação físico-química da PC. Dentre os modificadores utilizados em eletrodo de pasta de carbono (EPC) estão as nanopartículas metálicas, uma vez que podem apresentar excelentes propriedades eletrocatalíticas, principalmente nos casos de metais nobres. O uso de nanopartículas de prata (SNP) em análises voltamétricas é relativamente recente, Wang et al (WANG et al, p. 154, 2004) obteve melhora na atividade eletrocatalítica de um eletrodo de carbono vítreo modificado com SNP, quando comparado à um eletrodo de disco de prata convencional. Este eletrodo foi testado para a determinação de tiocianato em saliva humana e as nanoparículas obtidas ex situ. Considerando-se a importância do uso de nanopartículas metálicas em EPCMs, o objetivo deste trabalho foi investigar a possibilidade do uso do processo de eletrodeposição in situ de prata metálica como pré-etapa no processo de oxidação de dopamina e aplicação deste eletrodo no desenvolvimento de um método quantitativo para a mesma em amostras de medicamento.
Material e métodos
Todos os reagentes utilizados foram de grau analítico: NaCl (Proquimios®), AgNO3(Plat-Lab®), pó de grafite (Dinâmica®, granulometria < 50 μm), óleo mineral (Isofar®), cloridrato de dopamina (Sigma-Aldrich), bissulfito de sódio (Dinâmica ®), NaH2PO4 (Isofar®) e Na2HPO4 (Isofar®). As soluções aquosas foram preparadas com água destilada. As medidas eletroquímicas foram obtidas empregando-se um potenciostato/galvanostato IVIUM modelo Compactstat 800 mA/10V em uma célula eletroquímica de três eletrodos. Utilizou-se como eletrodos de referência, contra eletrodo e trabalho respectivamente: Ag/AgCl, KCl 1,0 mol L-1; fio de platina e eletrodos de pasta de carbono modificados com AgNO3, com e sem NaCl (EPCMs). A análise morfológica do eletrodepósito de prata foi realizada por microscopia eletrônica de varredura (MEV) e de transmissão (MET), utilizando se um microscópio de detecção por elétrons retroespalhados modelo JSM IT 300 (JEOL®) de baixo vácuo e um microscópio eletrônico de transmissão modelo JEM 2100 (JEOL®).A pasta de carbono modificada (PCM) foi obtida preparando-se inicialmente uma mistura de pó de grafite com AgNO3 e NaCl. Para tanto, os sais (AgNO3 e NaCl) foram dissolvidos em álcool etílico anidro 99,8% (Synth®) em um béquer, seguido pela adição de pó de grafite sob agitação mecânica. Esta mistura foi colocada para aquecimento em banho maria a 80° C com agitação por ultrassom, até que todo álcool fosse evaporado. A etapa seguinte foi a trituração de pó de grafite modificado e óleo mineral na proporção em massa de 70:30, em um almofariz de ágata. O EPCM foi montado em seringa de polipropileno (Φ interno de 4,45 mm) com a extremidade cortada, tendo como contato elétrico um fio de cobre. Para evitar a eletrodeposição da prata sobre o cobre foi inserida uma pré-camada de PC sem modificador sobre a extremidade do fio e sobre esta a PCM. A superfície do eletrodo foi polida com papel manteiga, aguardando-se 24 h antes de usar o dispositivo em medidas.
Resultado e discussão
A Fig. 1 (a) mostra uma curva voltamétrica típica para o EPCM contendo 1,0 ×
10-4 mol AgNO3/1,0 × 10-4 mol NaCl/ g PC em
solução de NaCl 1,0 mol L-1, a qual podem ser destacadas três
regiões catódicas (c1, c2 e c3) e uma anódica
(a1). Os processos que ocorrem a potenciais mais negativos que
0,000 V (c1) e -0,150 V (c2) estão relacionados a
redução de íons prata(I), enquanto que na região c3 ocorre a reação
de desprendimento de gás hidrogênio (RDH) em paralelo a deposição de prata. A
região anódica a1 está relacionada à oxidação da prata metálica.
Além disso, estudos voltamétricos mostraram que a redução de íons prata
ocorreu preferencialmente na camada mais próxima da interface PC/solução
aquosa, a qual foi fortemente influenciada pelo NaCl adicionado dentro da PC
(SHIMIZU, p. 29, 2015). As Figs. 1(b)-(c) mostram as imagens obtidas por MEV e
MET respectivamente para os eletrodepósitos de prata crescidos nos EPCMs em
potencial de deposição (Ed) de -0,300 V com carga de
deposição (qd) de 1,21 × 10-1 C (Figs. 2(a)-(b))
e 8,74 × 10-3 C. A imagem de MEV indica que a deposição de prata
ocorreu de forma heterogênea no volume de PC analisado e que recobriu
preferencialmente algumas placas de carbono. De modo geral, verifica-se que
nas placas recobertas, ocorreu um alto percentual de recobrimento por uma
camada de prata compacta com cristalitos de diferentes tamanhos, de escala
nanométrica e micrométrica. A determinaçaõ de dopamina (DA) através de métodos
eletroanalíticos tem sido realizada em sua maioria em soluções tampão fosfato
(PBS) em diferentes pH, o qual também atuou como eletrólito de suporte sendo
que alguns trabalhos tem demonstrado bons resultados em soluções de PBS em pH
7,0 (ATTA, p. 21, 2014; THOMAS, p. 73, 2012). Ademais, um dos excipientes em
formulações farmacêuticas de cloridrato de dopamina é o bissulfito de sódio
(Na2S2O5). Deste modo o estudo do uso dos
EPCMs para determinação de dopamina (DA) foi realizado em soluções de PBS (pH
7,0) e NaCl 0,10 mol L-1, sem e com
Na2S2O5 0,010 mol L-1. Em solução
contendo PBS e Na2S2O5 (resultado não
apresentado), observou-se que os perfis voltamétricos para os eletrodos foram
bastante similares em soluções sem e com DA, não apresentando resultado
satisfatório para o desenvolvimento do método eletroanalítico. As Figs. 2 (a)-
(b) mostram as curvas voltamétricas típicas dos EPCMs em solução de NaCl 0,10
mol L-1, sem e com DA. Pode-se observar que as correntes/cargas
anódicas em solução contendo DA são maiores, indicando que a oxidação da DA
ocorreu em paralelo à da prata. Ademais, verificou-se que a razão entre a
carga anódica (qa) para a curva voltamétrica em solução sem
e com DA, em solução sem Na2S2O5 (razão de
1,57) e com Na2S2O5 (razão de 1,76), foram
bastante similares, porém foram menores que aquelas obtidas utilizando-se o
EPC sem AgNO3 (razão de 1,88, para solução contendo
Na2S2O5). O desenvolvimento de uma curva
analítica por voltametria cíclica para determinação de DA nestas soluções não
foi satisfatória. Também foi investigado o uso do EPCM fazendo-se uma
deposição potenciostática em -0,300 V (crescimento de cristalitos de prata)
seguida por varredura linear de potencial de -0,300 V a +1,500 V. Foram
investigados inicialmente a influência da velocidade de varredura anódica
linear (Fig. 2 (c)) e do tempo de deposição em -0,300 V (Fig. 2 (d)). A Fig. 2
(c) apresenta a razão entre cargas anódicas em função da velocidade de
varredura, a qual indicou que a razão entre cargas foi consideravelmente
constante. A Fig. 2 (d) apresenta a razão entre as cargas anódicas das curvas
voltamétrica lineares obtidas em solução de NaCl 0,10 mol L1, sem e
com DA, em função de diferentes tempos de deposição potenciostática e
velocidade de varredura de 100 mV s-1, o qual indicou que a
maiordiferença entre as qa foi para 15s de deposição. Deste
modo, optou-se por utilizar como parâmetros para a obtenção de uma curva
analítica o tempo de deposição de 15 s e velocidade de varredura de 100 mV
s-1. A Fig. 2 (e) mostra as curvas analíticas para DA obtidas em
solução de NaCl 0,10 mol
L-1/Na2S2O5 0,010 mol
L-1, utilizando-se os parâmetros otimizados. Pode-se observar uma
região de linearidade na faixa de concentração de 2,00 × 10-4 a
9,50 × 10-4 mol L-1, porém, não se tem boa
reprodutibilidade entre as medidas obtidas com diferentes eletrodos e
diferentes dias. Este resultado de baixa reprodutibilidade quando se tem
bissulfito de sódio, indica que nestas condições avaliadas não é possível
o desenvolvimento um método para a determinação de dopamina.
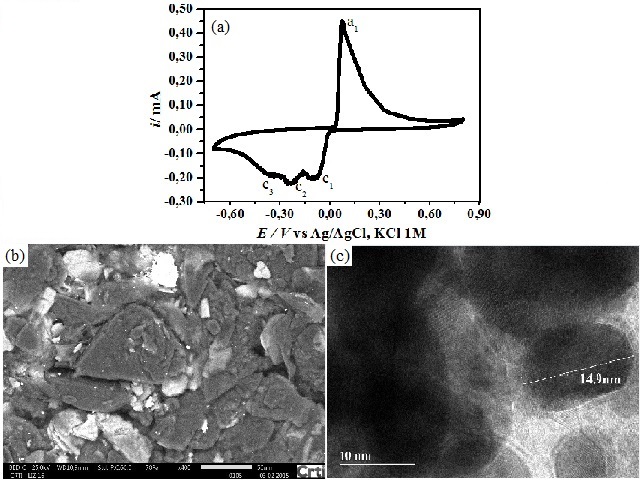
(a)Voltametria Cíclica EPCM; (b)MEV e (c)MET dos eletrodepósitos obtidos no EPCM em Ed=-0,300 V e v=10 mV/s. Solução NaCl 0,10 mol/L.
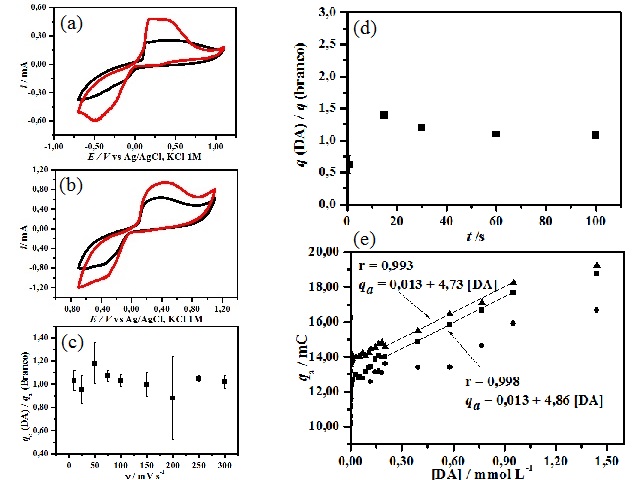
CV do EPCM em NaCl 0,10 mol/L, (a)sem (b)com Na2S2O5, v=10 mV/s. Razão entre cargas anódicas em função (c)velocidade (d)tempo.(e) Curva calibração DA.
Conclusões
Os resultados obtidos neste trabalho mostraram que a oxidação de dopamina durante a voltametria (Cíclica ou Linear) com o EPCM contendo AgNO3/NaCl ocorreu em paralelo a oxidação de prata. Verificou-se a possibilidade de obtenção de uma curva analítica para o eletrodo em solução de NaCl, porém, a adição de bissulfito de sódio (presente no medicamento) conduziu a um sistema com baixa reprodutibilidade, inviabilizando o uso deste eletrodo nas condições investigadas para a determinação de dopamina em formulações farmacêuticas.
Agradecimentos
Ao Programa de Pós Gradução em Ciências Aplicadas à Saúde/ UFG Regional Jataí
Referências
ADAMS, R.N. Carbon Paste Electrodes. Anal Chem, 1576, 1958.
ATTA, N. F.; ALI, S. M.; EL-ADS, E. H.; GALAL, A. Nano-perovskite carbon paste composite electrode for thesimultaneous determination of dopamine, ascorbic acid and uric acid. Electrochim Acta, n° 128, 16–24, 2014.
MAHANTHESHA, K. R., SWAMY, B. E. Pretreated/Carbon paste electrode based voltammetric sensors forthe det;ection of dopamine in presence of ascorbic acid and uric acid. J Electroanal Chem, n° 703, 1–8, 2013.
MAZLOUM-ARDAKANI, M.; BEITOLLAHI, H.; AMINIB, M. K.; MIRKHALAF, F.; ABDOLLAHI-ALIBEIK, M. New strategy for simultaneous and selective voltammetric determination of norepinephrine, acetaminophen and folic acid using ZrO2 nanoparticles-modified carbon paste electrode. Sensors Actuat B, n° 151, 243–249, 2010.
NIKOLAJSEN, R. P. H.; HANSEN, A. M. Analytical methods for determining urinary catecholamines in healthy subjects. Anal Chim Acta, n° 449, 1–15, 2001.
PALOMAR-PARDAVE, M.; ALARCON-ANGELES, G.; RAMIREZ-SILVA, M. T.; ROMERO-ROMO M.; ROJAS-HERNÁNDEZ, A.; CORONA-AVENDAÑO, S. Electrochemical and spectrophotometric determination of the formation constants of the ascorbic acid-b-cyclodextrin and dopamine-b-cyclodextrin inclusion complexes. J Incl Phenom Macrocycl Chem, n° 69, 91–99, 2011.
SATHISHA, T. V.; KUMARA SWAMY, B. E.; SCHELL, M.; ESWARAPPA, B. Synthesis and characterization of carbon nanoparticles and their modified carbon paste electrode for the determination of dopamine. J Electroanal Chem, n° 720-721, 1–8, 2014.
SHIMIZU, L. C. B. Desenvolvimento de um eletrodo de pasta de carbono modificado por prata eletrodepositada in situ e determinação eletroanalítica de dopamina. Dissertação de mestrado. 85 p. Universidade Federal de Goiás. Jataí, 2015.
TASHKHOURIAN, J.; NEZHAD, M. R. H.; KHODAVESI, S. J. Silver nanoparticles modified carbono nanotubes paste electrode for simultaneous determination of dopamine and ascorbic acid. J Electroanal Chem, n° 633, 85-91, 2009.
THIAGARAJAN, S.; CHEN, S. M. Preparation and characterization of PtAu hybrid film modified electrodes and their use in simultaneous determination of dopamine, ascorbic acid and uric acid. Talanta, n° 74, 212–222, 2007.
WANG, G. F.; LI, M.G.; GAO, Y. C.; FANG, B. Amperometric Sensor Used for Determination of Thiocyanate with a Silver Nanoparticles Modified Electrode. Sensors, n° 4, 147-155, 2004.
ZHAO, Y.; ZHAO, S.; HUANG, J.; YE, F. Quantum dot-enhanced chemiluminescence detection for simultaneous determination of dopamine and epinephrine by capillary electrophoresis. Talanta, n ° 85, 2650–2654, 2011.