ISBN 978-85-85905-15-6
Área
Química Analítica
Autores
Ribeiro, C.L. (UNIVERSIDADE DE BRASÍLIA) ; Souza, J.R. (UNIVERSIDADE DE BRASÍLIA) ; Paterno, L.G. (UNIVERSIDADE DE BRASÍLIA)
Resumo
O trabalho teve como objetivo quantificar o ácido salicílico extraído de orégano com HPLC/UV-Vis. Fases móveis diferentes foram testadas para se obter melhor sensibilidade e rapidez nas medidas. O limite de detecção e quantificação do método foi de 5,52 e 13,42 µg.L-1 respectivamente. A extração realizada teve recuperação de 82 % e as amostras de orégano analisadas apresentaram valor de concentração de 158,1±0,23 mg.Kg-1. O método proposto mostrou-se sensível e eficiente demonstrando que o orégano é uma importante fonte de ácido salicílico.
Palavras chaves
orégano; ácido salicílico; cromatografia
Introdução
Orégano (Origanum vulgare) é amplamente utilizado como um condimento e seu sabor e cheiro são muito apreciados em todo o mundo para aplicações culinárias. Esta erva aromática bem conhecida tem propriedades medicinais devido ao alto teor de compostos fenólicos (AGIOMYRGIANAKI et al, 2012). Dentre esses fenólicos é possível a presença de ácido salicílico (AS) que é um ácido fenólico produzido por plantas, como parte de seus sistemas de defesa contra o ataque de patógenos e estresse ambiental (DUTHIE et al, 2011). Este composto é o princípio ativo da aspirina, medicamento que reduz o risco de doença cardiovascular e atua como anti-inflamatório (BLACKLOCK et al, 2001). Diante disso, este trabalho tem como objetivo realizar a extração do ácido salicílico presente no orégano e quantificar com HPLC/UV-Vis.
Material e métodos
A extração do ácido salicílico no orégano foi realizada com três diferentes procedimentos apresentados a seguir, até se atingir valores aceitáveis de recuperação. Em todos os procedimentos as amostras foram previamente secas em estufa por 5 horas na temperatura de 55 °C. Procedimento 1: 2 g de orégano foram misturados com 10 mL de acetonitrila e 2 mL de ácido clorídrico 0,1 N e agitado em mesa rotatória por 2 horas à temperatura ambiente. A suspensão foi filtrada em papel filtro Whatman n°41. O solvente foi evaporado e os resíduos redissolvidos em 10 mL de fase móvel que foram filtrados em membrana de 0,45 µm. Este mesmo procedimento foi realizado substituindo acetonitrila por metanol e em outra adaptação foi realizado repetições por três vezes da extração na mesma amostra com um tempo de 1 hora cada em mesa rotatória (KIM et al, 2006 adaptado). Procedimento 2: Moagem de 1g de orégano adicionando posteriormente 20 mL de água:acetonitrila:ácido acético (54:45:1), a amostra foi agitada em mesa rotatória por 1 minuto e colocada em banho ultrassom por 30 minutos, o extrato foi então filtrado em membrana de 0,45 µm (VENEMMA et al, 1996). A quantificação foi realizada em um cromatógrafo líquido com detecção UV- Vis (Varian 920-LC), coluna phenomenex C18 (100x4,6 mm; 2,6 µm). O melhor comprimento de onda escolhido para as distintas fases móveis estudadas foi feito por análise em espectrômetro de UV-Vis (Agilent).
Resultado e discussão
Fases móveis diferentes foram testadas na concentração de 1,2 mg.L
-1 de AS
para obtenção de maior sensibilidade e menor tempo de retenção na medida do
ácido salicílico. A tabela 1 mostra os resultados obtidos.
A fase móvel escolhida foi a água: acetonitrila: ácido acético (54:45:1)
pois apresentou boa resolução do pico, maior sensibilidade e menor tempo de
retenção tornando a análise mais rápida. O eluente utilizado foi a própria
fase móvel.
A curva analítica apresentada na figura 1, obteve R2= 0,997 demonstrando
linearidade na relação entre a concentração medida e a área do pico. O
limite de detecção e quantificação do método proposto foi de 5,52 e 13,42
µg.L-1 respectivamente, valores estes abaixo dos limites descritos na
literatura para determinação de ácido salicílico por HPLC (WHEN et al,
2005). A faixa linear de trabalho foi de 0,1 mg.L-1 á 60 mg.L-1.
Dentre os procedimentos de extração do ácido salicílico no orégano o
realizado em mesa rotatória mesmo sendo feita adaptações obteve baixa
eficiência com valores de recuperação menores de 60%. O procedimento 2
apresentou valor de recuperação de 82%, mostrando a importância da moagem da
amostra e da realização de extração em ultrassom. As amostras de orégano
apresentaram valores de concentração de 158,1±0,23 mg.Kg-1 de ácido
salicílico valor acima do encontrado na literatura que foi de 11,8 mg.Kg-1
(VENEMMA et al, 1996).
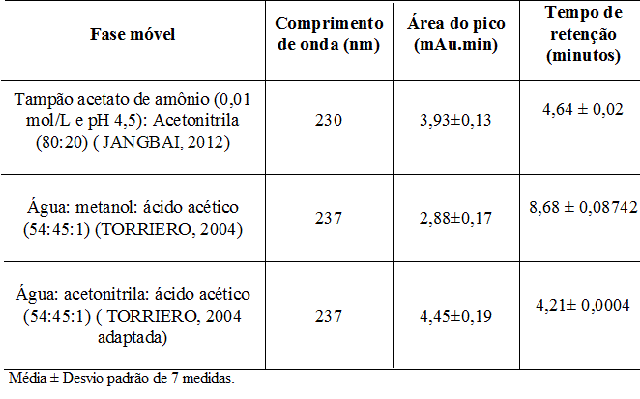
Comparação de diferentes fases móveis na detecção de ácido salicílico
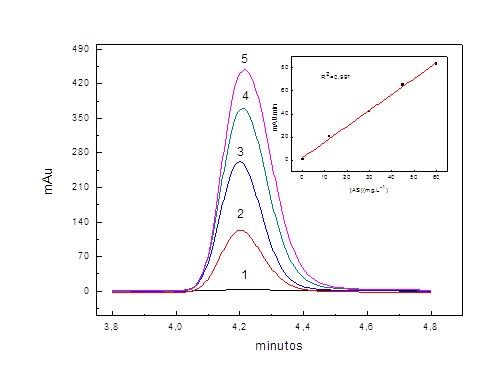
Cromatogramas de padrão de ácido salicílico nas concentrações (1) 0,1 (2) 12 (3) 30 (4) 45 e (5) 60 mg.L-1
Conclusões
O orégano é uma importante fonte de ácido salicílico, podendo ser alvo de estudos quanto a suas propriedades medicinais diante da evidência da presença desse composto terapêutico. O método de análise descrito nesse trabalho apresentou alta sensibilidade, rapidez e eficiência na determinação de ácido salicílico em orégano.
Agradecimentos
Ao apoio financeiro da UnB, Capes e FAP-DF.
Referências
AGIOMYRGIANAKI, A.; DAIS, P. Simultaneous determination of phenolic compounds and triterpenic acids in oregano growing wild in Greece by 31P NMR spectroscopy. Magn. Reson. Chem., 2012.
BLACKLOCK, C. J.; LAWRENCE, J. R.; WILES, D.;MALCOLM, E. A.; GIBSON, I. H.; KELLY, C. J.; PATERSON J. R. Salicylic acid in the serum of subjects not taking aspirin. Comparison of salicylic acid concentrations in the serum of vegetarians, non-vegetarians, and patients taking low dose aspirin. J Clin Pathol,n°54, 553–555, 2001.
DUTHIE, G. G.; WOOD, A. D. Natural salicylates: foods, functions and disease prevention. Food Funct., n° 2, 515-520, 2011.
JANGBAI, W.; WONGWILAI, W.; GRUDPAN, K.; LAPANANTNOPPAKHUN S. Sequential Injection Chromatography as Alternative Procedure for the Determination of Some Food Preservatives. Food Anal. Methods, n°5, 631–636, 2012.
KIM, E. H.; KIM, S. H.; CHUNG, J. I.; CHI, H. Y.; KIM, J. A.; CHUNG, I. M. Analysis of phenolic compounds and isoflavones in soybean seeds (Glycine max (L.) Merill) and sprouts grown under diferente conditions. Eur Food Res Technol, 222, 201–208, 2006.
TORRIERO, Angel A.J.; LUCO, Juan M.; SERENO, L.;RABA, J. Voltammetric determination of salicylic acid in pharmaceuticals formulations of acetylsalicylic acid. Talanta, n° 62, 247–254, 2004.
VENEMA, D. P.; HOLLMAN, P. C. H.; JANSSEN, K. P. L. T. M.; KATAN, M. B. Determination of Acetylsalicylic Acid and Salicylic Acid in Foods, Using HPLC with Fluorescence Detection. J. Agric. Food Chem., 44, 1762-1767, 1996.
WEN, D.; LI, C.; DI, H.; LIAO,Y.; LIU, H. A Universal HPLC Method for the Determination of Phenolic Acids in Compound Herbal Medicines. J. Agric. Food Chem. n° 53, 6624-6629, 2005.