ISBN 978-85-85905-15-6
Área
Produtos Naturais
Autores
Gomes, F.A. (UEMS) ; Mota, J.S. (UEMS) ; Santos, V.A.C. (UEMS) ; Frota, C. (UNICAMP)
Resumo
Este trabalho apresenta o estudo fitoquímico das folhas de Peperomia pereskiifolia. As folhas foram secas a temperatura ambiente e posteriormente pulverizadas com auxílio de um moinho de facas, o material pulverizado foi submetido a três extrações com etanol (92%), o extrato etanólico foi particionado resultando nas frações hexânica, clorofórmica, acetato de etila e hidroalcóolica. As frações semelhantes (hexânica e clorofórmica) foram reunidas e fracionadas em coluna de sílica gel em gradiente crescente de polaridade com hexano e acetato de etila. O fracionamento resultou no isolamento do cromeno 7-Metoxi-5-metil-2, 2-dimetil-2H-1-cromeno-6- carboxilato, que foi identificado por RMN de 1H e 13C.
Palavras chaves
pereskiifolia; cromatografia; RMS
Introdução
A família Piperaceae inclui 14 gêneros, os gêneros Piper, Potomorphe, Sarcorhachis, Trianoeopiper e Peperomia são predominantes na América do Sul (CALLE, 1983). O gênero Piper é o mais numeroso com cerca de 2.000 espécies (QUIJANO et. al. 2006). Algumas espécies de Peperomia (Piperaceae) são utilizadas como plantas ornamentais (HELBSING et. al. 1996). Outras espécies de Peperomia são utilizadas na medicina popular (MBAH et. al. 2002; MONACHE et. al. 1996). Estudos demonstram que as espécies pertencentes a esta família possuem ação analgésica e anti-inflamatória (PINHEIRO et. al. 20110). A espécie Peperomia pereskiaefolia possui os seguintes nomes Populares Erva-de Vidro; Erva-de-jabuti, jabotimembeca; jabuti-Membeca; jimenasana (CALLE, 1983). O presente trabalho, teve como objetivo o isolamento e identificação das substâncias das folhas de P. pereskiaefolia, através de métodos cromatográficos e RMN (Ressonância Magnética Nucelar) respectivamente.
Material e métodos
As folhas de P. pereskiifolia foram coletadas em novembro de 2010 em Dourados-MS(S22012’37,7”, WO54054’59,9”), Brasil. A espécie foi identificada pelo Dr. Elsie Franklin Guimaraes (Jardim Botânico do Rio de Janeiro, no Rio de Janeiro, Brasil), o espécimum (Kato-1137) foi depositado no Herbário do Jardim Botânico do Rio de Janeiro, Rio de Janeiro, Brasil. As folhas foram secas(43,3g) a temperatura ambiente e pulverizado com auxílio de um moinho de facas. O material pulverizado foi submetido a três extrações com etanol (92%) e destas foram obtidas 2954mg do extrato etanólico, que posteriormente foram dissolvidas em 100 mL de metanol água 8/2 v/v. A parte solúvel foi submetida a extrações sucessivas com hexano (3 x 35mL) obtendo-se 40mg. A extração com clorofórmio (3 x 35 mL), resultou em 984mg. A extração com acetato de etila (3 x 35 mL), resultou em 984 mg e a fração hidroalcoólica resultou em um total de 659 mg. Todos os extratos foram concentrados em rotaevaporador sob pressão reduzida. Após a analise por cromatografia em camadadelgada, as frações hexânica e clorofórmica mostraram-se semelhantes, estas foram reunidas e submetidas a um fracionamento em coluna de 4 cm de diâmetro e 30 cm de comprimento, empregando sílica gel, eluída em gradiente de polaridade crescente com hexano e acetato de etila. Este fracionamento resultou em 286 frações, que foram coletadas em frascos tipo penicilina de 20 mL. As frações foram reunidas de acordo com a semelhança apresentada em cromatografia de camada delgada.
Resultado e discussão
Dentre as frações analisadas por cromatografia em camada delgada uma mostrou-
se pura, a fração 59. Esta foi enviada para análise em RMN. Os dados de RMN de
1H e 13C (tabela 1) foram comparados com a literatura (SALAZAR, et al 2005),
confirmando a identificação da substancia 1 [metil 7-metoxi-5-metil-2,2-
dimetil-2H-1-cromeno-6-carboxilato] (figura 1).
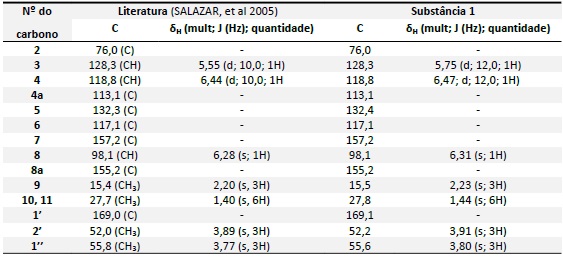
Dados comparativos de RMN entre os resultados obtidos na literatura e no presente trabalho.
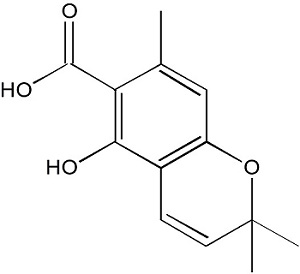
Estrutura molecular do 1 [metil 7-metoxi-5-metil- 2,2-dimetil-2H-1-cromeno-6-carboxilato]
Conclusões
O estudo fitoquímico resultou no isolamento de um cromeno.
Agradecimentos
UEMS, CNPq e Fundect.
Referências
CALLE, J. Estudy of some Piperaceae family species. Rev. Colom. Quím. Farm., v. 4, p 47-57, 1983.
QUIJANO, A. M. A.; MIRANDA, E. D. R. Areas of endemism and distribuition patterns for Neotropical Piper species (Piperaceae). J. Biogeography, v. 33, p. 1266-1278, 2006.
HELBSING, S.; RIEDERER, M.; ZOTZ, G. Cuticles of vascular epiphytes: efficient barriers for water loss after stomata closure. Annals of Botany, v. 1, p. 86-88, 2000.
MONACHE, F. D.; COMPAGNOSE, R. S. Secolignan from Peperomia glabella. Phytochemistry, v. 43, p 1097-1098, 1996.
MBAH, J. A.; TCHUENDEM, M. H. K.; FANE, P.; STERNER, O. Two chromones from Peperomia vulcanica. Phytochemistry, v. 60, p. 799-801, 2002.
PINHEIRO, B. G.; SILVA, A. S. B; SOUZA, G. E. P.; FIGUEIREDO, J. G.; CUNHA, F. Q.; LAHLOU, S.; SILVA, J. K. R; MAIA, J. G. S.; SOUZA, P. J. C. Chemical composition, antinociceptive and anti-inflammatory effects in rodents of the essental oil of Peperomia serpens (Sw.) Loud. Journal of Ethnopharmacology, v. 138, p. 479-485, 2011
SALAZAR, K. J. M.; PAREDES, G. E. D.; LLUNCOR, L. R.; YOUNG, M C. M.; KATO, M. J. Chromenes of polyketide origin from Peperomia villipetiola. Phytochemistry, v. 66, p. 573–579. 2005.