ISBN 978-85-85905-19-4
Área
Química Orgânica
Autores
Barros, C.G.C. (IFPE)
Resumo
Atualmente os compostos de origem tiazolidínica são de fundamental importância no desenvolvimento de medicamentos, tendo em vista a grande atividade biológica apresentada por seus derivados. Até o final do século passado e o início deste século, estes compostos se destacaram por apresentar atividades para diversos males. Várias pesquisas foram feitas tendo por base compostos obtidos a partir da Tiazolidina -2,4-diona, através de reações de N-alquilação, condensação ou tionação com aldeídos aromáticos. Visando estas propriedades foi assim, sintetizado o composto 5-(4- Acetamidabenzilideno)-tiazolidina-2,4-diona (Ju-655), pela reação de condensação da Tiazolidina-2,4-diona com o 4-Acetamidabenzaldeído em meio básico. Sua estrutura química foi confirmada por métodos espectroscópicos de RMN 1H.
Palavras chaves
Tiazolidina,; Tiazolidina-2,4-iona; Tiazolidinadiona
Introdução
A síntese de compostos tiazolidínicos é de grande importância para o desenvolvimento de novos medicamentos, tendo em vista a atividade biológica apresentada, como anticancerígena, anti-inflamatória, anticonvulsionante, antibacteriana, antiviral e hipoglicemiante (ALCÂNTARA, 2011). A Química Medicinal é a parte da química que envolve a invenção, descoberta, planejamento, identificação e preparação de novos compostos biologicamente ativos, com o estudo do seu metabolismo, a interpretação do seu modo de ação molecular e a construção das relações entre suas estruturas. (CARVALHO et al., 2003). A Tiazolidina-2,4-diona é um derivado tiazolidínico, correspondente a um anel de cinco membros, contendo um átomo de enxofre e outro átomo de nitrogênio nas posições 1 e 3, respectivamente, e carbonilas na posição 2 e 4 (BARROS, 2011). A literatura cita esses compostos como eficazes no tratamento de sistemas biológicos. A primeira reação foi sintetizada por Heintz, em 1865, a partir do esteretilcloroacético e tiocianato de potássio em meio ácido. Também pode ser sintetizada pela reação de ciclização entre os reagentes tiouréia e ácido monocloroacético.em meio aquoso e sob aquecimento e refluxo. Devido às atividades biológicas apresentadas pelos derivados tiazolidinicos é possível encontrar na literatura diversas pesquisas tendo por base, principalmente, a Tiazolidina- 2,4-diona. Esta pode sofrer reações de N-alquilação e condensação com aldeídos aromáticos. Dessa forma, a variedade de derivados tiazolidínicos é bastante grande, visto a diversidade de substituintes existentes, além da importância para a indústria de medicamentos. O composto 5-(4- Acetamidabenzilideno)-tiazolidina-2,4-diona foi obtido a partir da reação da Tiazolidina-2,4-diona e o aldeído aromático 4-Acetamidabenzaldeido
Material e métodos
A parte inicial desta reação foi a síntese da tiazolidina-2,4-diona partindo dos regentes ácido mono cloroacético e tiouréia em meio aquoso. A reação foi deixada em refluxo por um período de vinte e quatro horas. Após constatar a realização do produto, esse material foi cristalizado e seco para uso imediato. O composto 5-(4-Acetamidabenzilideno)-tiazolidina-2,4-diona (Ju – 655) foi sintetizado pela reação dos reagentes Tiazolidina-2,4-diona e 4- Acetamidabenzaldeído usando pirrolidina como catalizador (Fig 1). Em um balão de fundo redondo de 100 mL foram adicionados lentamente 0,051 g (4,35 x 10-4 moles) de Tiazolidina-2,4-diona (Ju-32) e 8 mL de etanol sob agitação magnética. Após a total solubilização da tiazolidina-2,4-diona (Ju-32), foram adicionadas 02 gotas de pirrolidina como catalisador. A reação continuou sob agitação magnética por 25 minutos para formação do ânion que irá atacar a carbonila do benzaldeído e formar o produto desejado. Em seguida, foi adicionado lentamente 0,0698 g (4,27 x 10-4 mols) de 4- Acetamidabenzaldeído (AM– 01) previamente seco em estufa a 37º C. Logo após adição da pirrolidina ao reagente tiazolidina-2,4-diona o conteúdo reacional adquiriu cor amarela. A seguir, a reação foi transferida para o banho de óleo a 75 °C, com refluxo e agitação magnética. A reação foi acompanhada por cromatografia de camada fina durante todo o desenvolvimento. Após o término, o conteúdo reacional presente no balão foi transferido para um béquer e deixado sob a bancada para cristalizar. Os cristais formados foram separados por filtração a vácuo em funil de Buchner sinterizado e colocados para secar em estufa a 37 ºC. Após secagem do produto, o material foi pesado, calculado o rendimento e determinados o Ponto de Fusão, a solubilidade e o fator de retenção (Rf).
Resultado e discussão
O composto 5-(4-Acetamidabenzilideno)-tiazolidina-2,4-diona (Ju - 655) foi
purificado por meio de recristalização com acetona, apresentando ponto de
fusão por decomposição, maior que 300 ºC, e Rf = 0,53 no sistema hexano
̸acetato de etila, 0,25 / 0,75. A confirmação da pureza do produto foi
verificada por meio de cromatografia de camada fina usando dois sistemas
diferentes, para assegurar que nenhuma mancha fique sobreposta na placa,
devido às diferentes polaridades dos solventes escolhidos para compor o
sistema. Todos apresentaram apenas uma mancha na placa confirmando que o
produto estava sem impurezas. O outro sistema usado foi cloreto de
metileno/metanol, 0,85/0,15. A reação apresentou rendimento de 18,7 % de
cristais puros. O tempo reacional foi de 23 horas a temperatura de 75 ºC do
banho de óleo. O produto foi submetido aos testes de solubilidades em quinze
solventes a frio e a quente. A solubilidade a frio foi em THF, Dioxano e
Acetona. O espectro de RMN1H (300 MHz, DMSO-d6) apresentou sinais
característicos de cada hidrogênio. Os hidrogênios do substituinte (CH3) em
3,88 ppm, apresentados como singleto (s). Além disso, os hidrogênios
aromáticos benzílicos foram apresentados como dublete (d) com constante de
acoplamento (J) mostrados a seguir: dois duplos dubletes em 7,39 referentes
aos hidrogênios das posições 2 e 6 do anel aromártico com (J= 6,39 Hz e J=
1,51). Para o hidrogênio ligado a dupla ligação carbono-carbono da posição 5
do anel heterocíclico o sinal apresentado foi um singlete em 7,91 ppm. O
hidrogênio da ligação N-H do anel heterocíclico apresentou um singlete em
12,6 ppm. O Hidrogênio da ligação NH da amida referente a posição 4 do anel
aromático apresentou um pico referente a um singlete em 8,42 ppm. O espectro
de massa confirmou o peso molecular.
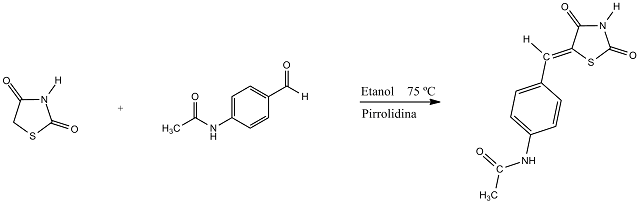
Síntese do composto 5-(4-Acetamidabenzilideno)- tiazolidina-2,4-diona (Ju-655).
Conclusões
O composto 5-(4-Acetamidabenzilideno)-tiazolidina-2,4-diona (Ju – 655) foi sintetizado usando tiazolidina-2,4-diona e 4-acetamidobenzaldeído e pirrolidina. como base. A reação foi processada em pouco tempo e foi acompanhada por cromatografia de camada fina. O Ju-655 foi apresentado puro após recristalização com acetona. A estrutura molecular foi determinada por espectrometria de Ressonância Magnética Nuclear de Hidrogênio e a espectroscopia de massas comprovou o peso molecular. Os sinais de NH metila e hidrogênios aromáticos foram observados. Todos as constantes químicas foram determinados.
Agradecimentos
A central analítica do Departamento de Química Fundamental da UFPE (DQF) pelos espectros realizados.
Referências
ALCÂNTARA, S.C. Síntese e avaliação das atividades citotóxicas e anti-microbianas de novas moléculas de Tiazolidina-2,4-diona/ Sandra Cristina de Alcântara. – Recife, 2011.
BARROS, C.D. Síntese de novos derivados da Tiazolidina-2,4-diona e avaliação como potenciais agentes terapêuticos/ Cleiton Diniz Barros. – Recife, 2011.
LIMA, J. G. Alguns aspectos químicos do anel Tiazolidina-2,4-diona. Rev. Univ. Rural, Sér. Ciênc. Exatas e da Terra, 18/20 (1/2): 1-8.











