ISBN 978-85-85905-19-4
Área
Produtos Naturais
Autores
Siqueira Pantoja, S. (UFPA) ; Albuquerque de Mescouto, V. (UFPA) ; Barbosa Albuquerque, C.F. (UFPA) ; Cunha de Melo, K. (UFPA) ; da Rocha Filho, G.N. (UFPA) ; Ferreira da Costa, C.E. (UFPA) ; Zamian, J.R. (UFPA) ; Santos do Nascimento, L.A. (UFPA)
Resumo
O buritizeiro é uma palmeira encontrada abundantemente na região Amazônica, dos frutos desta palmeira é extraído um óleo de cor alaranjada, rico em ácido oléico (C18:1), e bastante resistente a oxidação, devido sua composição em carotenóides, tocoferóis e compostos fenólicos, que são antioxidantes naturais. Diante do exposto, o presente estudo objetivou obter extratos etanólicos da polpa do buriti e avaliar o efeito da adição destes extratos para melhorar a estabilidade oxidativa do óleo de castanha, utilizando aparelho Rancimat. Os resultados obtidos foram satisfatórios, visto que, com a adição dos extratos houve um aumento no período de indução do óleo de castanha.
Palavras chaves
Buriti; Antioxidante natural; Estabilidade oxidativa
Introdução
O buritizeiro (Mauritia flexuosa L.f.) é uma palmeira encontrada nos biomas Amazônico e Cerrado, nos Estados do Acre, Amazonas, Rondônia, Mato Grosso, Goiás, Pará, Minas Gerais, São Paulo, Piauí e Maranhão. Encontra-se em lugares alagados, cada palmeira pode produzir de 150 a 200 Kg de fruto por safra, o fruto desta palmeira tem uma cor avermelhada, possui uma polpa com aroma peculiar, o qual geralmente é consumido na forma de doces, geleias, sorvetes, compotas e vinhos (Figura 1) (LORENZI et al., 2004; MARTIN, 1999). O interesse no estudo dos compostos fenólicos tem aumentado muito, devido principalmente à habilidade antioxidante destas substâncias em sequestrar radicais livres, os quais são prejudiciais à saúde humana (DORMAN et al., 2003). Os antioxidantes apresentam-se como uma alternativa para prevenir a deterioração oxidativa dos alimentos e minimizar os danos oxidativos nos seres vivos. Como o emprego de antioxidantes sintéticos na indústria de alimentos tem sido alvo de questionamentos quanto à inocuidade, demonstrando a possibilidade desses antioxidantes apresentarem alguma toxidez (BAUER et al., 2001), pesquisas encontram-se voltadas para a busca de compostos naturais que exibam esta propriedade funcional (MELO E GUERRA, 2002). O óleo da castanha do Brasil tem sido utilizado como óleo fino de mesa e na formulação de cosméticos (FREITAS et al., 2007), o óleo utilizado neste trabalho foi adquirido em uma empresa local, sem adição de antioxidantes e apresentava um baixo período de indução, por este motivo houve o interesse em testar o extrato neste óleo vegetal.
Material e métodos
Preparação dos extratos. Foram pesadas 50 gramas da polpa do buriti in natura e trituradas com 200 mL de etanol, a mistura foi mantida sob agitação por 12 horas. Em seguida efetuou-se a centrifugação do material, o sobrenadante foi separado e foram realizadas mais duas extrações 50 mL de etanol e centrifugação. A polpa foi filtrada, para retirada de todo álcool. O extrato obtido foi concentrado em evaporador rotativo e posteriormente guardado em vidro âmbar em geladeira para posteriores análises. Determinação da Estabilidade oxidativa. A Estabilidade Oxidativa foi determinada utilizando-se um Rancimat, modelo 743 da marca Metrohm, de acordo com o método AOCS Cd 12b-92. Foram utilizadas 5g do óleo de castanha, o fluxo de ar de 10L/h e a temperatura de 110 °C. Adição do extrato vegetal ao óleo. Os extratos foram utilizados para avaliar a influência das concentrações destes na estabilidade oxidativa do óleo vegetal. Para tanto, foram utilizadas concentrações de 500, 1000 e 2000 ppm de cada extrato no óleo de castanha, a homogeneização foi efetuada utilizando agitação magnética por 10 minutos. Em seguida, foram pesadas amostras de 5g, que foram levadas ao aparelho Rancimat para determinação do período de indução.
Resultado e discussão
Na tabela 1 são mostrados os períodos de indução obtidos para o óleo de
castanha com o extrato de buriti. As análises em aparelho Rancimat são
utilizadas principalmente para medir o período de indução, através da
detecção da formação de ácidos voláteis formados durante a oxidação do óleo
(MATHAUS, 1996). O óleo de castanha apresentava um período de indução baixo,
de apenas 2,1 h. Objetivando-se aumentar o período de indução deste óleo
adicionou-se o extrato alcoólico obtido da polpa dos frutos de buriti Este
extrato foi obtido da polpa in natura, obtendo-se um aumento significativo
no período de indução deste óleo. Como pode ser observado houve um aumento
de 2,3h no período de indução com a adição de 500 ppm de extrato; de 2,4h
com a adição de 1000 ppm e de 3,4h com a adição de 2000 ppm. Estes
resultados podem ser atribuídos a presença de antioxidantes naturais no
extrato obtido O teor de fenólicos totais em diferentes partes da espécie
Mauritia flexuosa, tais como folhas, polpa e casca dos frutos, mostra que
esta palmeira é rica em compostos polifenólicos, possuindo cerca de 378,07
mg Eq AG/100g (medido em equivalente de ácido gálico) na polpa, tais como:
ácido caféico, ácido clorogênico, narigerina, rutina, quercetina,
miricetina, entre outros (KOOLEN et al., 2013). Provavelmente estes
compostos fenólicos foram obtidos na extração alcoólica, sendo estes os
responsáveis pelo aumento no período de indução do óleo. Quanto maior a
concentração de fenólicos em um extrato, maior seu poder de inativação de
radicais livres através da doação de átomos de hidrogênio a estas espécies
(SOARES, 2002).

Frutos de buriti.
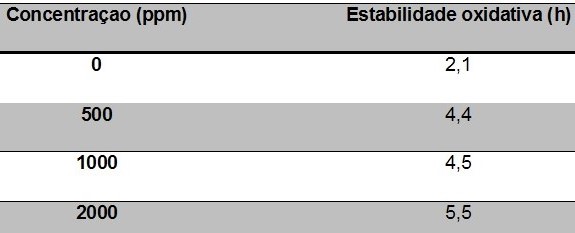
Estabilidade oxidativa do óleo de castanha com extrato alcóolico de buriti.
Conclusões
A partir do estudo desenvolvido foi possível constatar a eficiência da extração de antioxidantes naturais da polpa do buriti, visto que quando adicionou-se o extrato alcoólico ao óleo de castanha houve um aumento no período de indução. Assim, são necessários estudos mais profundos para caracterização do extrato, determinação e quantificação dos compostos bioativos com atividade antioxidante.
Agradecimentos
À UFPA (Universidade Federal do Pará), FAPESPA (Fundação de Amparo à Pesquisa do Estado do Pará), CNPq e LAPAC (Laboratório de Pesquisa e Análise de combustíveis) pel
Referências
AMERICAN OIL CHEMISTS´ SOCIETY. Official methods and recommended practices of the American Oil Chemists´ Society, Champaign, USA (A.O.C.S. Official Method Cd 12b-92: Oxidative Stability Index), 1992. BAUER, A.K. et al. The lung tumor promoter, butylated hydroxytoluene (BHT), causes chronic inflammation in promotion-sensitive BALB/cByJ mice but not in promotion-resistant CXB4 mice. Toxicology, v.169, n.1, p.1-15, 2001. DORMAN, H. J.D.; KOSAR, M.; KAHLOS, K.; HOLM, Y.; HILTUNEN, R. Antioxidant properties and composition of aqueous extracts from Mentha species, Hybrids, Varieties, and Cultivars. Journal of Agricultural and Food Chemistry, Washington, v.51, n.16, p.4563-4569, 2003. FREITAS, S.P.; FREITAS-SILVA, O.; DE MIRANDA, I.C.; COELHO, M.A.Z. Extração e fracionamento simultâneo do óleo da castanha-do-Brasil com etanol. Ciênc. Tecnol. Aliment., Campinas, 27(supl.), p.14-17, 2007. LORENZI, H., SOUZA, H. M., COSTA, J. T. M., CERQUEIRA, L. S. C., & FERREIRA, E. Palmeiras brasileiras e exóticas cultivadas. Nova Odessa: Instituto Plantarum, 2004.MARTIN, F.W. Perenial Edible Fruits of the Topics. Kansas City: United Departament of Agriculture, 1990. MATHÄUS, B. Determination of the oxidative stability of vegetable oils byrancimat and conductivity and chemiluminescence measurements. J. Am. OilChem. Soc. n.73, p.1039–1043, 1996. MELO, E.A.; GUERRA, N.B. Ação antioxidante de compostos fenólicos naturalmente presentes em alimentos. Boletim da Sociedade Brasileira de Ciências e Tecnologias de Alimentos, v.36, n.1, p.1-11, 2002. SOARES, S.E. Ácidos fenólicos como antioxidantes. Rev. Nutri., Campinas, v.15, n.1, p.71-81, 2002.











