ISBN 978-85-85905-19-4
Área
Química Verde
Autores
Loureiro, H.A. (UNIFAP) ; Cardoso, Y.M.N. (UNIFAP) ; Ferreira, I.M. (UNIFAP) ; de Oliveira, A.N. (UNIFAP)
Resumo
A utilização de biocatalizadores é uma alternativa aos processos químicos utilizados pela indústria que, em alguns casos, demandam altos custos e prejuízos à natureza. O objetivo deste trabalho é utilizar o caroço do cupuaçu na biotransformação de diferentes aldeídos como ferramenta alternativa aos métodos químicos existentes. Os resultados obtidos por meio de cromatografia em camada delgada e técnicas espectroscópicas demonstram que tal processo é viável e vantajoso, pois além de obter êxito na redução enzimática, o custo para adquirir a matéria-prima em grande quantidade é baixo.
Palavras chaves
biotransformação; biorredução; Theobroma grandiflorum
Introdução
O termo biotransformação abrange os processos em que enzimas que fazem parte de organismos vivos (microrganismos, plantas ou animais) são utilizadas para catalisar reações químicas, porém fora do sistema bioquímico, ou seja, com substratos não naturais (xenobióticos) às suas vias metabólicas (MOLINARI et al. 2007, FABER 2011). O emprego da biocatálise possibilita a aplicação dos princípios da Química Verde, uma vez que as reações biocatalisadas podem ocorrer em condições brandas de pH, temperatura e pressão, apresentando assim um excelente balanço de eficiência energética (LENARDÃO et al. 2003). Os produtos de interesse podem ser obtidos de forma altamente específica, evitando a formação de subprodutos e a ocorrência de reações “secundárias” e competitivas no meio reacional (FERREIRA et al. 2014). O uso de plantas como fontes de enzimas em biocatálise vem crescendo nos últimos anos, devido à simplicidade e ao baixo custo dos vegetais. Na literatura, há vários trabalhos com Daucus carota (cenoura) na redução de carbonila e o uso de diferentes espécies de Manihot (mandioca) na redução de aldeídos e cetonas (DOS SANTOS et al. 2009). O caroço do T. grandiflorum não possui grande utilidade comercial e, apesar de constituírem cerca de 20% do peso do fruto e possuírem alto valor nutritivo, as sementes são praticamente descartadas no beneficiamento do fruto (COHEN et al. 2005), o que reforça as vantagens da redução utilizando o caroço do T. grandiflorum, pois além de obter êxito na redução enzimática o custo para adquirir a matéria-prima em grande quantidade é baixo.
Material e métodos
O Theobroma grandiflorum (cupuaçu) foi adquirido no mercado local da cidade de Santana – AP. A polpa foi retirada e logo em seguida o caroço foi lavado, seco e armazenado em geladeira para posterior uso (4 °C). Em um frasco de 250 mL foi adicionado 100 mL de água destilada e autoclavado por 25 min à 121 °C. Em seguida 50 µL do aldeído solubilizado em 300 µL de etanol foi adicionado ao frasco reacional. Por fim, foi adicionado aproximadamente 12,20 g (1 unidade) do caroço de Theobroma grandiflorum. A reação foi acompanhada por cromatografia em camada delgada (CCD) a cada 48h e permaneceu em agitação magnética por 9 dias à temperatura ambiente. Após 9 dias de reação, a reação foi extraída com adição de 10 mL de água destilada e acetato de etila (3 x 50 mL). A fase orgânica foi seca com sulfato de sódio anidro, filtrada e o solvente foi rotaevaporado à pressão reduzida. Os produtos formados foram purificados por cromatografia em coluna por sílica gel 60, utilizando uma mistura de hexano e acetato de etila (7:3) como eluente. O composto 2a (Tabela 1) foi caracterizado por Cromatografia à Gás – Espectrometria de Massas.
Resultado e discussão
Foram selecionados diferentes aldeídos aromáticos para avaliar a influência
da cadeia e dos substituintes no processo enzimático. Para o aldeído 1a que
não contém grupos substituintes no anel aromático foi obtido o álcool 2a com
>99% de rendimento. O aldeído 1b e o aldeído 1d possuem tanto grupos
retiradores e doadores de elétrons e deram origem aos produtos 2b e 2d,
respectivamente, demonstrando que a reação de redução não é afetada pela
presença de tais grupos. Porém, nas reações 1e e 1f não foi observada a
formação do álcool, evidenciando que o tamanho da cadeia carbônica na qual o
grupo funcional está ligado influencia na reação de biotransformação. Este
resultado reforça o caráter altamente específico e quimiosseletivo das
enzimas (Tabela 1). As enzimas responsáveis pela redução de grupos
carbonílicos da classe das oxidases, neste caso podemos sugerir que este
processo é governado pela enzima álcool desidrogenase (ADH) (FERRAZ et al.
2008). Pela análise de CG-MS é possível confirmar a formação do composto
reduzido, com m/z = 138, através da ação das enzimas ADH provenientes do
caroço de cupuaçu (figura 2). A pesquisa continua em andamento e vem
demostrando ser promissora, pois além de mostrar que tal processo químico é
possível utilizando este resíduo como fonte biocatalítica, é também pioneiro
na utilização do caroço do cupuaçu para tal aplicação tecnológica.
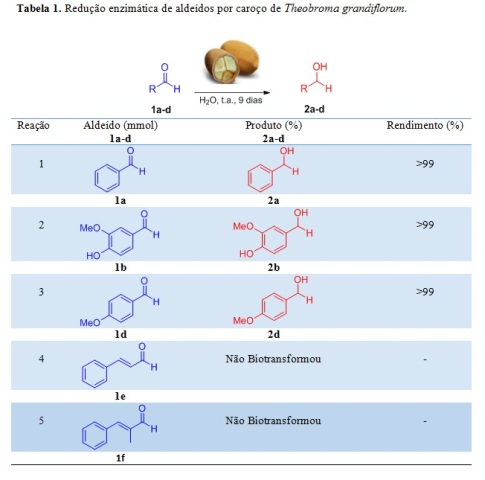
Redução enzimática de aldeídos por caroço de Theobroma grandiflorum.
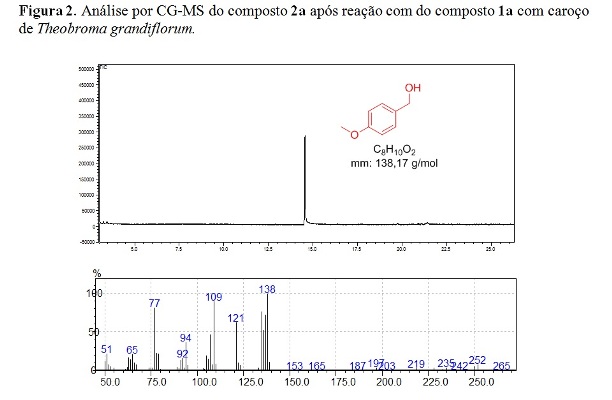
Análise por CG-MS do composto 2a após reação com do composto 1a com caroço de Theobroma grandiflorum.
Conclusões
Portanto, os resultados iniciais são satisfatórios e condizem com o objetivo do trabalho, demonstrando a possibilidade da utilização do caroço do cupuaçu como um biocatalizador. Além de mostrar as condições adequadas o mesmo é fonte de conhecimento para pesquisas futuras utilizando o cupuaçu ou outras plantas disponíveis na Amazônia como fonte enzimática para aplicação em biocatálise, seja na obtenção de novas substâncias ou de metodologias ambientalmente viáveis.
Agradecimentos
À UNIFAP pelo apoio financeiro, Projeto Nº 23125003351201556 / PAPESQ e ao Laboratório de Química Biocatálise e Química Orgânica – USP-IQSC.
Referências
FABER, K. Biotransformations in organic chemistry. 6.ed. Berlin: Springer-Verlag, 2011. 5p.
FERRAZ, Helena Maria Carvalho ; BIANCO, G. G. ; Bombonato, F. I. ; ANDRADE, Leandro H ; PORTO, A. L. M. . Bioreduction of substituted alpha-tetralones promoted by Daucus carota root. Química Nova, v. 31, p. 813-817, 2008.
FERREIRA, I. M.; ROCHA, L. C.; YOSHIOKA, S. A.; NITSCHKE, M.; JELLER, A. H.; PIZZUTI, L.; SELEGHIM, M. H. R.; PORTO, A. L. M. Chemoselective reduction of chalcones by whole hyphae of marine fungus Penicillium citrinum CBMAI 1186, free and immobilized on biopolymers. Biocatalysis and Agricultural Biotechnology, v. 3, n. 4, p. 358-364, 2014.
HANSON, J.R. An introduction to biotransformations in organic chemistry, 92 p., 1995.
LENARDÃO, E.J.; FREITAG, R.A.; DABDOUB, M.J.; BATISTA, A.C.F.; SILVEIRA, C.C. "Green chemistry" - Os 12 princípios da química verde e sua inserção nas atividades de ensino e pesquisa. Química Nova, v.26, p.123-129, 2003.
MOLINARI, F.; ROMANO, D.; GANDOLFI, R.; GUALANDRIS,R.; FERRARA, N. Biocatalysis for use in pharmaceutical manufacturing. Journal of Biotechnology, v.131, p.98-121, 2007.











