ISBN 978-85-85905-19-4
Área
Química Tecnológica
Autores
Côrtes, S.L. (UNIVERSIDADE ESTADUAL DE LONDRINA) ; Kimura, M. (UNIVERSIDADE ESTADUAL DE LONDRINA) ; Borsato, D. (UNIVERSIDADE ESTADUAL DE LONDRINA) ; Galão, O.F. (UNIVERSIDADE ESTADUAL DE LONDRINA) ; Moreira, I. (UNIVERSIDADE ESTADUAL DE LONDRINA) ; Costa, S.B. (UNIVERSIDADE ESTADUAL DE LONDRINA)
Resumo
Oito frutas diferentes foram analisadas para determinar o teor dos seguintes tipos de açúcares: glicose, frutose, sacarose e nistose. Neste trabalho foram analisadas as seguintes frutas: acerola, caju, cupuaçu, goiaba, jamelão de duas regiões(Santa Margarida e Londrina), manga Tommy, maracujá e uvaia por cromatografia líquida. Para os quatro tipos de açúcares, foram feitas curvas padrão para quantificação dos açúcares. As polpas apresentaram os seguintes resultados para açúcares totais: maracujá com 13,38%, manga com 11,61%, jamelão de Santa Margarida com 9,73%, caju 7,87%, jamelão de Londrina com 7,75%,goiaba com 6,93%, cupuaçu com 6,28%, uvaia com 3,27% e acerola com 1,79%.
Palavras chaves
Cromatografia líquida ; carboidratos ; açúcares de frutas
Introdução
Um dos fatores mais importantes de qualidade das frutas é o sabor, dado pelo teor de açúcares solúveis contidos nela e também de ácidos orgânicos. Durante o amadurecimento o conteúdo de ácidos orgânicos diminui e o de açúcares aumenta (MEDLICOTT, A.P.; THOMPSON, A.K. 1985). A sacarose é o principal açúcar da manga madura (MATOO, et al, 1975). Nas outras frutas a sacarose também se encontra presente, mas glicose, frutose e nistose também ocorrem. O açúcar também é muito importante para o consumo humano e para todos os organismos vivos, pois os açúcares são uma fonte de energia, faz parte do metabolismo humano (BRUICE, 2006; NELSON; COX, 2011). Os açúcares são carboidratos que constituem e mantêm partes importantes de todos os seres vivos. Nos primórdios da química os carboidratos eram representados com fórmulas moleculares que os fazem parecer hidratos de carbono, Cn(H20)n, justificando assim a origem de seu nome. Porém, não existe esse hidrato, mas os carboidratos são poli- hidroxialdeídos ou poli-hidroxicetonas. O poli-hidroxialdeídos são os que possuem algumas hidroxilas e um agrupamento aldeído ao longo de sua cadeia carbônica como exemplo a frutose e a poli-hidroxicetonas possui algumas hidroxilas e um agrupamento cetônico ao longo de sua cadeia carbônica, por exemplo, a glicose(BRUICE, 2006). Os seres vivos obtêm energia da glicose, pois a glicose sofre a oxidação com várias etapas e é o inverso da fotossíntese feito por plantas. As plantas usam tais processos para manterem-se em funcionamento e o restante vão armazenando, e uma dessas formas de armazenamento são em frutas que estão com as sementes, as quais vão perpetuar as espécies, seguindo o instinto de sobrevivência (NELSON; COX, 2011; BRUICE, 2006).O objetivo deste trabalho é identificar e quantificar os açúcares por cromatografia líquida encontrados nas amostras como potencial para a produção de álcool por fermentação.
Material e métodos
Cada análise foi programada com duração de 20 minutos, volume de injeção de 20 μL, temperatura do forno de 80°C e pressão de 1000 psi ±50. Através das curvas de calibração, foi possível obter os valores como a inclinação da reta e intersecção da reta que podemos apresentar como equações da reta e a coeficiente de determinação (R2)(SKOOG;HOLLER;CROUCH,2009).As absorvâncias das amostras estavam todas acima de LD e LQ, logo o método foi capaz de detectar e quantificar (SKOOG; HOLLER; CROUCH, 2009; RIBANI et al., 2004). Na determinação da concentração do analito foi considerado os fatores de diluição. Como todas as análises foram feitas em triplicatas, os resultados podem ser apresentados na forma de média, desvio padrão e o intervalo de confiança (IC) com o teste t de Student em nível de confiança de 95% sendo a probabilidade de encontrar um certo valor para as triplicatas de cada amostra (RIBANI et al., 2004; SKOOG; HOLLER; CROUCH, 2009).
Resultado e discussão
Foram identificados o tempo de retenção de cada padrão de forma individual para
se ter uma base comparativa entre os padrões e amostras.A nistose foi a que
possuiu o menor tempo de retenção devido a sua alta massa molecular e se
comparada com os demais açúcares e a disposição de seus carbonos redutores é
menor,assim tem menor interação com a fase estacionária.O tempo de retenção foi
de 4,7 min.A sacarose tem o menor tempo de retenção,devido a sua massa
molecular,interação com a fase estacionaria e é um dissacarídeo não redutor.O
tempo de retenção foi de 5,5 minutos.No padrão de glicose o tempo de retenção
foi de 6,3 min, na frutose encontrado de 9,2 minutos,sendo o tipo de
monossacarídeo com a maior interação com a fase estacionária.Assim a ordem de
menor para maior interação com a coluna foi nistose, sacarose, glicose e
frutose.Foi usado o método de padronização externa para a quantificação que
precisa construir curvas de calibrações para cada tipo de açúcar com o padrão
disponível,com cinco concentrações diferentes(ANVISA 2003).O LD e LQ para a CLAE
pode ser determinado de três formas: a visual, método sinal-ruído e baseado em
parâmetros da curva analítica (RIBANI et al., 2004).O método escolhido foi o
visual, que consiste em analisar qual a menor concentração do analito que possa
ser diferenciado do ruído por visualização.O mínimo de analito detectável e
quantificável pelo mínimo de concentração injetado, para a frutose e glicose foi
de 0,018%; para a nistose foi de 0,003% e para a sacarose foi de 0,002%.A
maioria dos sinais das amostras ficaram acima desses limites e os que ficaram
abaixo estão identificados como N.D.= não detectável nas tabelas.A acerola ficou
com 1,79 % de açúcares totais e 1,16% de redutores, ou seja a soma glicose e
frutose.De acordo com Brasil(2000) que é regulamento técnico geral para a
fixação dos padrões de identidade e qualidade de sucos de frutas do Ministério
da Agricultura,Pecuária e Abastecimento, uma Instrução normativa nº 01, 7 de
janeiro 2000, a polpa de acerola devia estar no intervalo de 4,0 - 9,5% de
açúcares totais naturais.Sendo que a polpa de acerola não possui a quantidade de
açúcar ideal.A soma dos açúcares da polpa de caju por CLAE ficou 7,87 % e dos
redutores ficou de 7,54%.O açúcar redutor próximo ao valor de Silva et al.(2012)
de 7,43±01,61%.E a polpa está de acordo com Brasil (2000).Os açúcares totais
naturais da polpa de caju devem ser no máximo 15 %.No Cupuaçu foi determinado
6,28% de açúcares totais e os redutores de 4,33%.O valor de açúcares totais não
se encontram nas exigências da legislação sobre açúcares totais naturais do
fruto (g/100g) que é de no máximo 6 % (BRASIL, 2000).Para a legislação deve ter
açúcares totais naturais da goiaba deve ser no máximo 15 % e
determinou-se 6,94% de açúcares totais, logo a polpa de goiaba se encontra de
acordo.Os açúcares redutores na cromatografia ficou de 5,73%.A polpa de jamelão
de Santa Margarida contém 9,74% de açúcares e de AR foi de 8,32%, na polpa de
jamelão de Londrina foi encontrado 7,76 % de açúcares e de AR foi encontrado
6,49%.A amostra de Santa Margarida ficou acima do valor relatado por Jadhav,
Kamble e Kadam (2009) de 8,09% de açúcares totais e o de Londrina foi o que
ficou mais próximo. A diferença entre as amostras para açúcar total foi de 20,34
% e para açúcar redutor foi maior ainda de 22,01 %.Rizzon e Miele (2005) fizeram
análises de maçãs de diferentes localidades de Santa Catarina e do Rio grande do
Sul, na qual se encontrou diferentes valores de concentração de açúcares, eles
afirmaram que o fato de algumas amostras possuírem teor maior estariam
relacionados às variáveis que participam na fotossíntese como a intensidade de
calor, a radiação solar e a umidade do solo.Quando por exemplo, uma fruta está
no período de maturação em regiões com clima quente, proporciona maior produção
de açúcar.Luciano et al.(2013)fizeram análises em uvas de diferentes tipos de
solo, relatam que os atributos e as demandas do solo influência na
disponibilidade de água nas plantas e seu desenvolvimento.O excesso de água, em
solos com baixa drenagem, prejudica a qualidade do fruto,ou seja, a
disponibilidade de água no solo modifica a concentração de açúcar,pois
ocorre menor consumo de carboidrato e crescimento vegetativo,tal que a
quantidade de carboidratos fiquem maiores e disponíveis para as frutas.Nessas
condições também favorece o amadurecimento e diminui o tamanho dos frutos,
devido a competição de carboidratos entre os frutos e outras partes da planta.
Então o que ocorreu com as uvas de Luciano et al.(2013) e maçãs de Rizzon;
Bernardi; Miele (2005) pode ter ocorrido com os jamelões.Na região de Bela Vista
do Paraíso possui a formação de unidade geológica de aluviões atuais que
predominam o solo arenoso, com intercalações de camadas argilosas, cascalho e
turfeiras(MINEROPAR, 2006b). E em Londrina pertence ao Grupo de São Bento –
Formação de Serra Geral, possui solos com terra roxa estruturada eutrófica,
latossolo roxo eutrófico entre outros (MINEROPAR, 2006a). Assim as duas
matrizes possuem solos diferentes e a do tipo arenoso não tem a retenção de
água, fica com a disponibilidade menor e faz com que os frutos desenvolvidos
nessa terra possuam maiores quantidades de açúcares ao compararmos com a de
terra roxa. Em relação ao clima, as diferenças entre essas duas localidades não
são muitas, assim não é uma justificativa para tal. Na amostra da manga ficou
11,61% de açúcares totais, porém a quantidade de açúcares redutores foi baixa se
comparada com as outras frutas aqui discutidas, já que o teor de 3,22%.Para
Rocha (2001) a manga Tommy possui 10,84 % de açúcares não redutores, assim o
valor encontrado, ficou abaixo, cujo valor da sacarose foi de 7,97%.Os picos
encontrados e quantificados estão de acordo com Bernardes-Silva (2003) que achou
em seus trabalhos usando a cromatografia líquida com outro método, apenas a
glicose, frutose e sacarose.Em seus trabalhos, a manga tinha teores menores que
1 % de glicose e explica que esse baixo valor é devido a razão da glicose por
frutose não ser equimolar, devido a hidrólise da sacarose pelas invertases em
que a fruta por via respiratória utiliza preferencialmente a glicose primeiro e
contendo mais frutose no sistema. Na legislação brasileira em relação à polpa de
manga exige que contenha açúcares totais naturais do fruto de no máximo 17 % e a
amostra trabalhada está de acordo(BRASIL, 2000).Foi determinado no método
cromatográfico que a polpa de maracujá possuía 13,31% de açúcares e 3,71% de
açúcares redutores.Em relação ao limite da legislação sobre a polpa é de no
máximo 18 % de açúcares totais naturais no fruto(BRASIL, 2000)com isso, a
amostra está de acordo.Ao comparar com o açúcar redutor ficou de acordo com
Ciabotti e Braga(2000) faixa de 3 a 5%.Para a uvaia determinou-se 3,27% de
açúcares totais e 1,94% de açúcares redutores.O valor de açúcares redutores
ficou próximo de 1,81±0,01% de açúcares redutores de Karwowski (2011) e muito
menor valor de 2,81±0,05%, em relação ao encontrado por Miyazawa(2009).Na tabela
1 dispõe os valores e identificação de açúcares totais detectáveis e
identificáveis para cada fruta em forma de média,IC e o desvio padrão.Analisa-se
na tabela 1 que a polpa que possui maior valor de açúcar total foi a de
maracujá, em seguida a manga e depois o jamelão de Santa Margarida.A menor foi a
acerola, uvaia e o cupuaçu.A goiaba que teve a maior quantidade de nistose, com
o valor de 1,10% e a uvaia foi a que apresentou menor quantidade de nistose com
0,08%. Para a sacarose o maracujá mostrou a maior quantidade com 9,61 % e a
menor foi a goiaba com 0,11%. Já a glicose foi o caju com o maior valor de
2,87%, a menor foi a acerola com 0,5809%,já a frutose tinha maior concentração,
no jamelão de Santa Margarida foi de 7,86% e a menor foi a acerola com 0,5809%,
já a frutose tinha maior concentração,no jamelão de Santa Margarida foi de
7,886% e a menor foi a acerola com 0,58%.
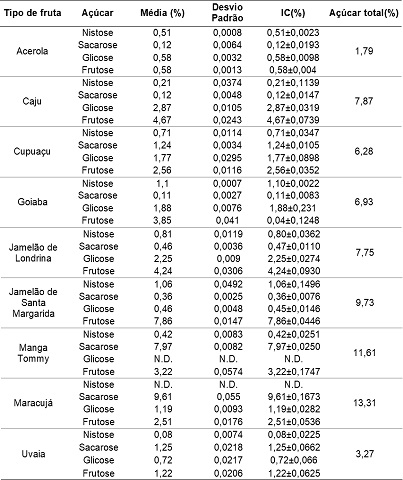
Relação do tipo de fruta com seus respectivos valores de média, desvio padrão,intervalo de confiança(IC) de cada tipo de açúcar e açúcar total.
Conclusões
Com os resultados cromatográficos foi possível identificar e quantificar a maioria dos açúcares das polpas de frutas assim determinou-se qual fruta tem a maior capacidade de produção de álcool, pois através de resultados obtidos da cromatografia sobre os açúcares totais, assim em ordem de maior para menor as melhores frutas para ser usada na fermentação são: maracujá com 13,38%, manga com 11,61%, jamelão de Santa Margarida com 9,73%, caju 7,87%, jamelão de Londrina com 7,75%, goiaba cupuaçu com 6,93%, uvaia com 3,27% e acerola com 1,79%.As amostras de origens distintas possuem diferentes concentrações de açúcares, sendo jamelão de Santa Margarida com 9,73% a maior e de Londrina com 7,75% a menor, ficando com 20,35% de diferença. Essa diferença foi por causa da disponibilidade dos recursos para a fotossíntese para a matriz das amostras.
Agradecimentos
Agradeço a Universidade Estadual de Londrina pelo apoio financeiro.
Referências
ANVISA - AGÊNCIA NACIONAL DE VIGILÂNCIA SANITÁRIA. Resolução n°899, 29 de maio de 2003. Brasília, p. 1- 15.
BERNARDES-SILVA, A. P. F.; LAJOLO, M.; CORDENUNSI, B. R. Evolução dos teores de amido e açúcares solúveis durante o desenvolvimento e amadurecimento de diferentes cultivares de manga. Ciênicia e tecnologia de alimentos, Campinas, v. 23, p. 116-120, dezembro, 2003.
BRASIL. Regulamento técnico geral para a fixação dos padrões de identidade e qualidade de sucos de frutas. Ministério da Agricultura, Pecuária e Abastecimento. Instrução normativa nº 01, 7 de janeiro 2000.
BRUICE, P. Química Orgânica. 4º. ed. São Paulo: Person, v. 2, 2006.
CIABOTTI, E. D.; BRAGA, M. E. D. Alterações das características físicos-químicas da polpa de maracujá amarelo submetido a diferentes tipos de congelamento inicial. Revista Brasileira de Produtos Agroindustriais, Campina Grande, v. 2, p. 51-60, 2000.
CIABOTTI, E. D.; BRAGA, M. E. D. Alterações das características físicos-químicas da polpa de maracujá amarelo submetido a diferentes tipos de congelamento inicial. Revista Brasileira de Produtos Agroindustriais, Campina Grande, v. 2, p. 51-60, 2000.
JADHAV, V. M.; KAMBLE, S. S.; KADAM, V. J. Herbal medicine : Syzygium cumini :A Review. Journal of Pharmacy Research, Mumbai, v. 2, n. 8, p. 1212-1219, August 2009.
KARWOWSKI , M. S. M. Estudo da estabilidade, comportamento reológico e dos compostos fenólicos de frutas da Mata Atlântica. Universidade Federal do Paraná. Curitiba. 2011.
LUCIANO, V. et al. Condições meteorológicas e tipo de solo na composição da uva 'Sauvignon'. Pesquisas agropecuárias brasileira, Brasília, v. 48, n. 1, p. 97-104, janeiro 2013.
MEDLICOTT A.P., THOMPSON A.K. Analysis of sugars and organic acids in ripening mango fruits (Mangifera indica L. var Keitt) by high performance liquid chromatography. Journal of the Science of Food and Agriculture 36:561-566, 1985.
MATOO, A.K.; et al Chemical changes during ripening and senescence. In: PANTASTICO, E.B. Post-harvest physiology, handling and utilization of tropical and subtropical fruits and vegetables. Connecticut: AVI, 1975. cap.7, p.272-283.
MINEROPAR. Carta geologica de Londrina. MINEROPAR, 2006. Disponivel em: <http://www.mineropar.pr.gov.br/arquivos/File/2_Geral/Geologia/PDF_Mapas_Geo_250000/Londrina.PDF>. Acesso em: 02 Dezembro 2015a.
MINEROPAR. Carta geologica de Presidente Prudente, 2006. Disponivel em: <http://www.mineropar.pr.gov.br/arquivos/File/2_Geral/Geologia/PDF_Mapas_Geo_250000/Presidente_Prudente.PDF>. Acesso em: 2 Dezembro 2015b.
MIYAZAWA , M. Compostos voláteis da uvaia (Eugenia pyriformis cambess). Universidade Estadua Paulista. São Paulo. 2009.
NELSON, D. L.; COX, M. M. Princípios de bioquímica de LEHNINGER. 5 °. ed. São Paulo: Artimed, 2011.
RIBANI, M. et al. Validação em métodos cromatográficos e eletroforéticos. Química Nova, v. 27, n. 8, p. 771-780, Junho 2004.
RIZZON, L. A.; BERNARDI, J.; MIELE, A. Características analíticas dos sucos de maça Gala, Golden delicious e Fuji. Ciência e tecnologia de alimentos, Campinas, v. 25, n. 4, p. 750-756, out-dez 2005.
ROCHA, R. H. C. et al. Uso do índice de degradação de amido na determinação da maturidade da manga 'TOMMY ATKINS'. Revista Brasileira de Fruticultura, Jaboticabal, v. 23, n. 2, p. 302-305, agosto 2001.
SILVA, M. R. D. et al. Estudo do comportamento reológico de polpas de caju (Anacardium occidentale, L.), acerola (Malpighia emarginata, D.C.) e manga (Mangifera indica, L.). Semina: Ciências Agrárias, Londrina, v. 33, p. 237-248, jan-mar 2012.
SKOOG, D. A.; HOLLER, F. J.; CROUCH, S. R. Princípios de Análise Instrumental. 6ª ed. ed. Porto Alegre: Bookman, 2009.











