SÍNTESE DA 2-AMINO-1,4-NAFTOQUINONA PELA REAÇÃO DE STAUDINGER
ISBN 978-85-85905-21-7
Área
Química Orgânica
Autores
dos Santos, H.J.C. (IFRJ) ; Silva, R.S.F. (IFRJ)
Resumo
A 2-amino-1,4-naftoquinona é um intermediário sintético empregado na preparação de vários produtos em Química Orgânica. Este trabalho apresenta um método alternativo de preparação desse intermediário por meio da reação de Staudinger.
Palavras chaves
Naftoquinonas; Reação de Staudinger; Trifenilfosfina
Introdução
A 2-amino-1,4-naftoquinona é um intermediário químico empregado na síntese de diversas quinonas bioativas. Entre as mais recentes está a N-(1,4-Dioxo-1,4- diidronaftalen-2-il)-benzamida que apresenta uma promissora atividade para o tratamento de doenças neurodegenerativas especialmente o mal de Parkinson (Josey et al 2013). A 2-amino-1,4-naftoquinona já foi preparada a partir do derivado 2-azido-1,4-naftoquinona, onde o grupo azida é reduzido por ácido clorídrico. Outra alternativa para a conversão do grupo azida em amina é a reação de Staudinger a qual empega trifenilfosfina em meio aquoso. O presente trabalho descreve um novo método de preparação da 2-amino-1,4-naftoquinona a partir do derivado azida pela reação de Staudinger.
Material e métodos
Preparação da 2-azido-1,4-naftoquinona: 237 mg (1 mmol) de 2-bromo- naftoquinona e 97 mg (1,5 mmol) de azida de sódio foram dissolvidos em acetona e submetidos a agitação magnética por 24 hs quando a acetona foi removida a pressão reduzida e o precipitado amarelo formado foi suspendido em água e filtrado a vácuo e lavado com água 3 vezes fornecendo o produto com 87 % de rendimento (174 mg). Preparação da 2-amido-1,4-naftoquinona: 150 mg (0,75 mmol) de 2-azido-1,4- naftoquinona foram dissolvidos em THF e então 294 mg (1.125 mmol) de trifenilfosfina foram adicionados a solução ocorrendo imediata liberação de N2. Após o termino da liberação de N2 (30 minutos) 10 ml de água foram adicionados à mistura ocorrendo à precipitação de um sólido amorfo marrom escuro. O THF foi evaporado a pressão reduzida e o sólido formado foi filtrado a vácuo e cromatografado em coluna de gel de sílica sendo eluído com uma mistura de Hexano-Acetato de etila 9:1 sendo isolado após evaporação do solvente como um sólido alaranjado em 62 % (80 mg). Preparação 2-amido-1,4-naftoquinona on pot: 237 mg (1 mmol) de 2-bromo- naftoquinona e 97 mg (1,5 mmol) de azida de sódio foram dissolvidos em THF e submetidos a agitação magnética por 24 hs quando 393 (1,5 mmol) de trifenilfosfina foram adicionados, após o termino da liberação de N2 (30 minutos) 10 ml de água foram adicionados à mistura ocorrendo à precipitação de um sólido amorfo marrom escuro. O THF foi evaporado a pressão reduzida e o sólido formado foi filtrado a vácuo e cromatografado em coluna de gel de sílica sendo eluído com uma mistura de Hexano-Acetato de etila 9:1 sendo isolado após evaporação do solvente como um sólido alaranjado em 30 % (52 mg).
Resultado e discussão
Inicialmente o preparo da 2-azido-1,4-naftoquinona foi realizado seguindo o
método descrito na literatura (Sakar et al. 2015) a partir da 2-bromo-1,4-
naftoquinona o que foi conseguido em 87% de rendimento. A 2-azido-1,4-
naftoquinona foi então submetida a redução pela reação de Staudinger
fornecendo em rapidamente a 2-amino-1,4-naftoquina em 61 % Esquema 1.
Baseado no sucesso inicial da primeira reação, foi tentada uma
preparação direta ''on pot'' a partir da 2-bromo-1,4-naftoquinona,
precursora da 2-azido-1,4-naftoquinona, para essa reação foi empregado THF
como solvente e o tempo de reação foi de 24 hs, Esquema 2. O método ''on
pot'' forneceu a 2-amino-1,4-naftoquinona em 30 % de rendimento, menor que o
rendimento global obtido em duas reações.
Um método já publicado na literatura de preparação da 2-amino-1,4-
naftoquinona envolve a hidrólise ácida da 2-azido-1,4-naftoquinona gerada in
situ pela reação da 1,4-naftoquinona e ácido hidrazoico (HN3) (Couladouros
et al 1997), embora o rendimento desse processo seja de alto rendimento, ele
não é muito seguro, visto que o ácido hidrazoico é exatamente tóxico e
explosivo. O método desenvolvido nesse trabalho apresenta menor rendimento,
entretanto uma vez que emprega menores quantidades de azida e é realizado em
meio neutro, não acarreta risco de explosão e toda azida não reagida é
convertida em nitrogênio gasoso, o principal subproduto da reação, o óxido
de trifenilfosfina apresenta baixa toxicidade, essas características tornam
o método mais seguro e menos agressivo para o meio ambiente.
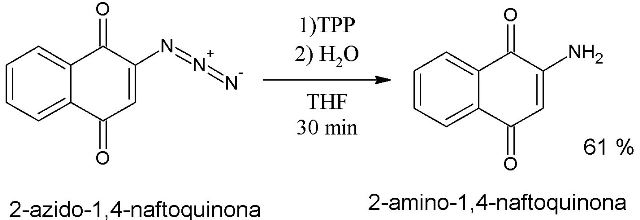
Síntese da 2-amino-1,4-naftoquinona pela reação de Staudinger.
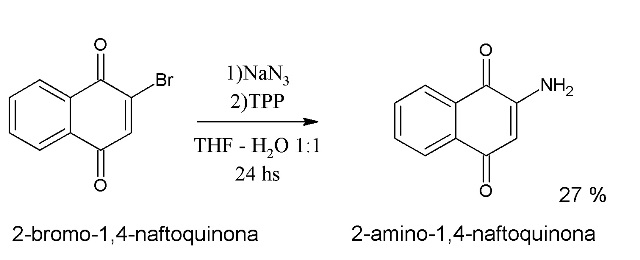
Síntese da 2-amino-1,4-naftoquinona on pot.
Conclusões
O trabalho apresenta um método eficiente e seguro para a preparação da 2- amino-1,4-naftoquinona. Estudos para melhora do rendimento estão em progresso.
Agradecimentos
IFRJ, CNPq e FAPERJ por auxílio financeiro. LAMAR-IPPN-UFRJ, nas pessoas de Maria do Carmo F. R. Pinto, Francisco de Assis D. dos Santos e Profª DrªLuzineide W. Tinoco
Referências
Couladouros, E. A.; Plyta, Z. F.; Haroutounian, S. A.; Papageorgiou, V. P.; Efficient Synthesis of Aminonaphthoquinones and Azidobenzohydroquinones: Mechanistic Considerations of the Reaction of Hydrazoic Acid with Quinones. An Overview. 1997, Journal of Organica Chemistry. v. 62, p. 6-10.
Josey, B. J.; Inks, E. S.; Wen, X.; Chou, C. J.; Structure−Activity Relationship Study of Vitamin K Derivatives Yields Highly Potent Neuroprotective Agents. 2013, Journal of Medicinal Chemistry, v. 56, p. 1007-1022.
Sarkar, S. K.; Sawai, A.; Kanahara, K.; Wentrup, C.; Abe, M.; Gudmundsdottir, A. D.; Direct Detection of a Triplet Vinylnitrene, 1,4-Naphthoquinone-2-ylnitrene, in Solution and Cryogenic Matrices. 2015. Journal of the American Chemical Society, v. 137, p. 4207-4214.
































