Síntese e Caracterização de Ferrocenilpirazóis com potencial atividade anticâncer
ISBN 978-85-85905-21-7
Área
Química Orgânica
Autores
Venturini Filho, E. (UNIVERSIDADE FEDERAL DO ESPÍRITO SANTO) ; Brito, A.F. (UNIVERSIDADE FEDERAL DO ESPÍRITO SANTO) ; Greco, S.J. (UNIVERSIDADE FEDERAL DO ESPÍRITO SANTO)
Resumo
A neoplasia maligna é apontada como uma das doenças mais temidas na população mundial, com 20 milhões de casos para 2025 sendo que no Brasil o biênio 2016- 2017 estima-se 600 mil novos casos. 1–3 E através dessa forma motriz, a síntese e avaliação de fármacos com potencial atividade biológica faz-se necessária. A partir da reação de uma ciclocondensação sob controle termodinâmico, semelhante à reação de Biginelli modificada por Atwal, foi possível, neste trabalho, sintetizar novos híbridos moleculares contendo os núcleos pirazóis e ferroceno ambos com potencial atividade anticâncer. A caracterização dessas moléculas foi feita por métodos espectroscópicos de infravermelho (IV) e Ressonância Magnética Nuclear (RMN).
Palavras chaves
Síntese de Heterociclos; Ferroceno; Pirazóis
Introdução
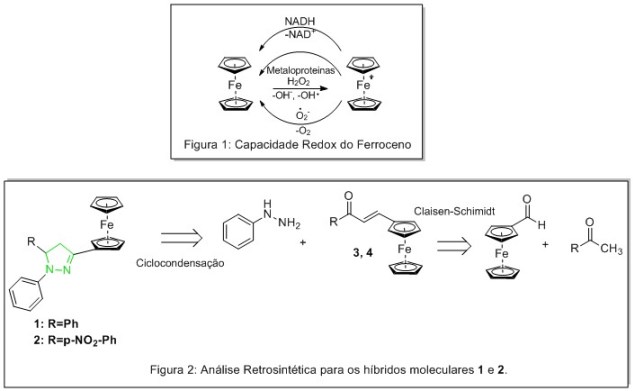
Uma das áreas de acelerado crescimento na química devido às amplas aplicações em produtos farmacêuticos, na agricultura e na indústria é a química dos heterociclos. 4–6 Os heteroátomos mais frequentes presentes nos anéis heterocíclicos são N, O e S. Essas estruturas são aplicadas em cosméticos, plásticos, eletrônica, óptica e ciências de materiais 7, porém, é no desenvolvimento de novos fármacos que se encontram um acervo considerável e promissor, colocando assim a química sintética como um dos melhores caminhos para obtenção e derivatização desses compostos possibilitando a síntese de intermediários e produtos de interesse. 8 Dentre os sistemas heterocíclicos o pirazol, um anel aromático simples de cinco membros contendo dois átomos de nitrogênio em posições adjacentes, tem alcançado popularidade considerável devido aos seus múltiplos usos. Seus derivados representam uma das classes mais ativas de compostos exibindo amplo espectro de atividades farmacológicas, tais como: antimicrobianos, anticonvulsivantes, anticâncer, analgésicos, anti-Inflamatório, entre outras. 9–11 Outro núcleo de promissora atividade biológica é o ferroceno, ou di-(η5- ciclopentadienil)ferro (II). Um composto organometálico neutro, estável, não tóxico e ainda permeável à membrana celular. O Fe (II) existe em equilíbrio com Fe (III) no meio celular sendo este equilíbrio determinado pelo potencial eletroquímico do par Fe2+/Fe3+. A reação redox entre os dois ocorre rápida e reversivelmente e necessita da contribuição de outro par redox biológico, doador/aceptor eletrobiológico. O ferroceno é biologicamente acessível à oxidação reagindo com peróxido de hidrogênio (H2O2), enquanto a redução do cátion ferricênio pode ser mediada por NADH, metaloproteínas ou espécies reativas de oxigênio (Fig. 1).
Material e métodos
As chalconas ferrocênica 3 e 4 foram sintetizadas via condensação clássica de Claisen-Schimidt enquanto que os híbridos moleculares 1 e 2 foram sintetizados através de uma reação de ciclocondensação entre as chalconas supracitadas e a fenil-hidrazina. O curso reacional foi acompanhado por cromatografia em camada fina (CCF), os compostos sintetizados tiveram seus pontos de fusão determinados e foram caracterizados por espectroscopia na região do infravermelho (IV) e espectroscopia de ressonância magnética nuclear (RMN) de 1H. A reação de preparação das chalconas ferrocênica 3 (com acetofenona) e 4 (com p-nitroacetofenona) foi realizada como descrito a seguir: em um balão de fundo redondo de 25 mL foram adicionados 1,5 mmol de NaOH, 4,0 mL de metanol, 1 mmol do ferrocenocarboxaldeído e 1 mmol da respectiva cetona. A mistura reacional foi mantida a temperatura ambiente e o controle do término da reação foi feito utilizando CCF. Com o final da reação foi vertido o conteúdo do balão em água destilada gelada e gelo e os sólidos formados laranja para 3 (P.f.= 131 ºC) e roxo para 4 (P.f.= 220 ºC), foram filtrados e lavados com água gelada. 12 Já para a síntese dos híbridos moleculares 1 e 2 foi utilizado um balão de fundo redondo de 25 mL onde adicionou-se 1,75 mmol de cloreto de fenil- hidrazina e 0,5 mmol das chalconas ferrocênica 3 e 4, respectivamente. Utilizou-se como solvente 10 mL de uma mistura etanol, água e ácido acético (5:1:3). A reação foi mantida sob agitação constante por 4 a 6h e sob refluxo. 13 Após o término da reação, monitorado por CCF, os sólidos formados, verde para 1 (P.f.= 114-115 ºC) e vermelha para 2 (P.f.= 164-165 ºC)foram filtrados e lavados abundantemente com água e etanol, ambos gelados, para em seguida ser recristalizado com etanol.
Resultado e discussão
Inicialmente sintetizou-se as chalconas 3 e 4 mediante reação de Claisen-
Schimidt, com rendimentos de 97% e 95%, respectivamente. Essas foram
utilizadas na síntese dos compostos 1 e 2, cujos rendimentos foram de 63% e
66%, respectivamente, e os produtos facilmente purificados (Fig. 2). Para
tal, empregou-se a reação de ciclocondensação em meio ácido sob controle
termodinâmico. A proposta mecanística para essa reação assemelha-se ao
mecanismo da reação de Biginelli modificada por Atwal, portanto, a reação
inicia-se pela adição conjugada da hidrazina à chalcona, seguida de
ciclização e subsequente desidratação, para formar o anel pirazólico (Fig.
3). 14
Os IV’s dos compostos 1 e 2 apresentaram as bandas características dos
grupos funcionais presentes nas moléculas alvo, como 1594/1592 cm-1,
atribuído ao ν(C=N) do anel pirazólico, 1492/1497 cm-1, ν(C=C) aromático,
814/819 cm-1 γ(C-H) e 740/746 cm-1 γ(C=C), atribuídas ao núcleo ferrocênico,
e em 2 uma banda em 1558 cm-1 do ν(NO2).
Ademais, nos espectros de RMN de 1H verificou-se os sinais característicos
do grupo ferrocenila, multipleto em 4.20 ppm (9H) para 1, e multipletos em
4.07, 4.10, 4.18 e 4.24 ppm, todos (1H) e 4.13 (5H) para 2. O composto 1
apresentou multipletos em 6.81 (1H) e 7.19 (4H) ppm, referentes ao anel N-
fenil que em 2 estão presentes em 6.88 (1H), 7.23 (3H) e 7.43 (1H) ppm. Os
multipletos em 7.36 (1H), 7.44 (2H) e 7.81 (2H) ppm atribuídos aos
hidrogênios aromáticos proveniente da acetofenona em 1, e da p-
nitroacetofenona para o híbrido 2 foram identificados os dubletos em 7.91
(2H) e 8.28 (2H) ppm. E por fim, nos compostos 1 e 2 os sinais em 3.74/3.79
e 5.06/5.20 ppm foram atribuídos aos hidrogênios metilênicos e metínicos do
anel pirazólico, respectivamente, que provam a formação do anel
diidropirazol.
Capacidade redox do Ferroceno e Análise retrosintética dos híbridos sintetizados.
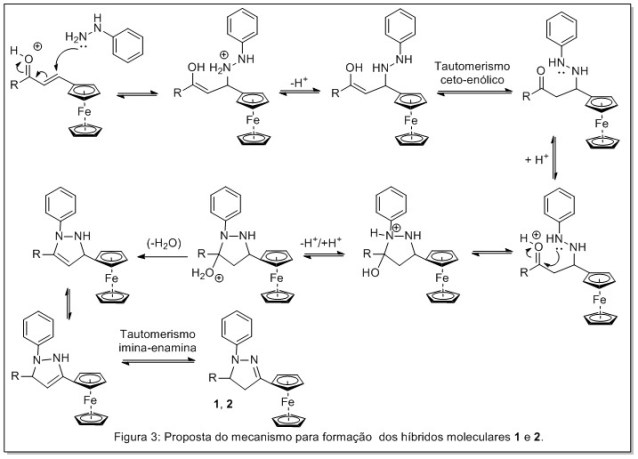
Proposta do mecanismo de ciclocondensação para formação dos ferrocenilpirazóis.
Conclusões
Através da metodologia escolhida para o preparo dos híbridos moleculares 1 e 2 com potencial atividade anticâncer foi possível sintetizar e isolar os compostos puros em bons rendimentos 63 e 66%, respectivamente. As moléculas alvo foram devidamente caracterizadas por IV e RMN 1H. Nesse último, foi atribuído os sinais do núcleo ferrocênico, dos hidrogênios aromáticos, e ainda foi comprovada a formação do diidropirazol.
Agradecimentos
Pela estrutura e apoio técnico agradecemos a UFES, ao Laboratório de Síntese orgânica e Medicinal (LSOA) e ao NCQP/DQUI. E aos órgãos de fomento CNPq e FAPES.
Referências
1. O que é o câncer? INCA. http://www2.inca.gov.br/wps/wcm/connect/cancer/site/oquee 2–3 (2017).
2. Bednarz, H., Shaw, A., West, S. & Nair, D. R. The Biology of cancer. http://sphweb.bumc.bu.edu/otlt/mph-modules/ph/ph709_cancer/ph709_cancer_print.html (2016). Available at: http://www.news-medical.net/health/Cancer-History.aspx.
3. Estimativa 2016: incidência de câncer no Brasi. Inst. Nac. Câncer José Alencar Gomes da Silva. Coord. Prevenção e Vigilância (2015).
4. Jain, K. S., Chitre, T. S., Miniyar, P. B., Kathiravan, M. K. & Bendre, V. S. Biological and medicinal significance of pyrimidines. Curr. Sci. 90, 793–803 (2006).
5. Taha, M. et al. Molecular hybridization conceded exceptionally potent quinolinyl- oxadiazole hybrids through phenyl linked thiosemicarbazide antileishmanial scaffolds : In silico validation and SAR studies. Bioorg. Chem. 71, 192–200 (2017).
6. Karthikeyan, C., Solomon, V. R., Lee, H. & Trivedi, P. Design, synthesis and biological evaluation of some isatin-linked chalcones as novel anti-breast cancer agents: A molecular hybridization approach. Biomed. Prev. Nutr. 3, 325–330 (2013).
7. Valverde, M. G. & Torroba, T. Sulfur-Nitrogen Heterocycles. Molecules 10, 318–320 (2005).
8. ScienceDirect. Pesquisa com as palavras ‘Bioactive heterocycles’ no portal de periódicos ScienceDirect. May http://www.sciencedirect.com (2017).
9. Khan, M. F. et al. The therapeutic voyage of pyrazole and its analogs : A review. Eur. J. Med. Chem. 120, 170–201 (2016).
10. Küçükgüzel, S. G. & Senkardes, S. Recent advances in bioactive pyrazoles. Eur. J. Med. Chem. 97, 786–815 (2015).
11. Li, M. & Zhao, B. Progress of the synthesis of condensed pyrazole derivatives ( from 2010 to mid-2013 ). Eur. J. Med. Chem. 85, 311–340 (2014).
12. Suwito, H., Novi Kristanti, A. & Nyoman Tri Puspaningsih, N. Chalcones: Synthesis, structure diversity and pharmacological aspects. J. Chem. Pharm. Res. 6, 1076–1088 (2014).
13. Li, P. & Liu, Z. Ferrocenyl-contained dendritic-like antioxidants with dihydropyrazole and pyrazole as the core : investigations into the role of ferrocenyl group and structure e activity relationship on scavenging radical and protecting DNA. Tetrahedron 69, 9898–9905 (2013).
14. Zsoldos-mády, V. et al. Ferrocenyl pyrazolines : Preparation , structure , redox properties and DFT study on regioselective ring-closure. J. Organomet. Chem. 694, 4185–4195 (2009).
































