Utilização de Célula de Cavidade para a síntese de Sulfonas Vinílicas
ISBN 978-85-85905-21-7
Área
Química Orgânica
Autores
Vicente, D.A. (UFPE) ; Pessoa, D.G. (UFPE) ; Navarro, M. (UFPE) ; Menezes, P.H. (UFPE)
Resumo
Será descrito um novo método para obtenção de sulfonas vinílicas, sem a utilização de solventes, através da descarboxilação eletroquímica em célula de cavidade do ácido cinâmico em eletrodo de grafite. Para o desenvolvimento do método foram utilizados como substratos o ácido cinâmico e p-toluilsulfinato de sódio, eletrodo de grafite sendo variado a solução eletrolítica, proporção entre substratos e corrente em milampére (mA). O melhor resultado foi encontrado quando utilizado uma solução eletrolítica de perclorato de lítio em H2O, proporção entre os substratos de 1:1 e corrente de 20mA. Após a extração do produto o mesmo foi análisado no CG-MS e foi constatado a taxa de conversão de 85,72%.
Palavras chaves
Vinil-Sulfonas; Cela de cavidade; descarboxilação
Introdução
A química verde é baseada em princípios que visam: diminuir a quantidade de resíduos, economia de átomos, utilização de solvente seguros ao meio ambiente, dentre outros (Anastas e Eghbali, 2009). Frente a esses princípios, a utilização da célula de cavidade surge como alternativa para o desenvolvimento de métodos eletroquímicos utilizando quantidades mínimas do solvente empregado na reação, utilização de solução aquosa como eletrólito, geração ínfima de resíduos. O emprego desse tipo de célula foi descrito primeiramente por Areias e colaboradores que em seu trabalho relataram o funcionamento da célula para a reação de Reformatsky (Areias et al., 2008). As sulfonas apresentam importância na química medicinal por sua atuação como inibidores de alguns processos enzimáticos e em química orgânica pela sua utilização em diversos tipos de reações (Meadows e Gervay-Hague, 2006). É destacado então, as vinil-sulfonas, que também possui capacidade de inibir processos enzimáticos e podem ser obtidas através de reação com oleofinas, via reagente organometálicos, métodos eletroquímicos, etc.(Meadows e Gervay- Hague, 2006; Qian et al., 2016; Roush e Palkowitz, 1987). Destacado a importância dessa classe de compostos, esse trabalho tem como objetivo descrever um novo método eletroquímico empregando célula de cavidade para obter as vinil-sulfonas em condições baseadas em alguns princípios da química verde.
Material e métodos
As eletrólises foram realizadas com uma fonte DC, utilizando-se eletrólitos de NaCl, LiClO4 e nBu4ClO4 em uma mistura de CH3CN:H2O, experimentos realizados em duas correntes diferentes (20mA e 40mA) em uma célula de cavidade não dividida que possui três eletrodos. O eletrodo de trabalho é formado por grafite em pó (150mg), ácido cinâmico (0,5mmol) e p-toluil sulfinato de sódio (0,5mmol) homogeneizados e prensados sob peso de 1,90 Kg cm-2 durante 10 minutos acima de um bastão de grafite (d= 13mm), que serviu como contato elétrico, o bastão de grafite é inserido em uma tampa de Teflon® de modo a formar uma cavidade (h= 2.0±0.2mm, d= 13mm). Um disco de papel filtro foi utilizado acima do eletrodo de trabalho. Em seguida, a tampa de Teflon® foi conectada à célula de vidro e foram adicionados 15mL de solução 0,1mol L-1 de solução de eletrólito. O eletrodo de referência e o eletrodo auxiliar foram adicionados à célula. Após o término da reação (1,1F mol-1 ou 2,2F mol-1), foi extraída a vinil-sulfona do eletrodo de trabalho. A extração foi realizada com o auxílio de um extrator de vidro, sendo ele conectado a tampa de Teflon®. Ao eletrodo de trabalho foi adicionado acetato de etila (2x 2,5mL) sendo a mistura formada separada por filtração simples. O filtrado foi lavado (3x 3mL) com solução saturada de cloreto de amônio (NH4Cl). A fase orgânica foi separa com o auxílio de um funil de bromo, seca sob MgSO4 anidro e filtrada. O filtrado foi análisado em GC-MS para obter a taxa de conversão do produto de interesse.
Resultado e discussão
No método desenvolvido foi empregado a célula de cavidade (FIGURA 1) para
promover a reação de descarboxilação eletroquímica visando a obtenção de uma
metodologia verde (Anastas e Eghbali, 2009; Areias et al., 2008). Sendo
variado: solução eletrolítica, proporção dos reagentes e corrente elétrica.
A quantidade do eletrodo de trabalho (pó de grafite) foi determinado no
trabalho de Areias e colaboradores (Areias et al., 2008). Os resultados da
variação dos parâmetros estão mostrados na (TABELA 1).
Quando utilizado solução eletrolítica de (nBu4ClO4) em sistema bifásico e
proporção entre os reagentes de (1:2) foi observado a formação do produto de
interesse e de um subproduto (ensaio 1) logo essa proporção entre os
reagentes foi alterada para (1:1) e foi observado a formação do produto de
interesse, ausência de subproduto, mas a taxa de conversão foi de 55,03% em
corrente de 20 mA (ensaio 2). A fim de otimizar a taxa de conversão
encontrada, foi realizado o (ensaio 3) e constatou-se a formação apenas do
produto de interesse quando a proporção entre os reagentes foi de (1:1) em
corrente de 20mA com taxa de conversão de 85,72% em solução eletrolítica de
(LiClO4) em água. Quando utilizado solução eletrolítica de (NaCl) foi
constatado a formação apenas do produto de interesse em corrente de 20 mA
com uma taxa de conversão de 36,37% (ensaio 4) e quando a corrente foi
alterada para 40 mA (ensaio 5) foi observado a formação tanto do produto de
interesse como de subproduto. Quando utilizado cinamato de sódio (ensaio 6)
devido à diminuição do potencial de oxidação da reação de descarboxilação
frente ao ácido correspondente foi encontrado uma taxa de conversão de
61,02% levando então a estabelecer as condições do (ensaio 2) como as ideais
para a obtenção da vinil-sulfona.
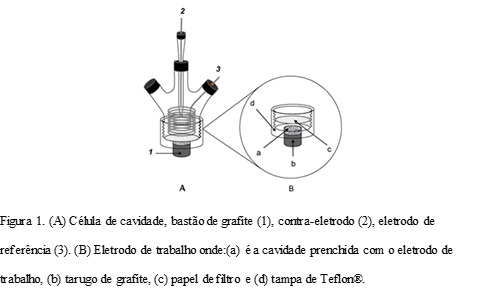
célula de cavidade
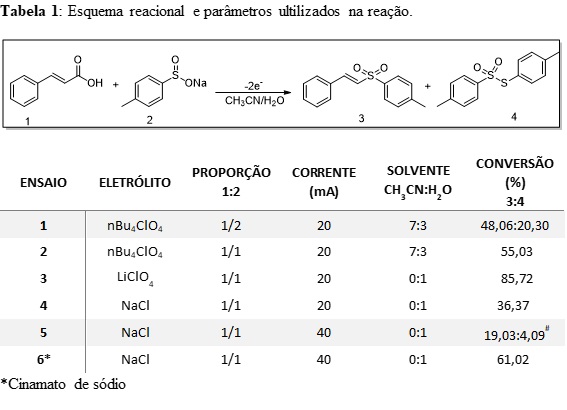
esquema reacional e parâmetros utilizados na reação.
Conclusões
A célula de cavidade levou a formação da vinil sulfona com conversão de 85,72% quando utilizado as condições descritas no ensaio dois mostrando ser um método eficiente. A otimização da reação levou a uma condição que atende a preceitos da química verde, tais como: ausência de solvente na reação, emprego de eletrólito não nocivo (utilização de água), economia de átomos na oxidação, evitando o uso de agentes oxidantes.
Agradecimentos
Ao CNPq, CAPES e FACEPE pelo apoio financeiro.
Referências
ANASTAS, P.; EGHBALI, N. Green Chemistry: Principles and Practice. p. 301–312, 2009.
AREIAS, M. C. C. et al. A novel electrosynthesis cell with a compressed graphite powder cathode and minimal organic solvent content: Application to the Reformatsky reaction. Electrochimica Acta, v. 53, n. 22, p. 6477–6483, 2008.
MEADOWS, D. C.; GERVAY-HAGUE, J. Vinyl sulfones: Synthetic preparations and medicinal chemistry applications. Medicinal Research Reviews, v. 26, n. 6, p. 793–814, 2006.
QIAN, P. et al. Electrosynthesis of (E)-Vinyl Sulfones Directly from Cinnamic Acids and Sodium Sulfinates via Decarboxylative Sulfono Functionalization. Journal of Organic Chemistry, v. 81, n. 11, p. 4876–4882, 2016.
ROUSH, W.; PALKOWITZ, A. Application of tartrate ester modified allylic boronates in organic synthesis: an efficient, highly stereoselective synthesis of the carbon(19)-carbon(29) segment of rifamycin S. Journal of the American Chemical …, v. 109, p. 953–955, 1987.
































