FILMES A BASE DE QUITOSANA/POLI (VINIL ÁLCOOL)/ NANOPARTÍCULAS DE COBRE: UM POTENCIAL CATALISADOR PARA REDUÇÃO DE NITRO COMPOSTOS
ISBN 978-85-85905-21-7
Área
Materiais
Autores
Ferreira de Souza, J. (UFPEL) ; Fajardo, A.R. (UFPEL)
Resumo
Neste estudo, nanopartículas de cobre (CuNPs) foram sintetizadas e estabilizadas em um filme de quitosana/poli(álcool vinílico) (QT/PVA) usando um protocolo simples sob condições brandas. O desempenho catalítico dos filmes de QT/PVA-NPsCu foi testado na reação de redução do nitrobenzeno (NB) à anilina (AN). Nossos resultados revelam que os filmes QT/PVA-NPsCu catalisaram a reação de forma eficiente e também diminuíram a sua energia de ativação (Ea) quando comparada com reações realizadas com outros catalisadores metálicos. A eficiência catalítica dos filmes de QT/PVA-NPsCu foi mantida mesmo após 6 ciclos consecutivos de uso. Este conjunto de resultados classificam este novo sistema como um proeminente catalisador na redução de compostos nitro aromáticos em aminas aromáticas.
Palavras chaves
Nanopartículas metálica; Quitosana; Catálise
Introdução
Nanopartículas metálicas (NPM) são atualmente o foco principal de muitas pesquisas reportadas na literatura, uma vez que essas possuem interessantes propriedades como, por exemplo, alta atividade e seletividade catalítica. Além dessa alta performance catalítica, a superfície das NPM oferece a flexibilidade de recuperação da estrutura após a adsorção em uma reação catalítica (CHEN, 2014). O cobre (Cu) é um metal de transição que vem sendo muito utilizado em catálise por ser altamente condutor. As nanopartículas de cobre (NPsCu) como todo material com dimensões nanométricas têm uma grande área de superfície em razão do seu volume o que faz ressaltar suas propriedades catalíticas. Sabe-se que o cobre desempenha papel catalisador fundamental em diversas reações orgânicas como, por exemplo, reações de cicloadiação de Huisgen, que consistem em uma reação entre uma azida e um alcino terminal para formar um triazol, e também reações de Ullmann, consiste em uma reação de acoplamento entre halogenetos de arila e cobre (NADOR, 2013; OKUYAMA, 2000). Dentre outras reações em que o cobre é utilizado como catalisadores encontram-se reações de hidrogenação, redução, oxidação e hidroxilação. No entanto, vale mencionar que as aplicações catalíticas envolvendo NPM suspensas são limitadas, já que ao longo do tempo as nanopartículas (NPs) dispersas em fase líquida tendem a se aglomerar para reduzir a alta energia livre de superfície (CHEN, 2014). As forças atrativas entre as NPs (por exemplo, forças de van der Waals), fazem com que átomos e moléculas neutras se atraiam e sejam atraídos por cargas elétricas devido a energia das forças dipolo-dipolo que estão sempre presentes. Esse fenômeno acaba acarretando em uma diminuição na atividade catalítica e muitas vezes na seletividade das NPs (ZHANGA, 2013). Uma forma de resolver esse problema é imobilizar essas NPs em um suporte sólido, contudo muitos fatores devem ser levados em consideração na escolha desse suporte, tendo em vista que a atividade catalítica pode ser afetada se a interação entre as NPs e o agente estabilizador for muito forte. Por outro lado, uma fraca interação entre as NPs e o agente estabilizador pode acarretar uma falha no processo de estabilização, resultando assim na aglomeração indesejada das mesmas (ZHANGA, 2013). Sabe-se que o alto peso molecular dos polímeros pode controlar a aglomeração indesejada de NPs, potencializando assim suas propriedades catalíticas. No entanto, muitas características devem ser levadas em consideração na escolha do polímero como, por exemplo, grupos funcionais presente na cadeia polimérica e resistência a diferentes ambientes. Derivada de resíduos da indústria da pesca, a quitina é um polímero natural que vem despertando um grande interesse comercial e tecnológico. A quitosana (QT) é obtida pela reação de desacetilação da quitina em meio alcalino (KUMAR, 2000). Grupos hidroxilas (-HO) estão presentes na estrutura geral desse biopolímero, além da presença de grupos amino (-NH2) (OKUYAMA, 2000). Embora insolúvel em água, é possível solubilizá-la em soluções aquosas de ácidos orgânicos, tais como ácido acético, fórmico e cítrico, e também em ácidos inorgânicos diluídos como ácido clorídrico, nítrico e perclórico, devido à protonação dos grupos amino (MAYER, 1998). A solubilidade da QT está intimamente relacionada com a quantidade de grupos amino protonados (- NH3+) em sua cadeia polimérica. Quanto maior a quantidade deste grupo, maior o número de interações eletrostáticas repulsivas entre as cadeias e também maior a solvatação em água (OKUYAMA, 2000). Considerando as propriedades condutoras das NPsCu e as propriedades de complexação desse polímero com Cu+2, a QT mostra-se uma ótima escolha para imobilização de NPsCu (RHAZI, 2002.). Embora sejam largamente empregados, esses sistemas poliméricos ainda precisam ser aperfeiçoados para se obter uma efetiva aplicabilidade e potencializar as propriedades físico-químicas. Com o objetivo de melhorar as propriedades mecânicas e variar a taxa de degradação deste polissacarídeo, é interessante se utilizar uma mistura de QT com outros polímeros sintéticos, tal como o poli (vinil álcool) (PVA). O PVA, um polímero sintético, possui excelente resistência química, à tração, compressão e abrasão, e estas propriedades associadas à sua boa estabilidade química, resultam em um vasto campo de aplicação tais como bioadesivo, material de bandagem, molde para enxerto de pele, filmes, géis, cápsulas ou microcápsulas (GALEMBECK, 1996). Frente à problemática de utilização de catalisadores metálicos, foi desenvolvida uma metodologia para a obtenção de um nanomaterial de catálise de fácil recuperação e reutilizável. Neste trabalho relatamos um procedimento de síntese simples para se obter NPsCu estabilizadas em uma matriz polimérica a base de QT/PVA. Dessa forma esperamos demonstrar que o sistema QT/PVA-NPsCu poderá apresentar potencial aplicação como sistema catalítico em diferentes reações químicas.
Material e métodos
Preparação dos Filmes de QT/PVA: Primeiramente foi preparada uma solução com 0,5 g QT (Mv 87 KDa, 15% desacetilação) a qual foi solubilizada em uma solução aquosa de ácido acético a 1% (v/v), sob agitação magnética a temperatura ambiente por 12 h. Uma segunda solução foi preparada contendo 1 g de PVA (Mw 124 KDa, 99% hidrolisado) que foi solubilizado em água, sob agitação magnética por 12 h, a temperatura de 80 ºC. As soluções de QT e PVA foram homogeneizadas e mantidas sob agitação por 1 h a temperatura ambiente. Em seguida, foram adicionados 80 μL de glutaraldeído (solução aquosa 25% v/v) à solução de QT/PVA, o qual atua como agente de reticulação. A solução foi então vertida em uma placa de Petri e seca em estufa à 37 ºC por 48 h para completa evaporação do solvente. Após a secagem do solvente, o filme foi removido da placa de Petri e purificado em água destilada. Síntese das NPsCu: Os filmes obtidos foram cortados em fragmentos com uma área média de 1 cm2. Posteriormente, esses foram submersos em uma solução de CuCl2.2H2O (0,2 M) a temperatura ambiente por 3 h. A quantidade de íons Cu2+ absorvidos pelas amostras de filme foi quantificada pela técnica de espectroscopia de absorção atômica de chama (FAAS). Os filmes contendo os íons Cu2+ (denotados como QT/PVA-Cu2+) foram imersos em uma solução contendo NaBH4 (0,6 M) por 3 h para que houvesse a redução dos íons (Cu2+) presentes nos filmes para Cu0. Os filmes de QT/PVA contendo cobre na sua forma reduzida foram denotados como QT/PVA-NPsCu. Os filmes QT/PVA, QT/PVA-Cu2+ e QT/PVA-NPsCu foram caracterizados por espectroscopia na região do infravermelho (FTIR), difração de raios-X (DRX) e análises termogravimétricas (TGA). Também foram avaliadas outras propriedades como, por exemplo, capacidade de absorção de água e resistência a diferentes solventes. A morfologia e a distribuição das NPs no interior da matriz QT/PVA foi investigada por microscopia eletrônica de transmissão (MET). Avaliação da atividade catalítica: Uma amostra do filme QT/PVA-NPsCu (100 mg) foi adicionada em um erlenmeyer contendo 5 mL de uma solução aquosa de nitrobenzeno (NB) 5 mM e 1 mL de solução de NaBH4 (50 mM). O sistema reacional foi mantido estático e a temperatura ambiente. A redução do NB a anilina (AN) foi monitorada utilizando um espectrofotômetro UV-Vis operando na faixa de 200 a 400 nm. A cinética de redução foi investigada por meio de medidas da intensidade na absorção do NB em λ = 270 nm. Deve ser mencionado que foi construída previamente uma curva de calibração da absorbância do NB em função da sua concentração (R2 > 0,999).
Resultado e discussão
A técnica de FT-IR foi utilizada para identificar a natureza química dos
filmes e dos seus materiais precursores. Como pode ser observado na Figura
1a. Em comparação com as amostras de filmes de QT/PVA, QT/PVA-Cu2+ e QT/PVA-
NPsCu, é possível observar as bandas em 3440cm-1, 3453cm-1 e 3471cm-1
respectivamente, as quais estão associadas ao estiramento axial dos grupos
amino (-NH2) e/ou hidroxila (-OH). Estes resultados sugerem a interação
entre os íons de cobre e os grupos -NH2 e -OH disponíveis dentro da matriz
QT.
É possível observar também o aparecimento da banda em 1095cm-1 referente às
ligações glicosídicas -C-O-C-. Também foram observadas bandas
características da QT em 1658cm-1 no filme QT/PVA e 1633 cm-1 para as
amostras de filme QT/PVA-NPsCu (C=O em grupo amida). O alongamento na banda
de 1455cm-1 que corresponde a ligação C-N.
As bandas em 1382cm-1 e 1375 cm-1, para os filmes QT/PVA e filmes QT/PVA-
NPsCu, respectivamente correspondem ao -CH3 ligado ao grupo -NH2. Isso
significa que o processo de formação das NPsCu envolve interação com os
grupos -NH2 da QT.
Padrões de DRX de difração de QT, PVA, e dos filmes QT/PVA, QT/PVA-Cu2+ e
QT/PVA-NPsCu são mostrados na Figura 1b.
Nos padrões de DRX foram observados picos de difração em 2θ igual a 19,5º e
40,6° que são designados pelos planos de reflexão respectivamente em (101) e
(220) que corresponde a estrutura semicristalina do PVA, que resulta em
ligações de hidrogênio entre as cadeias de PVA.
O padrão de DRX para os filmes QT/PVA e os QT/PVA-Cu2+ foram idênticos o que
permite concluir que a absorção de íons de Cu2+ não altera a estrutura dos
filmes. Já para os filmes QT/PVA-NPsCu há o aparecimento de dois novos
picos de difração em 2θ igual a 43,6º e 50,7º, com planos de reflexão em
(111) e (200), correspondente a estrutura cristalina cubica de face centrada
(CFC) do Cu0. Isto confirma que as NPsCu foram sintetizadas com sucesso
dentro da matriz de QT.
As propriedades térmicas dos filmes QT/PVA, QT/PVA-Cu2+ e QT/PVA-NPsCu foram
investigados por TGA (Figura 1c). Tal como observado para todas as amostras,
a primeira perda de massa ocorre na faixa de temperatura de 75-125 ºC. Esta
perda de peso é devida à vaporização da umidade e compostos voláteis. A
termogravimetria dos filmes exibiu quatro estágios de perda de massa, o
primeiro em 262°C é atribuído a eliminação de grupos OH secundários de PVA,
enquanto o segundo (a 299 ºC) e o terceiro (a 353 ºC) são atribuídos à
decomposição térmica das porções lineares de QT reticulada. A última etapa
em cerca de 430 ºC, é devido a degradação de polieno espinha dorsal de PVA.
Em contraste com os filmes QT/PVA, os filmes QT/PVA-Cu2+ e QT/PVA-NPsCu
exibiram termogramas com degradação térmica entre 200 e 300 ºC, o que sugere
a incorporação de espécies Cu2+/Cu0 dentro dos filmes diminui a sua
estabilidade térmica. Estes dados estão de acordo com outros estudos que
evidenciaram uma diminuição da temperatura de degradação de sistemas
poliméricos que contêm espécies de cobre, em comparação com amostras sem
adição de cobre. Isso se dá devido à natureza catalítica deste que diminui a
energia de ativação e aumenta a reação de despolimerização.
De acordo com o termograma dos filmes QT/PVA, o resíduo em 500 °C foi de
31,2%, enquanto que o resíduo de filme QT/PVA-NPsCu foi de 34,8%. Estes
resultados sugerem que NPsCu foram aprisionados dentro da matriz QT.
Os resultados dos ensaios de SD em função do tempo podem ser observados na
Figura 1d. As amostras foram intumescidas em água destilada, ambas
apresentaram um ritmo rápido inchaço pouco antes de sua imersão em água.
Além disso, os filmes QT/PVA e os filmes QT/PVA-NPsCu alcançaram máximo
inchaço em 60 min. Conforme o tempo passa, ambas as curvas inchaço tendem a
se estabilizar.
Apesar das amostras apresentarem comportamento semelhante, as NPsCu têm um
efeito claro sobre a capacidade de dilatação. O filme puro mostrou um SD a
cerca de 210%, o que pode ser atribuído à característica hidrofílica dos
polímeros usados. Por outro lado, a presença das NPsCu diminui a capacidade
de inchamento da matriz. Como referido acima, NPsCu aumentam a densidade de
reticulação dentro da matriz de QT devido à complexação de Cu0 com os grupos
funcionais de QT e PVA. Esta lacuna reduz a disponibilidade de grupos
funcionais para interagir com as moléculas de água. Além disso, os pontos de
reticulação adicionais conferem rigidez à matriz polimérica, que evitam o
influxo do líquido para dentro da massa do filme.
Imagens obtidas por MET (Figura 2 a,b) sugerem que as NPsCu apresentam
morfologia esférica e estas são distribuídas uniformemente pela matriz
QT/PVA. O diâmetro das partículas varia de 1 a 5 nm, o que sugere que o
protocolo utilizado é bastante eficiente. Além disso, não foi observada
agregação das partículas, o que confirma que a matriz QT/PVA atua de modo
efetivo na estabilização das NPsCu. A boa dispersão das partículas no filme
pode aumentar a eficiência desse dispositivo como catalisador.
Através dos espectros de UV-Vis, realizados para verificar a taxa de
conversão de NB para AN, fica evidente a ação catalítica do filme QT/PVA-
NPsCu, uma vez que é feita a comparação reacional sem o filme (Figura 2c) e
com o filme QT/PVA-NPsCu (Figura 2d). É possível observar na Figura 2c a
banda em 270 nm, característica do NB. No entanto, após uma hora de reação é
quase que imperceptível a formação da banda característica da AN em 230 nm,
já no espectro da Figura 2d é possível observar que com a presença do
catalisador de filme QT/PVA-NPsCu, após apenas cinco minutos de reação há a
formação da banda característica da AN, onde a mesma se intensifica no
decorrer do tempo reacional. Também foram realizados teste de reutilização
do catalisador, onde foi possível observar que o catalisador tem um
potencial de aplicação para no mínimo 6 ciclos reacionais com uma taxa de
conversão de NB de em média 85%.
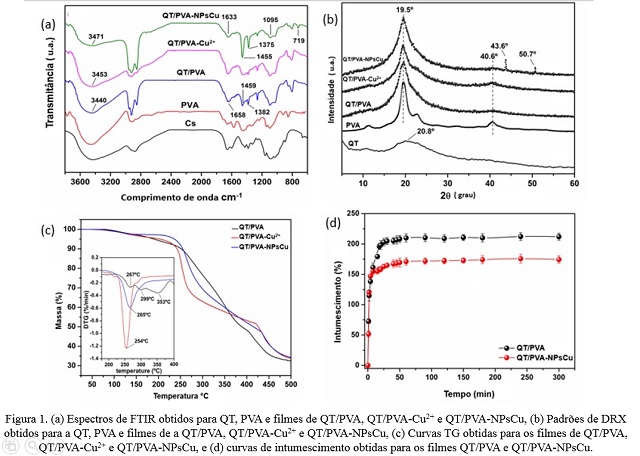
(a) Espectros de FTIR, (b) Padrões de DRX, (c) Curvas TG obtidas para os filmes e (d) curvas de intumescimento obtidas para os filmes.
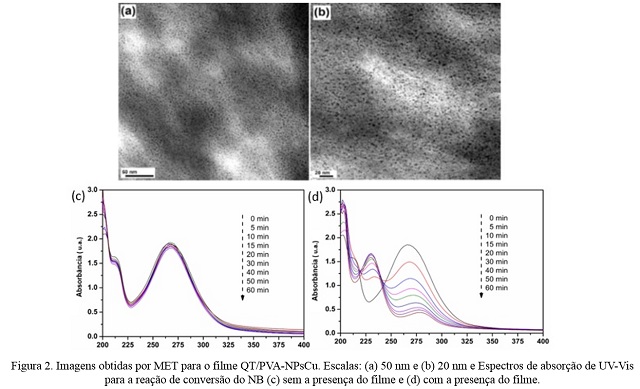
Imagens obtidas por MET. Escalas: (a) 50 nm e (b) 20 nm e Espectros de absorção de UV-Vis (c) sem a presença do filme e (d) com a presença do filme.
Conclusões
A partir dos resultados encontrados neste estudo, pode-se concluir que a metodologia desenvolvida foi eficiente para o preparo de NPsCu, onde foi possível observar com o DRX a formação da fase única, cristalina atribuída a elas. Os picos estreitos e intensos vistos sugerem que o material possui boa cristalinidade e alta pureza. Nas análises de FTIR verificou-se que a incorporação de NPsCu nos filmes não influência significativamente o espectro. Na análise de TGA, a incorporação de NPsCu foi comprovada com o aumento da massa residual. A morfologia dos filmes apenas apresentou-se lisa, compacta e sem poros. O método otimizado para a preparação das NPsCu mostrou-se fácil, eficiente, e com elevada reprodutibilidade. Os filmes obtidos apresentaram propriedades satisfatórias para a aplicação desejada e são bastante promissores como catalisadores em reações de redução de compostos nitro aromáticos.
Agradecimentos
Os autores agradecem a FAPERGS pela bolsa de iniciação científica de J.F.S. e ao CNPq pelo suporte financeiro (Chamada Universal - Processo 441888/2014-3).
Referências
CHEN, B.; LI, F.; HUANG, Z.; LU, T.; YUAN,T. Stability or Flexibility: Metal Nanoparticles Supported over Cross-linked Functional Polymers as Catalytic Active Sites for Hydrogenation and Carbonylation, Applied Catalysis A, General , 2014.
GALEMBECK, E. Propriedades físico-químicas e interação com membranas biológicas dos surfactantes não iônicos da série Renex (nonilfenoletoxilado). Dissertação de Mestrado, Instituto de Biologia, Universidade Estadual de Campinas, 1996.
KUMAR, M. N. R. A review of chitin and chitosan applications. Reactive & Functional Polymers, v. 46, p. 1–27, 2000.
MAYER, A. B. R. Formation of noble metal nanoparticles within a polymeric matrix: nanoparticle features and overall morphologies. Materials Science and Engineering C, v.6, p. 155-166, 1998.
NADOR, F.; VOLPE, M. A.; ALONSO, F.; FELDHOFF, A.; KIRSCHNING, A.; RADIVOY, G. Copper nanoparticles supported on silica coated maghemite as versatile, magnetically recoverable and reusable catalyst for alkyne coupling and cycloaddition reactions. Applied Catalysis A: General, v.455, p.39-45, 2013.
OKUYAMA K., NOGUCHI K., KANENARI M, EGAWA T., OSAWA K., OGAWA K. Structural diversity of chitosan and its complexes. Carbohydrate Polymers, v.41, p. 237–247, 2000.
RHAZI, M.; DESBRUÈRES, J.; TOLAIMATE, A.; RINAUDO, M.; VOTTERO, P.; ALAGUI, A. Contribution to the study of the complexation of copper by chitosan and oligomer. Polymer, v. 43, p. 1267-1276, 2002.
ZHANGA. Y.; QUEKA, X.; WUA, L.; GUANA,Y.; HENSENA,E. Palladium nanoparticles entrapped in polymeric ionic liquid microgels as recyclable hydrogenation catalysts. Journal of Molecular Catalysis A: Chemical, p 53 –58, 2013.
































