Projeto, construção e avaliação de um sistema de adsorção por variação de pressão
ISBN 978-85-85905-21-7
Área
Ambiental
Autores
Manera, C. (UNIVERSIDADE DE CAXIAS DO SUL) ; Perondi, D. (UNIVERSIDADE FEDERAL DO RIO GRANDE DO SUL) ; Junges, J. (UNIVERSIDADE FEDERAL DO RIO GRANDE DO SUL) ; Godinho, M. (UNIVERSIDADE DE CAXIAS DO SUL)
Resumo
O biogás é uma mistura gasosa produzida pela digestão anaeróbia da matéria orgânica que pode ser utilizada como combustível após a remoção do dióxido de carbono. No presente trabalho, um sistema PSA foi desenvolvido visando o refino de biogás. As colunas de adsorção foram dimensionadas baseadas em uma revisão da literatura de sistemas PSA utilizados por diversos autores em conjunto a dois modelos matemáticos teóricos. Testes para análise da curva de ruptura foram conduzidos a 8 bar e vazão de 1 NL/min de uma mistura sintética equimolar CO2/CH4. O tempo de ruptura observado experimentalmente foi de 1,5 min, sendo alcançada a concentração máxima de metano de 73,1 %. Os resultados obtidos neste trabalho indicam a possibilidade de separação de biogás no sistema estudado.
Palavras chaves
dióxido de carbono; adsorção; PSA
Introdução
O gás natural (GN) é um combustível fóssil composto basicamente por metano (75-95%) que é utilizado no Brasil como fonte de energia para indústrias, residências e meios de transporte (TIPPAYAWONG; THANOMPONGCHART, 2010). Outro exemplo de sua aplicação é em usinas termelétricas, que complementam as necessidades energéticas do país. Além das aplicações supracitadas, o GN é utilizado como matéria prima na produção de ureia, amônia, metanol e hidrogênio (SILVA, 2009). A produção nacional de gás natural em 2017 até o mês de maio foi de cerca de 105,04 milhões de m³/dia e as importações alcançaram 20,15 m³/dia neste mesmo período (BRASIL, 2017). O biogás produzido por digestão anaeróbia é um recurso renovável e uma alternativa ao uso de combustíveis fósseis como o gás natural. O biogás é composto basicamente por metano (50-75%) e dióxido de carbono (25-45%) podendo ainda, conter baixas concentrações de amônia, sulfeto de hidrogênio, hidrogênio, nitrogênio, oxigênio e monóxido de carbono (SUN et al., 2015). O dióxido de carbono, um dos constituintes presentes em elevadas concentrações, é inerte em termos de combustão não apresentando poder calorífico. Portanto, a sua presença diminui o teor energético do biogás devido à diluição do metano (TIPPAYAWONG; THANOMPONGCHART, 2010). Desta forma, para que sua aplicação industrial seja viável há a necessidade de remoção de parte do CO2, de forma a diminuir a densidade da mistura e aumentar a concentração de CH4, proporcionando o incremento do poder calorífico do gás natural. Os métodos disponíveis atualmente para purificação e/ou separação do biogás são: separação por membranas, purificação criogênica, tratamento com aminas, lavagem com água pressurizada e sistema de adsorção por variação de pressão (Pressure Swing Adsorption - PSA) (RAVINA; GENON, 2015). Dentre os métodos citados destaca-se o PSA, que possui baixa demanda energética e vem sendo amplamente estudado em escala piloto. A técnica de purificação do biogás por PSA é baseada na adsorção preferencial do CO2 em um material poroso sob alta pressão. Quando a pressão é reduzida o gás adsorvido é recuperado e o adsorvente pode ser reutilizado para o próximo ciclo de adsorção (SIRIWARDANE et al., 2001). Para atingir a separação, o sistema utiliza a diferença de afinidade entre um adsorvente e os compostos de uma mistura gasosa. O primeiro ciclo PSA foi desenvolvido por Charles W. Skarstrom para desidratação e separação do ar em correntes enriquecidas com nitrogênio e oxigênio (SKARSTROM, 1960). O ciclo Skarstrom pode ser considerado como um modelo simplificado de PSA, sendo operado em 4 etapas: (1) adsorção, (2) despressurização, (3) purga e (4) pressurização. De acordo com Grande et al. (2013), os adsorventes mais utilizados em sistemas PSA são a zeólita e o carvão ativado. As zeólitas foram descobertas em 1756, pelo mineralogista sueco Baron Axel Frederick Consted. Entre os diversos tipos de zeólitas, a mais conhecida é a zeólita 13X, com íons sódio na estrutura principal formando aberturas de 0,8 nm (ROUSSEAU, 1987), sendo esta uma referência para processos de purificação de CO2. O projeto de um sistema PSA, sem o prévio conhecimento de dados experimentais provenientes de um protótipo ainda não é viável, devido à complexidade das interações gás-sólido (SIRCAR, 2002). O dimensionamento de uma coluna de adsorção deve ser realizado considerando a influência da razão entre o comprimento e o diâmetro (L/D). Razões elevadas favorecem o aumento do coeficiente de transferência de massa, enquanto razões menores minimizam a perda de carga na coluna (KNAEBEL, 1995). Conforme Kovacevic (2000), o diâmetro do leito deve ser, no mínimo, entre 20 e 30 vezes maior que o diâmetro das partículas do adsorvente para evitar o efeito de parede no escoamento. De acordo com Choi et al. (2003) os parâmetros mais importantes para avaliação do processo são pureza das correntes de saída, recuperação dos componentes e produtividade. Abordagens analíticas para um sistema PSA de 4 etapas foram desenvolvidas por Kayser e Knaebel (1989) e Suh e Wankat (1989), em estudos independentes. Os modelos matemáticos, baseados em isotermas de adsorção não lineares, foram construídos com algumas considerações como: resistência à transferência de massa negligenciável, dispersão axial negligenciável, operação isotérmica, comportamento de gás ideal e perda de carga desprezível. Em ambos os estudos foram propostas equações para o cálculo da velocidade da curva de ruptura e recuperação do produto. Este trabalho tem por objetivo o dimensionamento e construção de um sistema PSA de escala laboratorial de duas colunas para separação de uma mistura equimolar CO2/CH4. As colunas foram dimensionadas baseadas em uma revisão da literatura de sistemas PSA utilizados por diversos autores e avaliadas por meio de um ensaio de curva de ruptura.
Material e métodos
O dimensionamento das colunas de adsorção foi baseado em uma série de 15 referências estudadas. A partir dos experimentos de separação por PSA realizados por estes autores foi construído um gráfico da razão do comprimento pelo diâmetro das colunas (L/D) em função do número de Reynolds da partícula para os escoamentos. De acordo com o gráfico foi definido um ponto médio de operação da coluna de adsorção em determinado L/D e número de Reynolds. A vazão de operação da coluna foi definida em 1,0 NL/min de uma mistura de biogás sintético (CO2-50%mol/mol e CH4-50%mol/mol) e por meio da equação do número de Reynolds foram então calculados a velocidade superficial, e por consequência, o diâmetro da coluna. O número de Reynolds (Re) pode ser definido como uma quantidade adimensional utilizada para prever padrões de fluxo. O referido é amplamente utilizado em cálculos de dimensionamento, com o intuito de garantir a semelhança dinâmica entre diferentes escoamentos. De acordo com Knaebel (1995), o número de Reynolds típico obtido em processos de adsorção encontra-se no intervalo entre 10 - 40. A definição do comprimento da coluna foi realizada com base no diâmetro da coluna calculado e a razão L/D observada no gráfico construído com os dados experimentais de diversos autores. Os tempos de ciclo foram calculados a partir da relação entre o comprimento da coluna e velocidade da curva de ruptura na coluna de adsorção. Esta velocidade foi obtida através de dois modelos matemáticos analíticos, propostos por Kayser e Knaebel (1989) e Suh e Wankat (1989). A zeólita 13X HP (Celta Brasil Ltda.) utilizada como adsorvente foi caracterizada por adsorção em nitrogênio líquido a -196,15 °C, em um analisador da marca Quantachrome Instruments e modelo Nova 1200e. Os dados de equilíbrio de adsorção dos gases CO2 e CH4 na zeólita 13X foram obtidos a partir dos experimentos realizados por Park et al. (2016). Os autores realizaram ensaios de adsorção de CO2 e CH4 em zeólita 13X e determinaram os parâmetros da isoterma de Langmuir para a adsorção. A determinação experimental do tempo de ciclo foi realizada por meio da observação da curva de ruptura do sistema em uma das colunas dimensionadas. O adsorvente utilizado para os ensaios foi regenerado em um forno aquecido a 400 °C durante 8 horas para remoção de possíveis impurezas adsorvidas. A mistura gasosa foi obtida a partir de um cilindro com dióxido de carbono (50%) e metano (50%), simulando uma corrente de biogás. Foram simuladas vazões na corrente de alimentação de 1,0 NL/min e pressão absoluta de 8,93 bar. Durante os ensaios, amostras da corrente purificada foram coletadas em intervalos de tempo pré- estabelecidos. As coletas foram realizadas em traps e a concentração dos gases foi obtida por meio de cromatografia gasosa em um equipamento da marca Dani Instruments, modelo Master GC, provido de detector por condutividade térmica (TCD).
Resultado e discussão
O gráfico construído com os dados de separações PSA de diversos autores
pesquisados está apresentado na Figura 1a. Por meio do gráfico
observa-se que a operação das colunas de adsorção de 8 dos 15 trabalhos
estudados localiza-se em uma faixa estreita de valores de Re,
delimitadas no gráfico por duas linhas tracejadas nos valores de 4 e 18.
Utilizando um valor de Re de 11, intermediário a esta faixa, foi
calculada uma velocidade superficial do escoamento de 0,0173 m/s. Após o
cálculo da velocidade, o diâmetro da coluna foi calculado em 0,0122
m. Visto isso foi optado por um diâmetro de 0,0127 m (1/2 in), diâmetro de
tubo comercial que mais se aproxima do valor calculado. O valor de
Re para este tubo foi calculado em 10,2, valor este que ainda se encontra na
faixa central das linhas tracejadas da Figura 1a. A determinação
do comprimento das colunas foi realizada com base em uma média dos valores
de L/D dos 8 trabalhos localizados na faixa de Re selecionada. Com
o valor médio de L/D de 34,2 e o diâmetro de 0,0127 m foi calculado o
comprimento de cada coluna em 0,44 m. Ambas as colunas foram construídas
com 0,47 m, considerando um pequeno comprimento adicional (3 cm) de
segurança. O sistema construído é apresentado pela Figura 2. O sistema foi
projetado com duas colunas (C01 e C02) fabricadas em aço carbono. Em um
ensaio de separação PSA o fluxo de gás no sistema é controlado por 3
válvulas solenoides de 3 vias (V02, V03 e V04) acionadas automaticamente por
3 temporizadores. O gás é alimentado em uma das colunas, enquanto
ocorre a despressurização e purga na outra. A Figura 2 apresenta na cor
preta o volume de controle do sistema responsável pela purificação em
elevadas pressões e na cor cinza, o volume de controle onde ocorre a
despressurização do sistema. Após determinado tempo de ciclo, as válvulas
são automaticamente acionadas e as etapas que acontecem em cada coluna são
invertidas, o que permite um processo contínuo de separação da
mistura gasosa. As velocidades da curva de ruptura calculadas por meio dos
modelos propostos por Kayser e Knaebel (1989) e Suh e Wankat (1989)
foram de 0,00075 m/s e 0,00077 m/s, respectivamente. Considerando o
comprimento da coluna de 0,47 m os tempos de ciclo foram estimados em 10,4
e 10,2 min, respectivamente. Os valores obtidos para o tempo de ruptura
entre os dois métodos apresentaram uma diferença percentual de apenas
2%. A isoterma de adsorção de N2 na zeólita 13X apresentou um
comportamento do tipo I, característica de materiais microporosos.
Após o valor de P/P0 de 0,9 foi observada uma inclinação positiva
da isoterma, relacionada ao tipo IV, indicando a presença de
mesoporos e macroporos no material. A estrutura meso-macroporosa pode estar
relacionada ao processo de conformação mecânica do material em
grânulos utilizando um agente ligante. Os poros de maior tamanho, também
chamados de poros de alimentação ou transporte, tem a função de
conduzir as moléculas de adsorbato até os microporos do material. A zeólita
apresentou área superficial (BET) de 516 m²/g. Na análise de
distribuição de tamanhos de poros foi observado que grande parte do volume
dos poros está concentrado em um intervalo de 0,8 a 1,0 nm. O valor
total de poros obtido foi de 0,35 cm³/g, coerente com o observado por outros
autores como Choi et al. (2003) e Kacem, Pellerano e Delebarre
(2015) que obtiveram 0,40 e 0,43 cm³/g. A investigação do tempo de ciclo
mais adequado para os ciclos PSA foi realizada utilizando apenas uma
coluna preenchida com 48,3 g de zeólita 13X. A verificação foi conduzida ao
longo de 10,5 min (630 s) para avaliar as variações nas
concentrações dos gases e observar o comportamento da curva de ruptura ao
longo do tempo de ruptura previsto por meio dos modelos teóricos. A
variação na concentração dos gases para a vazão de 1,0 NL/min e pressão
absoluta de 8,93 bar é apresentada pela Figura 1b. Por meio da Figura
1b é possível observar que a concentração volumétrica de CH4
atinge um valor máximo de 73,1% no intervalo de tempo de 45 a 60 s.
Além disso, também é possível observar que não é obtida a concentração
máxima de CH4 nos instantes iniciais de operação, que
caracteriza um comportamento atípico de uma coluna de adsorção. O
comportamento típico de uma curva de ruptura com formato em S foi obtido por
diversos autores (GRANDE et al., 2013; KHUNPOLGRANG et al., 2015; KIM et
al., 2006; LESTINSKY et al., 2015; NA et al., 2001). Esta diferença
entre o comportamento inicial da curva de ruptura obtido pelos autores
citados em comparação ao presente trabalho pode ser atribuída à forma
de pressurização da coluna. Neste trabalho o controle da vazão no sistema
(válvula V06) foi posicionado na corrente purificada, na saída do
sistema. Desta maneira a coluna e as tubulações foram pressurizadas até a
pressão de operação com a própria mistura
CO2/CH4 sem nenhum controle de vazão. Durante esta
etapa a mistura é inserida com uma vazão muito alta no interior da
coluna até a total pressurização do sistema. Esta condição ocasiona uma
velocidade superficial muito elevada no interior da coluna,
dificultando a separação da mistura. Quando a pressão de operação é atingida
a vazão de entrada passa a ser controlada no valor pré-
estabelecido de 1,0 NL/min e a separação da mistura passa a ocorrer de
maneira mais eficiente, purgando a tubulação localizada após a coluna e
ocasionando o aumento da concentração volumétrica de CH4 até o
valor de 73,1%. Schell et al. (2013) observaram um comportamento
semelhante de aumento na concentração do composto menos adsorvido
(H2) nos instantes iniciais da etapa de adsorção em ciclos PSA.
Os autores atribuíram o comportamento ao vazamento seletivo de H2
nas tubulações da corrente purificada no intervalo entre os
ciclos. Com o objetivo de evitar este comportamento da curva de ruptura, que
diminui a pureza final do produto, Khunpolgrang et al. (2015)
utilizaram a pressurização inicial da coluna com o produto, sendo que o
volume de produto utilizado na pressurização é recuperado na corrente
purificada. De outra forma, Grande et al. (2013) utilizaram He na
pressurização do sistema, evitando assim a presença do composto mais
adsorvido na corrente purificada. Ainda, Kim et al. (2006), Lestinsky et al.
(2015) e Na et al. (2001) utilizaram uma pressurização do sistema
com vazão controlada, contribuindo assim para a manutenção de uma velocidade
superficial também controlada e a separação da mistura nos
instantes iniciais de operação. A curva de ruptura obtida no experimento
apresentou um formato extenso, indicando um comprimento elevado da
zona de transferência de massa. De acordo com Kovacevic (2000), uma estreita
zona de transferência de massa é desejável para que o adsorvente
seja utilizado de maneira mais eficiente. O comportamento da curva de
ruptura depende da taxa de transferência de massa, vazão de alimentação
e o formato da curva de equilíbrio de adsorção (ROUSSEAU, 1987). Segundo
Knaebel (1995), o formato dilatado da curva de ruptura pode ser
superado com o aumento do comprimento da coluna ou com o aumento no tempo de
ciclo causado pela diminuição da vazão de alimentação.
Entretanto, as medidas propostas acarretam na diminuição da produtividade do
processo. A divergência entre o tempo de ruptura obtido por meio
dos modelos teóricos (10,2 - 10,4 min) e o resultado obtido
experimentalmente (1,5 min) pode ser atribuída ao formado estendido da curva
de
ruptura e também às diversas considerações assumidas pelos autores no
desenvolvimento dos modelos matemáticos. Entre as considerações, as que
mais atribuem imprecisão aos modelos são: a operação isotérmica, resistência
à transferência de massa negligenciável e produto constituído
pelo componente menos adsorvido puro.
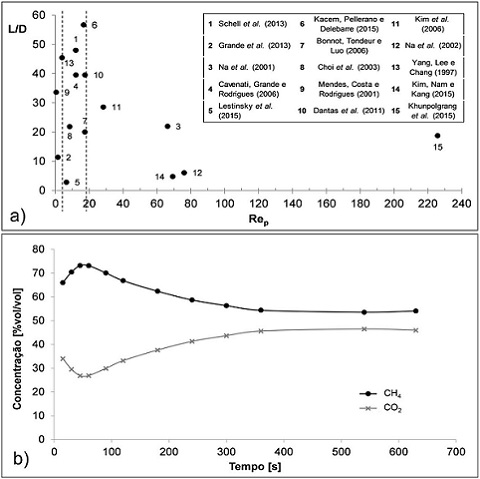
(a) Gráfico da razão entre o comprimento e o diâmetro das colunas de adsorção em função de Re e (b) concentrações de CH4 e CO2 no teste de adsorção
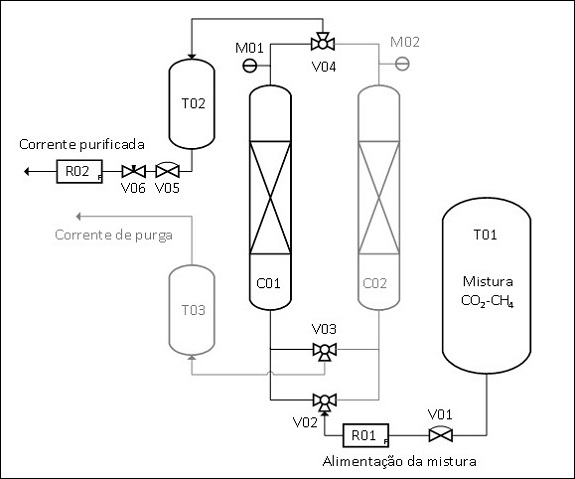
Desenho esquemático do sistema PSA construído
Conclusões
Com base em uma revisão de parâmetros de separações PSA de vários autores foi possível estabelecer faixas para os principais parâmetros de operação. A partir destes intervalos foi possível dimensionar as colunas de adsorção de um sistema PSA. A análise da área superficial do adsorvente utilizado, zeólita 13X, indicou isoterma com comportamento tipo I, característica de materiais microporosos. A análise da distribuição do tamanho de poros apresentou uma maior concentração dos mesmos na região próxima a 0,9 nm, justificando sua utilização como adsorvente para separação de misturas gasosas. A partir dos resultados obtidos para o tempo de ruptura por meio de dois modelos teóricos pode-se concluir que os modelos apresentam respostas semelhantes, entretanto, não podem ser utilizados para a descrição do sistema construído. A imprecisão dos modelos é atribuída às diversas considerações realizadas na elaboração do modelo, muitas delas não atendidas pelo sistema estudado. O tempo de ruptura obtido experimentalmente foi de 1,5 min. Os resultados obtidos neste trabalho indicam a possibilidade de separação de biogás no sistema construído. No entanto, tornam-se necessários experimentos complementares para definição de parâmetros de operação que melhorem a eficiência de separação.
Agradecimentos
Os autores agradecem o Laboratório de Energia e Bioprocessos da Universidade de Caxias do Sul e a Companhia Estadual de Distribuição de Energia Elétrica (CEEE-D).
Referências
BONNOT, K.; TONDEUR, D.; LUO, L. A. Effects of composition, temperature and purge on the performance of the cyclic adsorption of CO2 and CH4 on activated carbon. Chemical Engineering Research and Design, v. 84, n. 3, p. 192-208, 2006.
BRASIL. Associação Nacional do Petróleo, Gás Natural e Biocombustíveis. Dados estatísticos da produção nacional de gás natural. Disponível em: <http://www.anp.gov.br/wwwanp/dados-estatisticos>. Acesso em: 28 julho 2017.
CAVENATI, S.; GRANDE, C. A.; RODRIGUES, A. E. Removal of carbon dioxide from natural gas by vacuum pressure swing adsorption. Energy and Fuels, v. 20, n. 6, p. 2648-2659, 2006.
CHOI, W. K.; KWON, T. I.; YEO, Y. K.; LEE, H.; SONG, H. K.; NA, B. K. Optimal operation of the pressure swing adsorption (PSA) process for CO2 recovery. Korean Journal of Chemical Engineering, v. 20, n. 4, p. 617-623, 2003.
DANTAS, T. L. P.; LUNA, F. M. T.; SILVA JR, I. J.; TORRES, A. E. B.; DE AZEVEDO, D. C. S.; RODRIGUES, A. E.; MOREIRA, R. F. P. M. Carbon dioxide–nitrogen separation through pressure swing adsorption. Chemical Engineering Journal, v. 172, n. 2-3, p. 698-704, 2011.
GRANDE, C. A.; BLOM, R.; MÖLLER, A.; MÖLLMER, J. High-pressure separation of CH4/CO2 using activated carbon. Chemical Engineering Science, v. 89, p. 10-20, 2013.
KACEM, M.; PELLERANO, M.; DELEBARRE, A. Pressure swing adsorption for CO2/N2 and CO2/CH4 separation: Comparison between activated carbons and zeolites performances. Fuel Processing Technology, v. 138, p. 271-283, 2015.
KAYSER, J. C.; KNAEBEL, K. S. Pressure swing adsorption: Development of an equilibrium theory for binary gas mixtures with nonlinear isotherms. Chemical Engineering Science, v. 44, n. 1, p. 1-8, 1989.
KHUNPOLGRANG, J.; YOSANTEA, S.; KONGNOO, A.; PHALAKORNKULE, C. Alternative PSA process cycle with combined vacuum regeneration and nitrogen purging for CH4/CO2 separation. Fuel, v. 140, p. 171-177, 2015.
KIM, M. B.; BAE, Y. S.; CHOI, D. K.; LEE, C. H. Kinetic separation of landfill gas by a two-bed pressure swing adsorption process packed with carbon molecular sieve: nonisothermal operation. Industrial and Engineering Chemistry Research, v. 45, n. 14, p. 5050-5058, 2006.
KIM, Y. J.; NAM, Y. S.; KANG, Y. T. Study on a numerical model and PSA (pressure swing adsorption) process experiment for CH4/CO2 separation from biogas. Energy, v. 91, p. 732-741, 2015.
KNAEBEL, K. S. A how to guide for adsorber design. Adsorption Research Inc., p. 1-27, 1995.
KOVACEVIC, S. B. Screening adsorbents for a layered adsorbent bed for hydrogen separation using breakthrough experiments. 2000. 123 f. Thesis (Master of Applied Science) - University of British Columbia, Department of Chemical Engineering, Vancouver, 2000.
LESTINSKY, P.; VECER, M.; NAVRATIL, P.; STEHLIK, P. The removal of CO2 from biogas using a laboratory PSA unit: Design using breakthrough curves. Clean Technologies and Environmental Policy, v. 17, n. 5, p. 1281-1289, 2015.
MENDES, A. M. M.; COSTA, C. A. V.; RODRIGUES, A. E. Oxygen separation from air by PSA: Modelling and experimental results - Part I: Isothermal operation. Separation and Purification Technology, v. 24, n. 1-2, p. 173-188, 2001.
NA, B. K.; KOO, K.-K.; EUM, H.-M.; LEE, H.; SONG, H. CO2 recovery from flue gas by PSA process using activated carbon. Korean Journal of Chemical Engineering, v. 18, n. 2, p. 220-227, 2001.
NA, B. K.; LEE, H.; KOO, K. K.; SONG, H. K. Effect of rinse and recycle methods on the pressure swing adsorption process to recover CO2 from power plant flue gas using activated carbon. Industrial and Engineering Chemistry Research, v. 41, n. 22, p. 5498-5503, 2002.
PARK, Y.; JU, Y.; PARK, D.; LEE, C.-H. Adsorption equilibria and kinetics of six pure gases on pelletized zeolite 13X up to 1.0 MPa: CO2, CO, N2, CH4, Ar and H2. Chemical Engineering Journal, v. 292, p. 348-365, 2016.
RAVINA, M.; GENON, G. Global and local emissions of a biogas plant considering the production of biomethane as an alternative end-use solution. Journal of Cleaner Production, v. 102, p. 115-126, 2015.
ROUSSEAU, R. W. Handbook of separation process technology. New York: John Wiley and Sons, 1987. 1010 p.
SCHELL, J.; CASAS, N.; MARX, D.; MAZZOTTI, M. Precombustion CO2 capture by pressure swing adsorption (PSA): Comparison of laboratory PSA experiments and simulations. Industrial and Engineering Chemistry Research, v. 52, n. 24, p. 8311-8322, 2013.
SILVA, C. A. B. V. Limpeza e purificação de biogás. 2009. 91 f. Dissertação (Mestrado em Engenharia Mecânica) - Universidade de Trás-os-Montes e Alto Douro, Departamento de Engenharias, Vila Real, 2009.
SIRCAR, S. Pressure swing adsorption. Industrial and Engineering Chemistry Research, v. 41, n. 6, p. 1389-1392, 2002.
SIRIWARDANE, R. V.; SHEN, M.-S.; FISHER, E. P.; POSTON, J. A. Adsorption of CO2 on molecular sieves and activated carbon. Energy and Fuels, v. 15, n. 2, p. 279-284, 2001.
SKARSTROM, C. W. Method and apparatus for fractionating gaseous mixtures by adsorption. US. Patent 2.944.627. 1960.
SUH, S. S.; WANKAT, P. C. Pressure swing adsorption process for binary gas separation with Langmuir isotherms. Chemical Engineering Science, v. 44, n. 10, p. 2407-2410, 1989.
SUN, Q.; LI, H.; YAN, J.; LIU, L.; YU, Z.; YU, X. Selection of appropriate biogas upgrading technology-a review of biogas cleaning, upgrading and utilisation. Renewable and Sustainable Energy Reviews, v. 51, p. 521-532, 2015.
TIPPAYAWONG, N.; THANOMPONGCHART, P. Biogas quality upgrade by simultaneous removal of CO2 and H2S in a packed column reactor. Energy, v. 35, n. 12, p. 4531-4535, 2010.
































