Otimização do método organossolve etanol para extração da lignina do bagaço de cana-de-açúcar
ISBN 978-85-85905-21-7
Área
Química Verde
Autores
Magalhães, C.A.P.M. (IBILCE/UNESP) ; Fertonani, I.A.P. (IBILCE/UNESP) ; Damaceno, A.J. (IBILCE/UNESP) ; Quinelato, C. (UFSCAR) ; Fertonani, F.L. (IBILCE/UNESP) ; Lima, L.P. (IBILCE/UNESP) ; Abra, L.M. (IBILCE/UNESP)
Resumo
Para esse estudo utilizou o método Organossolv-Etanol variando a concentração de etanol (40%, 50% e 60%) para verificar a melhor proporção de etanol na extração de lignina do bagaço de cana-de-açúcar. A caracterização das ligninas extraídas foi feita pela técnica da espectrometria de infravermelho (FTIR), com intuito de analisar as possíveis diferenças na estrutura da lignina em relação à porcentagem de etanol adicionado. Esse estudo poderá contribuir para o uso desta lignina nas biorrefinarias.
Palavras chaves
caracterização; lignina; bagaço de cana-de-açúcar
Introdução
Os desafios de atender as necessidades do desenvolvimento humano e, ao mesmo tempo, à possibilidade de escassez das reservas de petróleo, principal matriz energética mundial e aos efeitos negativos ao meio ambiente, como a emissão de gases causadores do efeito estufa, aumenta a preocupação com a preservação ambiental e a busca de fontes alternativas de combustíveis que sejam renováveis e sustentáveis. Dentre elas se destaca a cana-de-açúcar, que é largamente utilizada no Brasil pela indústria sulcroalcooleira, devido ao seu grande potencial de produção de combustíveis (etanol) iniciada com Programa Pró-Alcool em 1975. Atualmente a indústria passou a ser chamada de sulcroenergética devido à produção de energia elétrica a partir da queima do bagaço e palha da cana-de-açúcar. No futuro, as biorrefinarias poderão ser acopladas as usinas, tendo como uma das matérias-primas a lignina para a produção de diversos compostos químicos: Adesivos, Fenóis, Vanilina, Dimetil Sulfito, Benzeno, entre outros1. Sendo assim, o objetivo deste trabalho é modificar o método organossolve utilizando etanol a fim de obter o melhor rendimento na extração da lignina do bagaço de cana-de-açúcar e efetuar a caracterização da lignina extraída.
Material e métodos
O bagaço de cana-de-açúcar passou por um pré-tratamento pelo método do digestor (CTC, 2005) para a remoção dos açúcares (sólidos solúveis) e abertura das fibras. Após essa etapa o bagaço foi submetido à remoção da lignina utilizando o método Organossolve-etanol, que consiste em aquecer 12 g de bagaço com uma solução de 120 ml de etanol (40%, 50% e 60%), por meio do uso de um reator de Paar, cujos parâmetros foram 190º C/ 90 minutos. O reator foi resfriado em temperatura ambiente e a mistura foi transferida para um béquer. Para a solubilização da lignina adicionou-se NaOH 0,1 mol L-1 a 60º C sob agitação mecânica por 10 minutos. Na sequência a mistura foi filtrada para a obtenção do licor negro. Adicionou-se no filtrado H2SO4 diluído até pH 3,0 e mantido em banho Maria por 45 minutos a 65º C para a precipitação da lignina. Logo após a mistura foi centrifugada (rotação de 10 mil rpm / 40 minutos / 20º C) e lavada com água destilada a temperatura de 12º C para a retirada de sulfato até o desaparecimento da espuma.
Resultado e discussão
Os ensaios foram realizados em triplicatas, partindo de mesma massa (36,01
g) do bagaço de cana-de-açúcar, obtendo assim, a maior porcentagem de
extração para a solução etanólica a 50% tendo como média 8,0 %. As demais
proporções apresentadas tiveram resultados semelhantes 60% etanol – 3,4 % de
lignina e 40% etanol – 3,8 %.
Durante a adição de ácido sulfúrico no licor negro, a amostra mudou a
coloração passando a ser marrom e viscoso.
No processo de aquecimento realizado no banho-Maria cuja a temperatura era
de 65º C, notou-se a formação de pequenos flocos de lignina, conforme o
tempo esses flocos aumentaram de tamanho e decantaram pela ação da
gravidade.
Pode-se observar também que a porcentagem de etanol - 40% teve menor
velocidade na decantação da lignina após a adição do ácido sulfúrico e uma
rápida velocidade de decantação da lignina no etanol - 50%.
Os resultados de infravermelho demostraram que a lignina extraída com maior
porcentagem de etanol apresentou bandas mais intensas para as regiões de
2842 – 3000 (estiramento C-H em grupos metílicos e metilênicos); 1709 - 1738
(stiramento C=O em cetonas não conjugadas, carbonilas e grupos éster); 1682
(estiramento C=O - não conjugado); 1593 - 1605 (vibrações no esqueleto
aromático influenciada por estiramento C=O); 1500 - 1515 (vibrações do
esqueleto aromático); 1457 – 1470 (deformações assimétricas C-H em C-H3 e C-
H2-); 1422 – 1430 (vibrações do esqueleto aromático combinados com
deformação C-H no plano); 1327 (C-O de anel siringil); 1221 – 1230
(estiramento C-C, C-O, C=O); 1166 (estiramento C=O em grupos éster
conjugados); 1030 – 1035 (deformação no plano de C-H aromático, deformação
C-O em álcoois primários, influenciada por estiramento C=O não conjugado);
817 – 832 (deformação de C-H fora do plano nas posições 2, 5 e 6 de unidade
G).
Os gráficos de infravermelho de lignina para as porcentagens de etanol (40%
e 50%) ficaram com bandas menos intensos devido a menor quantidade de etanol
utilizada no processo.
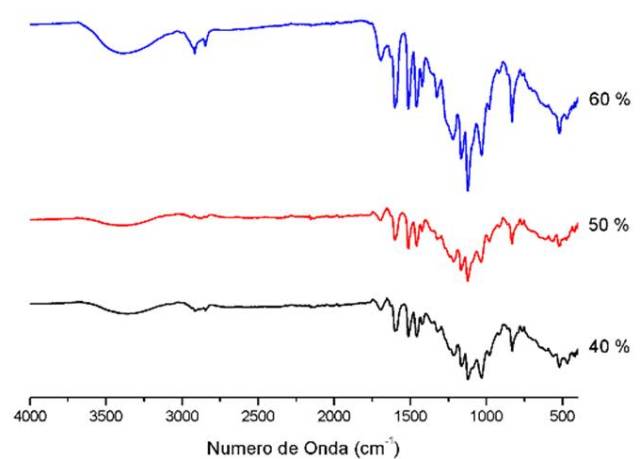
Análise de FTIR das ligninas extraídas para 40%, 50% e 60% de etanol
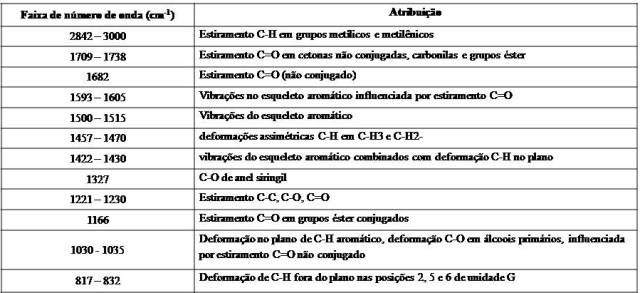
Atribuições das bandas do espectro de absorção no infravermelho da lignina
Conclusões
O trabalho permitiu constatar que a porcentagem de lignina extraída pelo método Organossolve-Etanol a 50% foi mais eficiente em relação às demais proporções. Os resultados obtidos para a espectrometria da região do infravermelho (FTIR) da lignina apresentaram bandas mais intensas para maior porcentagem de etanol, já nas proporções de etanol 50% e 40% as bandas foram menos intensas. Podemos inferir que a maior porcentagem de etanol corroborou para maior intensidade das bandas.
Agradecimentos
Laboratório de Fotoquímica - IBILCE/UNESP
Referências
1- PANOULAS VF, MILIONIS HJ, DOUGLAS KM, NIGHTINGALE P, KITA MD, KLOCKE R, et al. Association of serum uric acid with cardiovascular disease in rheumatoid arthritis. Rheumatology, V. 46, n. 1466-70, 2007.
2-FAIX, O. Fourier transformed infrared spectroscopy. Methods in Lignin Chemistry, p. 458-464, 1992.
3-DING, T. Y.; HII, S. L.; ONG, L. G. A. Comparison of pretreatment strategies for conversion of coconut husk fiber to fermentable sugars. BioResources, v. 7, p. 1540-1547, 2012.
4-SHI, J.; LI, J. Metabolites and chemical group changes in the wood forming tissue of Pinus koralensis under inclined condition. BioResources, v. 7, p. 3463-3475, 2012.
5-KUBO, J. H.; KADLA, J. F. Hydrogen bonding in lignin: a Fourier transform infrared model compoundstudy. Biomacromolecules, v. 6, p. 2815-2821, 2005
































