Caracterização térmica e análise do perfil de dissolução da mistura física e do complexo de inclusão entre 2-oleil-1,3-dipalmitoil-glicerol e β-ciclodextrina
ISBN 978-85-85905-23-1
Área
Química Orgânica
Autores
Cavalcante, A.N. (UFPI) ; Feitosa, C.M. (UFPI) ; Santos, F.P.S. (UFPI) ; Sousa, A.P.R. (UFPI) ; Araújo, C.M. (IFPI) ; Lima, L.K.F. (UFPI) ; Nascimento, A.S. (UFPI) ; Figuerêdo, J.S. (UFPI)
Resumo
A banha extraída das sementes de Platonia insignis Mart apresenta um alto teor de ácidos graxos; sendo muito usada para o tratamento de várias doenças, como problemas de pele, cicatrizante e anti-inflamatória. A substância 2-oleil-1,3-dipalmitoil- glicerol (ODG) apresenta baixa solubilidade, a fim de aumentar a solubilidade, foi elaborado o complexo de inclusão entre ODG e β-CD. O objetivo desse estudo foi caracterizar a mistura física e o complexo de inclusão (CI) e avaliar o perfil de dissolução. O CI foi obtido por solubilização e caracterizado por DSC, TG, MEV e ensaios de dissolução. Os resultados sugeriram a formação do CI entre ODG e β-CD. Portanto a taxa de dissolução do complexo de inclusão e da mistura física foram significativamente melhorados em comparação com a substância ODG.
Palavras chaves
Platonia insignis Mart; complexo de inclusão; dissolução
Introdução
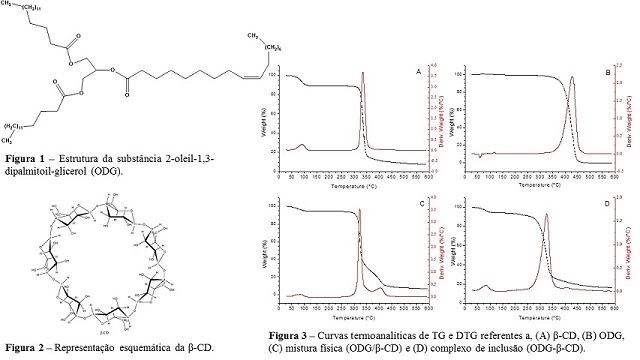
O bacurizeiro é uma espécie vegetal que pertence à família Clusiaceae, subfamília Clusioideae, gênero Platonia Mart. é uma espécie monotípica, classificada como Platonia insignis Mart. (BRAGA, 1976), composta ao menos por 1000 espécies e 47 gêneros distribuídos em regiões tropicais e subtropicais da Terra. P. insignis Mart é oriunda da região amazônica do Brasil e Guiana, sendo também encontrada na Colômbia e no Paraguai, sempre ocorrendo em áreas abertas de vegetação rasteira, e principalmente, em vegetação secundária, sendo raramente encontrada em floresta primária densa (CAVALCANTE, 1988; CHITARRA; CHITARRA, 2005). O bacuri, fruto obtido a partir da P. insignis Mart., é grande, arredondado, com casca grossa possuindo coloração amarelado e dentro dela contém a polpa, de coloração esbranquiçada, sendo viscosa apresentando odores e sabores bastante agradáveis (FONTENELE et al., 2005). Espécies pertencentes à família Clusiaceae são importantes plantas medicinais bastante utilizadas na medicina popular brasileira, principalmente para o tratamento de eczemas, herpes, doenças gastrointestinais, dermatite, esquistossomose, leishmaniose e malária. Estudos envolvendo as propriedades biológico-farmacológicas dessas espécies podem ser observados na literatura sendo que a maior parte desses estudos se concentram, sobretudo nos extratos vegetais das sementes da P. insignis Mart. A “banha de bacuri”, extraída das sementes, comumente é usada na medicina popular como cicatrizante de queimaduras e no tratamento de doenças dermatológicas (AGRA et al., 2007). Em ensaios in vivo a banha demostrou um grande potencial para acelerar a cicatrização de feridas de pele em ratos (SANTOS et al., 2013; FEITOSA et al., 2016). 2-oleil-1,3-dipalmitoil-glicerol (ODG), Figura 1, extraído das sementes da P. insignis Mart. é solúvel em solventes apolares e pouco solúvel em água, não havendo, portanto, relatos na literatura sobre as suas propriedades farmacológicas e toxicológicas, justificando assim, a necessidade da realização desse estudo. Fármacos pouco solúveis em água, geralmente manifestam comportamento in vivo inferior aqueles de maior solubilidade, como baixa biodisponibilidade, maior variabilidade inter-paciente e liberação incompleta das formas farmacêuticas (SPRICIGO et al., 2007). Dessa forma, fármacos pouco solúveis em água, como a substância ODG, apresentam, em geral, problemas de biodisponibilidade, sendo a dissolução o fator limitante para a absorção dos mesmos (AMIDON et al., 1995). Dentre as técnicas empregadas para aumentar a taxa de dissolução destaca-se o emprego da complexação de fármacos com ciclodextrinas – CD’s (LIU, 2000). As CD’s são produtos cíclicos da hidrólise enzimática do amido por alguns microorganismos (LOFTSSON; MASSON, 2001). As três ciclodextrinas naturais são chamadas de alfa (α- CD), beta (β-CD) e gama (γ-CD), constituídas, respectivamente, por seis, sete e oito unidades de D-(+)-glicopiranose, estas unidades estão unidas por ligações α-1,4 (FRACETO et al., 2007), como pode-se observar na estrutura da β-CD representada na Figura 2. As moléculas de CD’s apresentam conformação espacial com tronco de forma cônico, com grupos hidroxilas primários e secundários voltados para a face externa, conferindo um caráter hidrofílico para a superfície externa, enquanto que a cavidade interna da molécula é ligeiramente hidrofóbica, ou seja, as CD’s possuem a parte externa hidrofílico e uma cavidade interna um pouco hidrofóbica (AGUIAR et al., 2014), esta cavidade permite às CD’s encapsularem moléculas que apresentem dimensões compatíveis, alterando as propriedades físico-químicas dessas moléculas, como, solubilidade em água, estabilidade e biodisponibilidade (MATIOLI, 2000). As CD’s são solúveis em água e possuem a capacidade de formar complexos de inclusão reversíveis com moléculas apolares, incrementando de forma bastante significativa sua solubilidade em meio aquoso (VEIGA et al., 2006). Apesar do grande número de trabalhos na literatura desenvolvidos na linha de pesquisas de compostos de inclusão com CD’s, não existem nenhum estudo envolvendo a encapsulamento de compostos extraídos das sementes de P. insignis Mart. com β-CD. Nesse contexto, este trabalho teve como objetivo preparar e caracterizar o complexo de inclusão entre a substância 2-oleil-1,3-dipalmitoil-glicerol e beta-ciclodextrina, utilizando para caracterização físico-química calorimetria diferencial exploratória (DSC), termogravimetria (TG), microscopia eletrônica de varredura (MEV) e testes de dissolução ou liberação in vitro, a fim de comparar os efeitos da complexação nas propriedades físico-químicas do composto na ausência e na presença da β-CD.
Material e métodos
Os frutos foram coletados na cidade de Água Branca – PI. As sementes dessa espécie foram então separadas dos frutos e após secagem, a 50 °C numa estufa, foram trituradas. A substância 2-oleil-1,3-dipalmitoil-glicerol (ODG) foi isolada por cromatografia em coluna a partir da fração hexânica e caracterizada por RMN 1H, RMN 13C e IR. Preparação da mistura física (ODG/β-CD): Este método baseia-se na simples mistura dos componentes sem adição de água de acordo com Zhou e colaboradores (2013) com algumas modificações. Preparação do complexo de inclusão (ODG-β-CD): Pesou-se 30 mg de ODG e solubilizou-se em 20 mL de etanol P.A. a solução foi mantida a 40 ºC sob agitação por 2 h. Em seguida pesou-se 81,9 mg de β-CD que foi solubilizada em 250 mL de uma mistura de etanol-água (1:4). Depois misturou-se as soluções onde o sistema foi mantido sob agitação magnética com aquecimento de 70 °C por 2 h. O sistema foi roto-evaporado para eliminação do etanol. Posteriormente a solução foi resfriada a -45 ºC e em seguida liofilizada por 48 horas. Análises termogravimétrica (TG) e calorimetria exploratória diferencial (DSC): As curvas de TG/DSC foram produzidos usando um equipamento Shimadzu®, modelo TGA-51 no Laboratório Interdisciplinar de Materiais Avançados (LIMAV) da Universidade Federal do Piauí (UFPI). As amostras (10,0 mg para as duas técnicas) foram colocadas em panelas herméticas de alumínio, com os experimentos sendo realizados sob um fluxo de gás inerte de nitrogênio (100 mL min-1), a uma taxa de aquecimento de 20 °C min-1 e em uma faixa de temperatura de 30 ºC a 600 °C para ambas as técnicas. Microscopia eletrônica de varredura (MEV): As estruturas morfológicas foram investigadas e fotografadas utilizando um microscópio eletrônico varredura (MEV) com fonte de elétrons por emissão de campo, marca FEI, modelo Quanta, FEG 250, com tensão de aceleração de 1 a 30 kV, equipado com EDS de SDD (Silicon drift detectors), marca Ametek, modelo HX-1001 (detector Apollo X-SDD) no Laboratório Multiusuário de Microscopia Avançada (LMMA) da UFPI. As amostras foram fixadas em fita dupla face de carbono e para melhorar a condutividade elas foram recobertas com Au (ouro) na metalizadora, marca Quorum, modelo Q150R, durante 30 s, a uma corrente de íon de 20 mA, por plasma gerado em atmosfera de argônio. Ensaios de dissolução: As amostras (1,0 mg) foram encapsuladas dentro de cápsula de gelatina dura. O teste de dissolução foi realizado em triplicata, usando 900 mL de solução aquosa de HCl, pH 1,3 e temperatura de 37 °C a fim de permitir que a realização do ensaio ocorresse em condições análogas às verificadas no trato gastrointestinal usando equipamento dissolutor (Nova Ética – Modelo 299) com pá rotativa a 50 rpm. Foram coletadas alíquotas de 5 mL em intervalos de tempo pré- determinados e, imediatamente, filtradas em papel filtro de 25 µm. Após filtração, as concentrações foram determinadas por espectrofotometria UV-Vis modelo AJX-3000PC Espectrofotômetro a 225
Resultado e discussão
Análises térmicas - Os métodos de análises térmica são bastante utilizados na
caracterização de sistemas constituídos por mais de um componente como os complexos
de inclusão. Estes métodos são feitos comparando-se os comportamentos térmicos dos
componentes isoladamente com os dos possíveis complexos de inclusão. Comumente, se
detecta a formação do complexo de inclusão, utilizando análise termogravimétrica
(TG), comparando-se a temperatura de início de degradação da molécula encapsulada
com a do complexo. Quando ocorre a complexação, a degradação da molécula hóspede
ocorrerá a temperaturas mais elevadas uma vez que esta molécula estará protegida na
cavidade da ciclodextrina (ARAÚJO et al., 2007). Na análise termogravimétrica obtém-
se duas curvas, uma relacionada ao percentual de perda de massa (TG) e outra
relacionada a derivada de perda de massa (DTG). A última permite a determinação
precisa da temperatura em que ocorre determinada perda de massa da amostra (MACEDO,
2010). A calorimetria exploratória diferencial (DSC) é uma técnica bastante
utilizada para confirmar a formação do complexo de inclusão no estado sólido, devido
sua sensibilidade em detectar possíveis alterações nos eventos térmicos
característicos da molécula encapsulada quando se encontra no interior da cavidade
da CD, assim como a estabilidade do sistema e sua cristalinidade (LYRA et al., 2010;
WANG et al., 2011). As curvas de TG e DTG para β-CD, ODG, mistura física e complexo
de inclusão são mostradas na Figura 3 enquanto que as curvas de DSC são mostradas na
Figura 4. O termograma da β-CD (Figura 3A) mostra dois estágios de perda da massa: o
primeiro foi registrado entre 50 °C e 114 °C, indicando a perda de moléculas de
água. As moléculas de água estão incluídas na cavidade e também localizadas nos
interstícios entre as macromoléculas (LOUIZ et al., 2015). O segundo estágio de
maior intensidade foi registrado entre 309 °C e 375 °C relacionado com a
decomposição de estrutura β-CD devido à transição da fase sólida para líquida. Curva
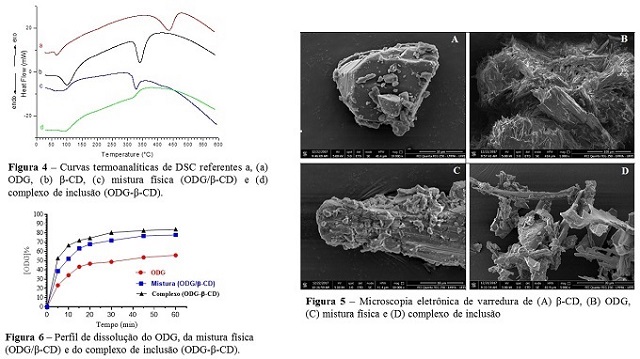
de DSC da β-CD (Figura 4b) corroborou com estas observações. A Figura 4b mostrou a
presença de dois eventos endotérmicos, o primeiro, iniciando em 70 °C e finalizando
em 100 °C, possivelmente referente ao processo de evaporação de água presente no
interior de sua cavidade hidrofóbica (WANG et al., 2011) e o segundo evento com
início em 312 ºC até 335 °C, provavelmente resultante da fusão das unidades
glicosídicas da β-CD. O termograma de ODG (Figura 3B) mostrou que a decomposição
dessa substância iniciou em 350 °C e terminou em 475 °C. A curva de DSC da ODG
(Figura 4a) confirmou este resultado onde mostrou um evento endotérmico iniciando em
75 °C e terminando por volta de 435 °C podendo ser atribuído ao início de fusão dos
produtos de decomposição desta substância. As curvas termoanalíticas da mistura
física (Figura 3C e Figura 4c) parecem ser a simples superposição dos compostos
livres como pode ser observado na curva DTG onde mostra claramente os três picos da
derivada de perda de massa correspondente das substâncias na sua forma livre.
Enquanto que as curvas termoanalíticas do produto obtido pela técnica de
liofilização (Figura 3D) mostrou que a decomposição do complexo de inclusão ocorreu
numa faixa maior de temperatura 225-400 °C. Entretanto, um padrão diferente foi
observado na curva de DSC do complexo de inclusão (Figura 4d), resultando em um
sistema com características únicas, diferentemente do comportamento termoanalítico
das duas substâncias livres, sugerindo uma mudança na estrutura da substância após a
formação do complexo de inclusão. Verifica-se que o pico endotérmico em 437 °C no
DSC da ODG, associado a fusão dessa substância, desaparece na curva do complexo de
inclusão, indicando uma maior estabilidade do ODG complexado quando comparado ao ODG
livre. Tal comportamento evidencia um ganho de estabilidade térmica para o fármaco
encapsulado, provavelmente como resultado de interações com a cavidade, indicando a
complexação entre o ODG e β-CD. Nossas observações foram consistentes com outros
trabalhos encontrados na literatura (Zhou et al., 2014; KFOURY et al., 2014).
Microscopia eletrônica de varredura (MEV) - A microscopia eletrônica de varredura é
uma técnica de análise qualitativa bastante adequada para visualizar a textura
superficial dos filmes superficiais depositados, isto é, visualizar os aspectos
morfológicos de materiais diversos, tais como, CD's e medicamentos (ARAÚJO et al.,
2008; DUCHÊNE, 1987). Esta análise constitui uma ferramenta importante para
verificar mudanças no perfil cristalino de moléculas, decorrentes do processo de
síntese ou do processamento farmacêutico (RIBEIRO et al., 2008). A Figura 5 mostra
as imagens obtidas por MEV de β-CD, ODG, mistura física e complexo de inclusão. As
imagens de MEV mostraram que a forma e o tamanho do complexo de inclusão foram
completamente diferentes das imagens dos componentes livres, β-CD e ODG. As
micrografias da β-CD (Figura 5A) apresentou-se com morfologia homogênea e cristais
poliédricos, estando esse resultado de acordo com os achados de Chen e colaboradores
(2011), indicando um perfil mais cristalino. A Figura 5B, mostra as imagens da
substância ODG, nela pode-se observar que se trata de uma substância com
característica amorfa. As imagens da mistura física (Figura 5C) revelaram
semelhanças tanto com os cristais das moléculas de β-CD e a forma amorfa das
moléculas de ODG, ou seja, a mistura física continha a morfologia de ambos os
componentes livres. Em contraste, o complexo de inclusão (Figura 5D) apareceu como
partículas irregulares, nas quais a morfologia original de ambos os componentes
desapareceram e pequenos agregados de peças amorfas e de tamanho irregular estavam
presentes. Essas imagens demonstraram ainda que, quando os pós de β-CD e ODG
simplesmente se misturaram fisicamente, eles continuaram a existir em suas formas
originais e individuais, enquanto que, quando as soluções dos dois compostos foram
misturados, formaram uma estreita associação, em que a ODG já não existia em seu
estado totalmente amorfo, revelando-se, assim, uma aparente interação entre ODG e β-
CD, confirmando assim, a formação do complexo de inclusão. Ensaios de dissolução - A
dissolução consiste no processo de liberação do fármaco de sua forma farmacêutica,
tornando-se, dessa forma disponível para ser absorvido ou aproveitado pelo organismo
(CHOWDARY E RAJYALAKSHMI, 1987). Assim os estudos de dissolução são importantes uma
vez que permitem, através de ensaios in vitro, prever a disponibilidade do fármaco
in vivo. Por meio da técnica de espectrofotometria na região do UV-Vis, observou-se
que a substância 2-oleil-1,3-dipalmitoil-glicerol possui um pico máximo de
absorbância no comprimento de onda, λ, de 225 nm em solução binária etanol-água
(9:1). A Figura 6 mostra os diferentes perfis de dissolução da substância ODG, da
mistura física e do complexo de inclusão em cápsulas de gelatina. Em todos os tempos
analisados a porcentagem acumulada de ODG na forma livre foi sempre menor que da
mistura física (ODG/β-CD) e esta foi menor que do complexo de inclusão (ODG-HP-β-
CD). Na Figura 6 mostra que as porcentagens acumuladas de ODG no complexo foram
ligeiramente maiores do que a da mistura física. A percentagem cumulativa liberada
da ODG na forma livre e na forma encapsula, tanto complexo de inclusão quanto a
mistura física, manteve-se praticamente constante a partir dos 30 min. Assim, a
melhoria significativa da eficiência de dissolução do complexo de inclusão e da
mistura física deve ser atribuída à formação de complexos.
FIGURAS AGLUTINADAS
FIGURAS AGLUTINADAS
Conclusões
O composto 2-oleil-1,3-dipalmitoil-glicerol (ODG) foi obtido a partir do extrato hexânico das sementes de Platonia insignis Mart. O complexo de inclusão entre a substância ODG e β-CD foi preparado com êxito pelo método de solubilização seguido por liofilização e caracterizado por DSC, TG e MEV. Os resultados deste trabalho indicaram claramente a efetiva formação do complexo de inclusão entre a substância ODG com β- ciclodextrina (ODG-β-CD). O trabalho mostrou que a complexação do ODG provocou mudanças nas propriedades deste fármaco, como um aumento na sua solubilidade e alteração no seu perfil de liberação. Estas mudanças são de grande importância na aplicabilidade deste composto, podendo causar melhoras na biodisponibilidade do mesmo. Os resultados mostraram que β-CD pode ser um excipiente adequado para aumentar a solubilidade e libertação controlada do fármaco ODG. Tais resultados foram importantes para um melhor entendimento das propriedades físico-química do complexo de inclusão, podendo futuramente ser um potencial alternativa para a terapia de algumas doenças.
Agradecimentos
Ao Laboratório Interdisciplinar de Materiais Avançados (LIMAV) da UFPI pelas análises de TG e DSC. Ao Laboratório Multiusuário de Microscopia Avançada (LMMA) da UFPI pe
Referências
AGUIAR, U. N.; LIMA, S. G.; ROCHA, M. S.; FREITAS, R. M.; OLIVEIRA, T. M.; SILVA, R. M.; MOURA, L. C. B.; ALMEIDA, L. T. G. Preparação e caracterização do complexo de inclusão do óleo essencial de Crton zehntneri com β-ciclodextrina. Química Nova, n. 1, v. 37, p. 50-55, 2014.
AGRA, M. F.; FREITAS, P. F.; BARBOSA-FILHO, J. M. Synopsis of the plants known as medicinal and poisonous in Northeast of Brazil. Brazilian Journal of Pharmacognosy, v. 17, p. 114–140, 2007.
AMIDON, G. L.; LENNERNÄS, H.; SHAH, V. P.; CRISON, J. R. A Theoretical Basis for a Biopharmaceutic Drug Classification: The Correlation of in Vitro Drug Product Dissolution and in Vivo Bioavalailability. Pharmaceutical Research, v. 12, p. 413-420, 1995.
ARAÚJO, E. C. et al. Use of medicinal plants by patients with cancer of public hospitals in João Pessoa (PB). Revista Espaço para a Saúde, v. 8, n. 2, p. 44-52, 2007.
ARAUJO, M. V. G.; VIEIRA, E. K. B.; LÁZARO, G. S.; CONEGERO, F. S.; FERREIRA, O. P.; ALMEIDA, L. E.; BARRETO, L. S.; COSTA-JR, N. B.; GIMENEZ, I. F. Sulfadiazine/hydroxypropyl-β-cyclodextrin host-guest system: characterization, phase solubility and molecular modeling. Bioorganic & Medicinal Chemistry, v.16, p. 5788-5794, 2008.
BRAGA, R. Plantas medicinais do Nordeste: especialmente do Ceará, ESAM, Mossoró, Brazil, 1976.
CAVALCANTE, P. B. Frutas comestíveis da Amazônia. 6 ed. Belém:CNPq/Museu Paraense Emílio Goeldi, 279 p. (ColeçãoAdolpho Ducke), 1996.
CHITARRA, A. B.; CHITARRA, M. I. F. Pós-colheita de frutos e hortaliças, Lavras, 256, 2005.
CHOWDARY, K. P. R.; RAJYALAKSHMI, Y. Dissolution rate in modern pharmacy. Eastern Pharmacist, v. 30, p. 51-4, 1987.
DUCHÊNE, D. Cyclodextrins and their industrial uses. Paris: Editions de Santé, 1987
FEITOSA, C. M.; CHAVES, S. K. M.; SANTOS, P. R. P.; CAVALCANTE, N. C.; COSTA JÚNIOR, J. S.; RASHED, K. Anticholinesterase activity and effects on memory in adult rats of 1, 3-distearoyl-2-oleoylglycerol substance isolated from Platonia insignis Mart. (bacurizeiro). The Pharma Research, n. 14, v. 2, p. 39-52, 2016.
FONTENELE, M. A.; FIGUEIREDO, R.W.; MAIA, G. A.; ALVES, R. E.; SOUSA, P. H. M. D.; SOUZA, V. A. B. D. Conservação pós-colheita de bacuri (Platonia insignis Mart.) sob refrigeração e embalado em PVC. Revista Ceres. v.57, p. 292-296, 2005.
FRACETO, L.F.; GONÇALVES, M.M.; MORAES, C.M.; ARAÚJO, D.R.; ZANELLA, L.; PAULA, E.; PERTINHEZ, T.A. Caracterização do complexo de imclusão ropivacaína:β-ciclodextrina. Química Nova, v. 30, p. 1203-1207, 2007.
LIU, R. Water Insoluble Drug Formulation, Interpharm, CRC Press. New York, 2000.
LOFTSSON, T.; MASSON, M. Cyclodextrins in topical drug formulations: theory and practice. International Journal of Pharmacy. v. 225, p. 15, 2001.
LOUIZ, S.; LABIADH, H.; ABDERRAHIM, R. Synthesis and spectroscopy studies of the inclusion complex of 3-amino-5-methyl pyrazole with beta-cyclodextrin. Spectrochimica Acta Part A: Molecular and Biomolecular Spectroscopy, v. 134, p. 276-282, 2015.
LYRA, M. A. M.; ALVES, L. D. S.; FONTES, D. A. F.; SOARES SOBRINHO, J. L.; ROLIM NETO, P. J. Revista de Ciências Farmacêuticas Básica e Aplicada, v. 31, p. 117, 117, 2010.
MACEDO, L, F, O. Preparação e Caracterização de complexo de inclusão entre trimetoprim e 2-Hidroxipropil-Gama-Ciclodextrina. Dissertação - Mestrado. Universidade Federal de Sergipe. 2010.
MATIOLI, G. Ciclodextrinas e suas aplicações em: alimentos, fármacos, cosméticos, agricultura, biotecnologia, química analítica e produtos gerais, Eduem, Maringá, Brazil, 2000.
RIBEIRO, A.; FIGUEIRAS, A.; SANTOS, D.; VEIGA, F. Preparation and solid-state characterization of inclusion complex formed between miconazole and methyl-β-ciclodextrin. AAPS PharmSciTech, v. 9, p. 1102-1109, 2008.
SANTOS, P. R. P.; CARVALHO, R. B. F.; COSTA JUNIOR, J. S.; FREITAS, R. M.; FEITOSA, C. M. Survey of physicochemical and pharmacological properties of extracts and compounds isolated from Platonia insignis Mart. a perspective for developing phytomedicines. Brazilian Journal of Pharmaceutical Sciences, v. 94, p. 161-168, 2013.
SPRICIGO, R.; BOTELHO, K.; CONSIGLIERI, V.; SERRA, C. H. R. Obtenção e Avaliação de Complexos de Inclusão de Furosemida com β-ciclodextrina e hidroxipropil-β-ciclodextrina: Efeitos sobre as Propriedades de Dissolução do Fármaco. Latin American Journal of Pharmacy, v. 27, n. 5, p. 645-653, 2008.
VEIGA, F.; PECORELLI, C.; RIBEIRO, L. As ciclodextrinas em tecnologia farmacêutica. Edições Minerva Coimbra. Coimbra. 1ª edição, 2006.
ZHOU, Q.; WEI, X.; DOU, W.; CHOU, G.; WANG, Z. Preparation and characterization of inclusion complexes formed between baicalein and cyclodextrins. Carbohydrate Polymers, v. 95, p. 733-739, 2013.
WANG, J.; CAO, Y.; SUN, B.; WANG, C. Physicochemical and release characterisation of garlic oil-β-cyclodextrin inclusion complexes. Food Chemistry, v. 127, p. 1680-1685, 2011.











