Crescimento e Estudo das Propriedades Estruturais e Térmicas do Cristal Ternário de Cu(II) com 1,10- Fenantrolina e Serina para aplicação em antitumorais.
ISBN 978-85-85905-23-1
Área
Materiais
Autores
Ramos, M.C.R. (UNIVERSIDADE FEDERAL DO MARANHÃO) ; Gomes de Oliveira Neto, J. (UNIVERSIDADE FEDERAL DO MARANHÃO) ; Oliveira dos Santos, A. (UNIVERSIDADE FEDERAL DO MARANHÃO)
Resumo
Íons de metais de transição como o cobre tem sido alvo de estudos e vem ganhando espaço no meio científico, especialmente em terapias no tratamento do câncer. Este trabalho descreve o crescimento e a caracterização do cristal pelo método da evaporação lenta do solvente. O material foi caracterizado por DRX e TG/DTA. O resultado de DRX em conjunto com o refinamento Rietveld confirma que o cristal apresenta estrutura triclínica, grupo espacial P1 e parâmetros de rede: a = 7,6358(3) Å, b = 10,0523(4) Å, c = 12,0204(7) Å. A curva de TG/DTA mostrou uma transição de fase em 68,1 ºC, e três eventos em 129,8, 200,4 e 299,3 ºC atribuídos a decomposição. Assim, o método de evaporação lenta do solvente demonstrou ser eficaz na formação do cristal ternário de Cu (II) com Fenantrolina e Serina.
Palavras chaves
Cristal; Serina; Antitumoral
Introdução
Os complexos de metais de transição caracterizados pela sua alta estabilidade, versatilidade estrutural e com propriedades espectroscópicas e redox únicas, tem sido amplamente explorado em estudos de ligação ao DNA, com objetivo de desenvolver novas drogas com propriedades farmacológicas significativas, ou atuar como novos agentes de diagnósticos (VARADARAJAN et al., 2007) Uma das utilizações mais importantes e promissoras de complexos metálicos em terapia é no tratamento do câncer, a pesquisa de complexos metálicos com propriedades antitumorais iniciou-se com a descoberta da atividade antitumoral do complexo cis-diaminodicloroplatina(II), comumente conhecido como cisplatina, por Rosenberg e van Camp no final dos anos sessenta e tem sido estimulada com a descoberta da atividade citotóxica de diversos outros complexos de platina e outros metais, tais como gálio e cobre (NEIDLE, 2005; ROSENBERG et al., 1969; ROSENBERG, 1970; ZHANG et al, 2009). Os compostos de cobre têm se destacado devido este metal estar presente em inúmeros processos biológicos no corpo humano e tem ganhado espaço na área da química medicinal inorgânica, principalmente quando comparado a drogas antitumorais sintetizados a partir de metais de transição não encontrados naturalmente no organismo como é o caso da cisplatina (KELLETT et al., 2012) Inúmeros complexos de Cu (II) com ligantes heterocíclicos divergentes, como ácido glutâmico, fenantrolina, bipiridina, ácido aspártico, e L- ou DL- aminoácidos (serina, glicina, arginina, lisina, etc) tem sido sintetizado, e suas interações com o DNA caracterizadas por YODOSHI et al. e ZHANG et al. O objetivo do trabalho foi crescer e caracterizar o cristal de Cobre (II) com 1,10 – Fenantrolina e Serina, pelo método da evaporação lenta do solvente.
Material e métodos
O cristal foi crescido por meio da preparação de solução equimolar, pelo método da evaporação lenta do solvente. Inicialmente a 1,10- Fenantrolina(0,495g), foi solubilizada com um volume de 10 ml, sendo 7ml de metanol e 3ml de água deionizada sob agitação constante. Logo após foi adicionado o nitrato de cobre II (0,625g) ficando por alguns minutos em agitação a temperatura de 70 °C. Adiante, foram adicionados um por vez o aminoácido (0,053g) e o bicarbonato de sódio (0,042g). Esta solução foi deixada sob agitação constante na mesma temperatura acima mencionada por um período de 3 horas para total homogeneização. Ao final, a solução foi coberta com papel PVC realizando pequenos furos aleatórios e colocada em uma estufa com temperatura constante de 35 °C, até a formação do cristal. Para a técnica de Difratometria de Raios X, foi utilizado o difratômetro D8 advance (Bruker) com Radiação Cu Kα (λ = 1.5406 Å) tubo operando a 40 Kv/ 40 mA e detector linear LynxEye. Os dados foram coletados em geometria do tipo Bragg-Bretanona faixa angular de 5-50° 2θ com passo de 00,2° e tempo de contagem de 0,5 seg./passo. Conjuntamente com a difração de raios X do cristal complexado será empregado o método Rietveld (YOUNG, 1999). As curvas de TG/DTA foram realizadas em simultâneo por um analisador térmico da marca Shimadzu Instruments modelo DTA-60, com aproximadamente 4mg de amostra, em atmosfera de nitrogênio com vazão de 100mL/min, e razão de aquecimento de 10 °C, utilizando cadinho de α-alumina, com faixa de 25 a 900 °C.
Resultado e discussão
A estrutura cristalina do material foi confirmada por intermédio de medidas de
DRX. A Figura 1a exibe o padrão de DRX do pó refinado pelo método de Rietveld.
O refinamento apresentou fatores Rwp= 8,08%, Rp= 5,37% e S = 2,897 e,
portanto, em conformidade com padrões de confiabilidade. A amostra cristaliza-
se em estrutura triclínica, grupo espacial P1. Os parâmetros de rede obtidos
pelo refinamento Rietveld podem ser visualizados na Figura 2a, com um
comparativo dos dados cristalográficos obtidos por (ESPARZA et al.,1995). Na
curva de TG fig. 1b os dois primeiros eventos endotérmicos observados na aérea
pontilhada I do gráfico, nas temperaturas entre 22,4 a 47,7 °C e 48,6 e 73,9
°C refere-se à evaporação de água no complexo. Na aérea II destaca-se dois
eventos na temperatura entre 110,3 a 131,1 ° C e 177,7 a 210,6 °C referente a
decomposição da fenantrolina. No 5ª evento sugere-se a decomposição do
aminoácido na estrutura cristalina, nas temperaturas entre 285,1 a 327,3 °C, o
que se confirma com o surgimento de um pico exotérmico na curva DTA em 299,3
°C. No último evento na temperatura entre 389 a 545,3 °C a perda de massa é de
42,79%, estando em concordância com a decomposição da amostra. O pico
exotérmico presente na curva DTA em 462,3 °C infere a perda de matéria
referente ao material sintetizado.
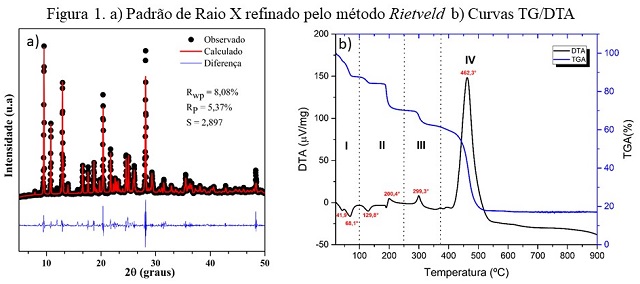
a) Padrão de Raio X refinado pelo método Rietveld b) Curvas TG/DTA
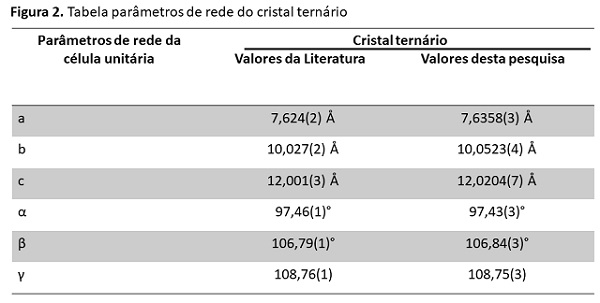
Parâmetros de rede do cristal
Conclusões
O estudo estrutural demonstrou alta cristalinidade para o cristal obtido. A análise térmica evidenciou uma transição de fase pela perda de água de hidratação, bem como não apresenta estabilidade térmica alta, visto que ao atingir a temperatura superior a 60ªC apresenta perda de água. Assim, o método de evaporação lenta do solvente demonstrou ser eficaz na formação do cristal ternário de cobre com fenantrolina e serina que poderá ser utilizado como antitumoral.
Agradecimentos
Os autores agradecem a Capes, UFMA e FAPEMA pelo apoio financeiro e bolsas disponibilizadas.
Referências
ESPARZA, R. M.; MOLINS, E.; BRIASO-PENALVA, J.L.; REDON, R. Aqua (1,10-phenanthroline)(L-serinato)-copper (II) Nitrate. Acta Crystallographica, C51, (1995), pp. 1505-1508.
KELLETT, Andrew et al. Radical-induced DNA damage by cytotoxic square-planar copper(II) complexes incorporating o-phthalate and 1,10-phenanthroline or 2,2′-dipyridyl. Free Radical Biology And Medicine, v. 53, n. 3, p.564-576, ago. 2012.
NEIDLE, Stephen; THURSTON, David E. Chemical approaches to the discovery and development of cancer therapies. Nature Reviews Cancer, v. 5, n. 4, p. 285-296, 2005.
ROSENBERG, B.; CAMP, L.V.; TROSCO, J.E.; MANSOUR, V.H. Platinum Compounds: a New Class of Potent Antitumoral Agents. Nature, 222, 385-386, 1969.
ROSENBERG, Barnett; VANCAMP, Loretta. The successful regression of large solid sarcoma 180 tumors by platinum compounds. Cancer Research, v. 30, n. 6, p. 1799-1802, 1970.
VARADARAJAN, Uma, MUNUSAMY, Elango, B. U. Nair. Copper(II) Terpyridine Complexes: Effect of Substituent on DNA Binding and Nuclease Activity. Eur. J.Inorg. Chem. 2007, 3484-3490.
YODOSHI, M.; ODOKO, M.; OKABE, N., Structures and DNA-Binding and cleavage properties of ternary copper(II) complexes of glycine with phenanthroline, bipyridine, and bipyridylamine. Chemical Pharmaceutical Bulletin, Japan, v. 55, p. 853-860, 2007.
YOUNG, R. A. The rietveld method. International union of crystallography, 1993.
ZHANG, S.; ZHOU, Ternary copper(II) complex of 1,10-phenthroline and L-glycine: crystal structure and interaction with DNA. Journal of Coordination Chemistry, United Kingdom, v. 61, p. 2488-2498, 2008.











