NANOPARTÍCULAS A BASE DE QUITOSANA PARA ENCAPSULAMENTO DE CARVACROL
ISBN 978-85-85905-23-1
Área
Iniciação Científica
Autores
Almeida, J.L.I.O.A. (UECE) ; Junior, J.R.P. (UFC) ; André, W.P.P. (UECE) ; Abreu, F.O.M.S. (UECE)
Resumo
Nanopartículas de Quitosana (NPs) têm sido estudadas para diversas aplicações como em liberação controlada de fármacos e adsorção de metais devido as características que podem apresentar. Nesse trabalho desenvolveu- se 8 sistemas para o encapsulamento de carvacrol. As nanopartículas com melhor conjunto de propriedades foram selecionadas para caracterização por espectroscopia de infravermelho (FTIR) e curva de liberação in vitro. A análise de FTIR apresentou as principais bandas do carvacrol e dos polímeros que compõem as NPs. Os perfis de liberação in vitro das NPs foram em torno de 30% e 55%, após 72h, indicando um perfil de liberação controlada, por fim, as NPs desenvolvidas à base de QUI apresentaram um conjunto promissor de características para o encapsulamento e liberação do carvacrol.
Palavras chaves
Encapsulamento; Quitosana; Carvacrol
Introdução
Os sistemas de liberação controlada têm sido amplamente estudados, com grande aplicação na área farmacêutica e biomédica, também são utilizados para proteger e liberar com regularidade alguns princípios ativos, diminuindo a toxicidade e prolongando a sua atividade biológica. São utilizados polímeros naturais à base de polissacarídeos com a finalidade de aprimorar a biocompatibilidade do sistema. Encapsulamento é um processo que retém o material em um revestimento que isola e protege este contra o ambiente externo (IMBROGNO et al., 2015). As NPs à base de polissacarídeos têm sido amplamente estudadas devido à capacidade de encapsular princípios ativos de forma eficiente em suas matrizes poliméricas hidrofílicas, através de interações iônicas entre compostos que apresentam cargas opostas (ABREU, 2008). As NPs são estruturas coloidais, que são utilizadas para revestir os fármacos visando evitar a degradação de princípio ativo, melhorar a eficácia de sua atividade, diminuir a sua toxicidade e expandir a sua atividade biológica (CLEMENTE-NAPIMOGA, et al, 2012). As NPs do tipo core-shell têm em sua composição, um polímero reticulado por um reticulador iônico e revestido por outro polímero. Deste modo, dependendo de seus constituintes, concentração da solução e método de produção das NPs, pode ocorrer variação de suas propriedades, como o tamanho médio das NPs e a capacidade de encapsulamento. O carvacrol tem atividades microbiológicas relatadas na literatura, dentre elas: atividade antioxidante, atividade bactericida, atividade antifúngica e atividade antiparasitária (BASER, 2008). Portanto, buscou-se produzir 8 sistemas de NPs, variando a o teor de surfactante, o número de camadas de revestimento (monocamada e bicamada) e o tipo de revestimento externo (GA ou GC).
Material e métodos
Os polímeros utilizados na produção das partículas foram a quitosana, (Grau de desacetilação: 72%), goma arábica (Dinâmica) e goma do chichá. Como agente reticulante, foi utilizado o Tripolifosfato de Sódio (TPF) (Dinâmica). O Tween 80 (Dinâmica) fui utilizado como surfactante. O carvacrol (Sigma Aldrich) fornecido pelo Laboratório de Doenças Parasitárias (LABODOPAR). As NPs foram caracterizadas quanto a eficiência de encapsulamento, FTIR, e perfil de liberação. A cinética de liberação foi determinada através da análise das amostras in vitro por um período de 72 h. As alíquotas foram analisadas no espectrofotômetro UV-Vis Genesys10S (ThermoScientific) no comprimento de onda de 276 nm, a fim de quantificar o carvacrol liberado. O pH ácido foi escolhido, buscando simular o pH estomacal, visando aplicações biomédicas posteriores. O processo de obtenção das NPs foi adaptado do método de complexação polieletrolítica, descrito por Abreu (2008). Em um frasco foi adicionada a solução de QUI 1%, o surfactante Tween 80 e o carvacrol, a fim de obter uma emulsão. A mistura foi levada ao banho ultrassônico. Em seguida adicionou-se, a solução de TPF 0,1 mol/L, formando o pré-núcleo das NPs. A mistura foi mantida sob agitação, posteriormente, adicionou-se o revestimento das partículas (GA ou GC). A amostra foi centrifugada o sobrenadante foi descartado. Para formação da segunda camada, as partículas foram dispersas novamente em água destilada e levadas ao agitador magnético, adicionou-se a solução de QUI 1% m/v. Após, adicionou-se a solução de revestimento. Completando assim a segunda camada de revestimento. As amostras foram centrifugadas a 4000 rpm e o sobrenadante foi descartado. As partículas foram secas por liofilização.
Resultado e discussão
As NPs de 1 a 4 (monocamada) obtiveram um rendimento médio de 62,9%,
enquanto as NPs de 5 a 8 (bicamada) obtiveram um rendimento médio inferior,
com uma média de 56,5%. A diminuição no rendimento ocorre devido ao aumento
das perdas de material durante a produção da segunda camada de revestimento
da NP. As NPs 1 e 2 (baixo teor de tween e monocamada) alcançaram um melhor
percentual de eficiência de encapsulamento, com uma média de 19 %. As NPs de
3 à 6 obtiveram uma média de 12,9 %. Já as NPs 7 e 8 (alto teor de tween e
bicamada) obtiveram os menores percentuais de encapsulamento de carvacrol,
com uma média de 3,8 %. Os sistemas em monocamada alcançaram uma maior
eficiência de encapsulamento de carvacrol, podendo ser justificado pela alta
volatilidade do óleo. Portanto, as NPs em bicamada precisam de mais tempo de
processo, e pelo carvacrol ser muito volátil, sua evasão é favorecida. A
avaliação do encapsulamento mostrou que o aumento no teor de tween e no
número de camadas ocasiona uma menor eficiência de encapsulamento. Foram
selecionados as NPs 1 e 2 para caracterização. Todos os picos
característicos dos constituíntes aparecem nos espectros de NPs no mesmo
número de onda indicando nenhuma modificação ou interação entre as
nanopartículas com carvacrol e quitosana (HOSSEINI et al, 2013). Para
finalizar a caracterização das NPs 1 e 2, foi feito um estudo de liberação
em meio aquoso com HCl e pH ajustado para 3,0. As NPs 1, liberaram em torno
de 30% do óleo liberado em 72 h, enquanto as NPs 2 liberaram em torno de 55%
do óleo em 72 h. A grande diferença em termos de liberação pode ser
explicada por uma repulsão entre as cargas negativas presentes nas cadeias
da GC e do TPF presente no núcleo, fazendo com que a camada de revestimento
seja desfeita com mais facilidade.
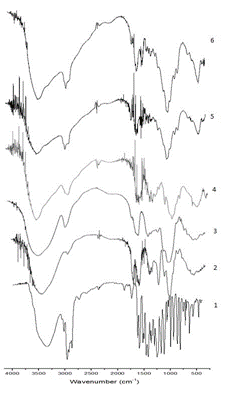
Espectros na região do infravermelho: (1): Carvacrol; (2): GC; (3): GA; (4): QUI; (5): NP 2 - GC/0,1 mL/MC e (6): NP 1 - GA/0,1 mL/ MC
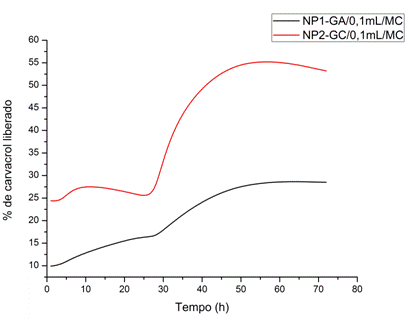
Cinética de liberação in vitro em pH 3,0
Conclusões
Foram produzidas NPs para o encapsulamento do carvacrol e avaliou-se suas características. Constatou-se que o número de camadas influencia no rendimento e na eficiência de encapsulamento do carvacrol. As NPs 1 e 2, apresentaram as bandas características dos constituintes no FTIR. Quanto a liberação in vitro em pH ácido, as NPs apresentaram perfil controlado, entretanto, a NP 1 mostrou-se mais eficiente na retenção do óleo. Por fim, as NPs à base de QUI apresentaram um bom conjunto de características para o encapsulamento e liberação de carvacrol visando aplicações farmacêuticas e biomédicas.
Agradecimentos
UECE, CNPq, aos laboratórios LAQAM e LABODOPAR e a central analítica UFRGS
Referências
ABREU, F.O.M.S. Síntese e caracterização de hidrogéis biodegradáveis à base de quitosana com morfologia controlada com potencial aplicação como carreadores de fármacos, in depto de materiais. 2008. 198f. Tese (Doutorado em Engenharia de Materiais) - Escola de Engenharia Porto Alegre, Universidade Federal do Rio Grande do Sul, Rio Grande do Sul, 2008.
BASER, K.H.C. Biological and pharmacological activies of carvacrol and carvacrol bearing essential oils. Current Pharmaceutical Design, v. 14, p. 3106-3120, 2008.
CLEMENTE-NAPIMOGA, J.T.; MOREIRA, J.A.; GRILLO, R.; MELO, N.F.S.; FRACETO, L.F.; NAPIMOGA, M.H. 15d-PGJ2-loaded in nanocapsules enhance the antinociceptive properties into rat temporomandibular hypernociception. Life Sciences, v. 90, p. 944-949, 2012.
HOSSEINI, S.F.; ZANDI, M.; REZAEI, M.; FARAHMANDGHAVI, F. Two-step method for encapsulation of oregano essential oil in chitosan nanoparticles: Preparation, characterization and in vitro release study. Carbohydrate Polymers, v. 95, p. 50-56, 2013.
IMBROGNO, A.; DRAGOSAVAC, M. M.; PIACENTINI, E.; VLADISAVLJEVIĆ, G. T.; R.G. HOLDICH, R. G.; GIORNO, L. Polycaprolactone multicore-matrix particle for the simultaneous encapsulation of hydrophilic and hydrophobic compounds produced by membrane emulsification and solvent diffusion processes. Colloids and Surfaces B: Biointerfaces, v. 135, p. 116-125, 2015.











