Uso de UPLC-ESI-QTOF-MS/MS na Identificação de Alcaloides Indólicos Monoterpênicos de Espécies do Gênero Psychotria.
ISBN 978-85-85905-23-1
Área
Produtos Naturais
Autores
de Carvalho Junior, A.R. (IFSC) ; Hahn Pacheco, Y. (IFSC) ; Fernandes Cunha, V. (IFSC) ; Ferreira, R.O. (UFT) ; Marques Canuto, K. (EMBRAPA) ; de Carvalho, M.G. (UFRRJ) ; Braz-filho, R. (UENF E UFRRJ) ; Curcino Vieira, I.J. (UENF)
Resumo
O gênero Psychotria (Rubiaceae) é considerado uma potencial fonte de alcaloides indólicos monoterpênicos (AIMs) que são marcadores quimiotaxonômicos do subgênero Heterosychotria. No ponto de vista biológico, alcaloides têm apresentado diversos resultados promissores, os colocando em destaque em pesquisas voltadas à busca de novos possíveis fármacos. O objetivo deste trabalho foi identificar AIMs de folhas de três espécies do gênero por (UPLC-ESI-QTOF-MS/MS). Estrictosidina (1), 5-carboxi- estrictosidina (2), 5-carboxi-3,4-dehidro-estrictosidina (3), vincosamida (4), 5-carboxi-vincosamida (5), 5-carboxi-5,6-dehidrovincosamida (6), 10- hidroxi-vincosamida (7) e lialosídeo (8) foram identificados de P. nuda e ácido-N-Glicopiranosil-3,4-dehidroestrictosidínico (9), composto 7, ácido l
Palavras chaves
PSYCHOTRIA; ALCALOIDES; UPLC-ESI-QTOF-MS/MS
Introdução
A família Rubiaceae compreende mais de 600 gêneros, que totalizam aproximadamente 13000 espécies, distribuídas pelo mundo (RYDIN et al., 2009) (BARBHUIYA et al., 2014). O gênero Psychotria é o maior da família, possuindo mais de 2000 exemplares encontrados principalmente em regiões tropicais e subtropicais (MARQUES DE OLIVEIRA; et al., 2013). Com base em características morfológicas e distribuição geográfica, o gênero Psychotria é dividido em três subgêneros: Psychotria (pantropical), Heteropsychotria (espéciesneotropicais) e, Tetramerae, encontradas na Africa e Madagascar (MORAES et al., 2011). Os alcaloides indólicos monoterpênicos são considerados marcadores quimiotaxonômicos do subgênero Heteropsychotria (espécies encontradas no Brasil) e estudos têm apontado que estes metabólitos apresentam atividades biológicas como anticancerígena, antimalárica (O’CONNOR; MARESH, 2006), analgésica (BOTH et al., 2002), etc. Devido à importância destes metabólitos, neste estudo objetivou-se identificar AIMs presentes nas espécies P. nuda (Cham & Schltdl) Wawra, P. leiocarpa Cham & Schltdl e P. suterella Müll.Arg, utilizando cromatografia líquida de alta performance acoplada a espectrometria de massa de alta resolução (UPLC-ESI-QTOF-MS/MS).
Material e métodos
Coleta do Material Vegetal e Preparo do Extrato As espécies P. nuda, P. leiocarpa e P. suterella foram coletadas na Reserva Biológica do Tinguá, Nova Iguaçu-RJ, (autorização n° 52722). Os extratos em metanol das folhas foram obtidos por maceração de 20 g de cada material e foram, posteriormente, submetidos a extração em fase sólida (SPE), eluídos com solução metanol:água (9:1). Análise Cromatográfica A cromatografia ocorreu num sistema Acquity UPLC (Waters), acoplado a um sistema de Quadrupolo/Tempo de Voo (Qtof, Waters) da EMBRAPA (Fortaleza-CE). As corridas cromatográficas aconteceram em coluna Waters Acquity UPLC BEH (150 x 2,1 mm, 1,7 um), T fixa de 40 °C, fases móveis água com 0,1% de ácido fórmico (A) e acetronitrila com 0,1% de ácido fórmico (B), variando de 2% a 95% de B (15 minutos), fluxo de 0,4 mL/min e volume de injeção de 5 µL. Condições do Espectrômetro de massa de Alta Resolução O modo ESI+ foi adiquirido na faixa de 110-1180 Da, T da fonte fixa a 120 °C, T de dessolvatação 350 °C, fluxo do gás de dessolvatação de 500 L/h, cone de extração de 0,5 V, voltagem capilar de 3,2 kV.
Resultado e discussão
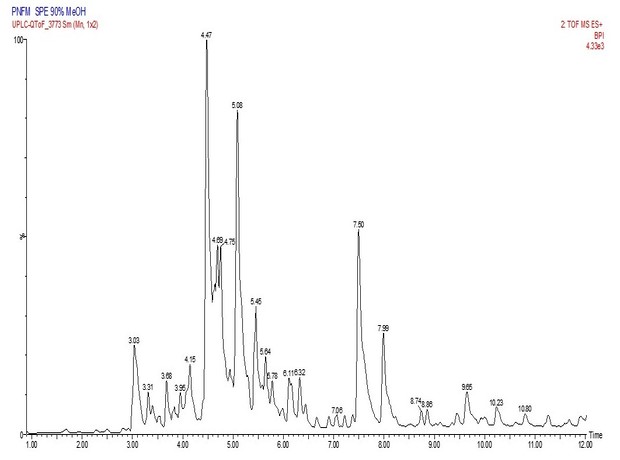
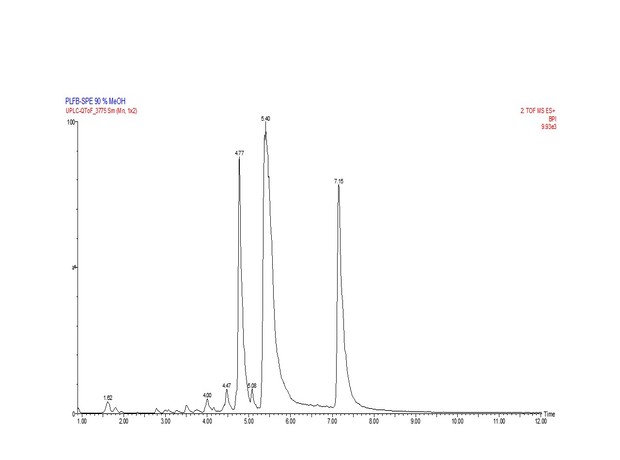
A identificação dos compostos foi realizada com base nos espectros de massas
obtidos no modo positivo (os cromatogramas são apresentados nas Figuras 1a e
1b). A estratégia adota foi comparar os espectros de massa observados com o
esperado para a estrictosidina (1) que é o precursor dos AIMs. Levou-se em
consideração, também, as principais características no ponto de vista da
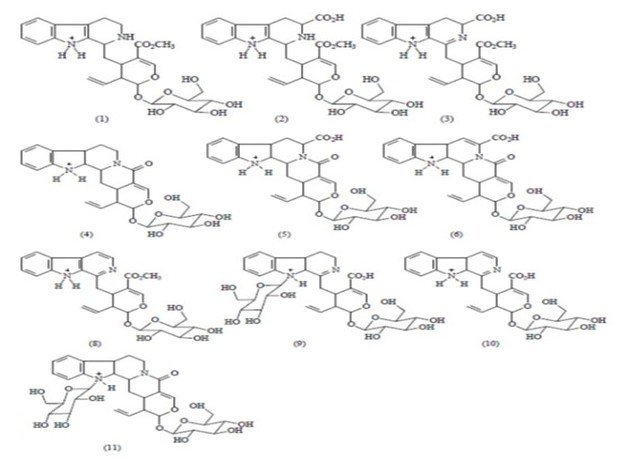
biossíntese de alcaloides do gênero (CARVALHO JUNIOR et al., 2017). Dentre
os compostos identificados, o composto 8, presente na P. leiocarpa, é
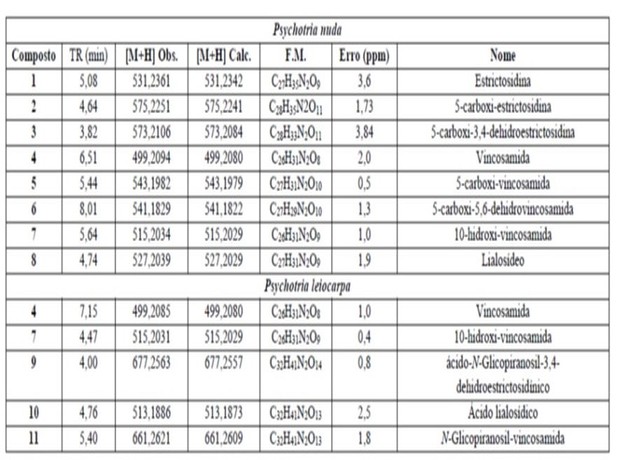
relatado pela primeira vez na literatura (Figura 2, Tabela1). Os espectros
de massas, em geral, apresentaram características que confirmam presença de
glicose, oriunda da secologanina (perda de 162 Da). O espectro de massas do
composto 9 ([M+H] = 677,2563) mostrou picos que caracterizam uma segunda
unidade de glicose, provavelmente, ligada ao N-1. Este perfil também foi
observado no caso do composto 11 ([M+H] = 661,2621), isolado anteriormente
desta espécie (HENRIQUES et al., 2004).
Conclusões
A identificação de AIMs traz mais informações relevantes ao conhecimento da química do gênero. Dentre os compostos identificados, o composto 9 está sendo relatado pela primeira vez na literatura e a presença da glicose em N-1 pode ser corroborada pela identificação do composto 11, que apresenta a mesma característica.
Agradecimentos
Ao CNPq, CAPPES e FAPERJ.
Referências
BARBHUIYA, H. A.; DUTTA, B. K.; DAS, A. K.; BAISHYA, A. K. The family Rubiaceae in southern Assam with special reference to endemic and rediscovered plant taxa. Journal of Threatened Taxa, [s.l.], v. 6, no April, p. 5649–5659, 2014.
BOTH, FERNANDA L.; KERBER, VITOR A.; HENRIQUES, AMÉLIA T.; ELISABETSKY, E. Analgesic Properties of Umbellatine from Psychotria umbellata. Pharmaceutical Biology, [s.l.], v. 40, p. 336–341, 2002.
CARVALHO JUNIOR, A. R.; VIEIRA, I. J. C.; DE CARVALHO, M. G.; BRAZ-FILHO, R.; LIMA, M. A. S.; FERREIRA, R. O. JOSÉ MARIA, E. DE OLIVEIRA, D. B. et al. 13C-NMR spectral data of alkaloids isolated from psychotria species (Rubiaceae). Molecules, [s.l.], v. 22, no 1, p., 2017.
MARQUES DE OLIVEIRA, A.; LYRA LEMOS, R. P.; CONSERVA, L. M. β-Carboline alkaloids from Psychotria barbiflora DC. (Rubiaceae). Biochemical Systematics and Ecology, [s.l.], v. 50, p. 339–341, 2013.
MORAES, T. M. DA S.; DE ARAUJO, M. H.; BERNARDES, N. R.; DE OLIVEIRA, D. B.; LASUNSKAIA, E. B.; MUZITANO, M. F.; DA CUNHA, M. Antimycobacterial Activity and Alkaloid Prospection of Psychotria Species ( Rubiaceae ) from the Brazilian Atlantic Rainforest. Planta medica, [s.l.], v. 77, p. 964–970,
O’CONNOR, S. E.; MARESH, J. J. Chemistry and biology of monoterpene indole alkaloid biosynthesis. Natural product reports, [s.l.], v. 23, no 4, p. 532–547, 2006.
RYDIN, C.; KAINULAINEN, K.; RAZAFIMANDIMBISON, S. G.; SMEDMARK, J. E. E.; BREMER, B.. Deep divergences in the coffee family and the systematic position of Acranthera. Plant Systematics and Evolution, [s.l.], v. 278, no 1–2, p. 101–123, 2009.











