ÁREA: IC-Iniciação Científica
TÍTULO: ESTUDO DE METODOLOGIAS DE OXIGENAÇÃO DO MONOTERPENO CARVONA: PREPARAÇÃO DE MODELOS DE α-METILENO-γ-BUTIROLACTONAS.
AUTORES: R. C. SALLES*; R.B.DOS SANTOS
DEPARTAMENTO DE QUíMICA, UNIVERSIDADE FEDERAL DO ESPíRITO SANTO - UFES, AV. FERNANDO FERRARI, 514, CEP: 29 075-910, VITóRIA, ES.
BETASALLES84@YAHOO.COM.BR
RESUMO: Neste trabalho estudaram-se metodologias de oxigenações estereosseletivas do monoterpeno carvona na tentativa de obtenção de intermediários na preparação de modelos de α-metileno-γ-butiro-lactona. Nesse sentido, reação de epoxidação da carvona com H2O2 em meio alcalino, seguido de cloração alílica com Ca(OCl)2 em água, obteve-se a 10-cloro-epoxicarvona; substituição nucleofílica com íons AcO- em DMF seguido de redução estereosseletiva da C=O com o sistema NaBH4/CeCl3 levou à formação do epóxi-álcool com funcionalidade efetiva no carbono C-10 do derivado da carvona. Alternativamente, outra rota de síntese foi testada, utilizando o cetal-epoxicarvona. A tentativa de cloração alílica de C-10 desse derivado levou à formação inesperada de uma cloroidrina.
PALAVRAS CHAVES: carvona, α-metileno-γ-butirolactona, monoterpeno.
INTRODUÇÃO: As α-metileno-γ-butirolactonas têm sido amplamente estudadas devido as suas atividades biológicas, como, por exemplo: atividade citotóxica e anti-tumor, inibição de crescimento de micróbios, ação tóxica em vertebrados, ação quimioprofilática em esquitossomose e inibição do crescimento de plantas. Além das pesquisas de isolamento, elucidação estrutural e ensaios biológicos, há um grande interesse em estudos sintéticos relacionados muitas vezes com a complexidade estrutural apresentada por essa classe de compostos (DOS SANTOS, 1995).
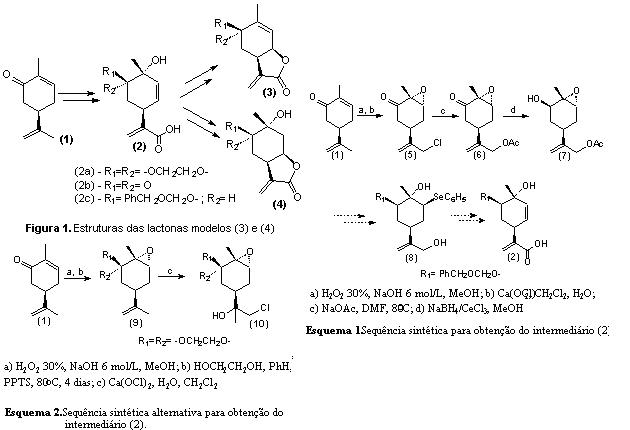
Uma das linhas de pesquisa do nosso laboratório se baseia no aproveitamento de monoterpenos naturais e abundantes isolados de óleos essenciais brasileiros. E, dentro dessa filosofia, fixou-se a atenção em (R)-(-)-carvona (1) como matéria prima para a síntese dos intermediários, compostos (2), de α-metileno-γ-butirolactonas (3) e (4), Figura 1.
O objetivo principal deste trabalho é desenvolver metodologias de funcionalidades (oxigenações) estereosseletivas nos carbonos 1 e 5 do monoterpeno carvona (1) que levem a intermediários precursores das lactonas citadas e de outros monoterpenos oxigenados.
MATERIAL E MÉTODOS: Todas as reações foram realizadas sob agitação magnética à temperatura ambiente ou sob aquecimento (quando indicado). Os solventes utilizados eram de grau técnico e foram purificados por destilação antes do uso. As reações foram acompanhadas por cromatografia em camada delgada, utilizando sílica gel como fase estacionária e também por cromatografia gasosa. Os produtos das reações foram purificados por cromatografia em coluna. Todos os compostos foram analisados por infravermelho e por ressonância nuclear magnética de hidrogênio e carbono 13.
RESULTADOS E DISCUSSÃO: Neste trabalho relatamos nossos resultados preliminares na preparação de intermediários que levem à síntese de modelos de α-metileno-γ-butiro-lactona segundo as metodologias a seguir, Esquemas 1 e 2.
Reação de epoxidação químio e estereosseletiva da carvona (1) com H2O2 30% em meio básico (LINDQUIST, 1985), seguida de cloração alílica com Ca(OCl)2 em água (WOLINSKY, 1982), forneceu a 10-cloro-epoxicarvona (5) em 70% de rendimento nas duas etapas. Substituição nucleofílica com íons AcO- levou ao 10-acetato-epoxicarvona (6) em 90% de rendimento com a funcionalidade efetiva no carbono C-10 do derivado da carvona. Redução da C=O do composto (6) com o sistema NaBH4/CeCl3 (LUCHE, 1978) forneceu estereosseletivamente o álcool (7) em 80% de rendimento, Esquema 1.
Alternativamente, outra rota foi estudada, Esquema 2. Reação de cetalização da epóxicarvona com etileno glicol, PPTS em benzeno, forneceu o cetal (9) em 70% de rendimento. A tentativa de cloração alílica do composto (9) com Ca(OCl)2, levou à formação da cloroidrina (10) em rendimento de 60%. ESQUEMA 2
CONCLUSÕES: Os resultados observados são bastante promissores. Algumas reações merecem um melhor estudo a fim de otimização de rendimentos. A partir dos resultados obtidos, Esquema 1, proteção do grupo OH do álcool (7) com BOM-Cl, seguido de abertura da função epóxido com PhSeNa gerado sob CTF em meio alcalino, oxidação da hidroxila alílica ao nível de ácido carboxílico e posterior desselenilação oxidativa levaria ao composto chave (2), precursor das lactonas terpênicas.
A tentativa de eliminação da hidroxila terciária da cloroidrina (10), Esquema 2, está sob investigação.
AGRADECIMENTOS:Symrise Perfumes e Aromas Ltda pela generosa doação de monoterpeno carvona.
REFERÊNCIAS BIBLIOGRÁFICA:DOS SANTOS, R. B., Tese de Doutorado, UFSCar, 1995 e referências ali citadas.
LINDQUIST, N., et. al.; Phytochemistry, 24, 863, (1985).
LUCHE, J. L.; J. C. S. Chem. Comm., 601-602, (1978).
WOLINSKY, J.; HEGDE, S. G.; J. Org. Chem., 47, 3148, (1982).
