ÁREA: Química Analítica
TÍTULO: DETERMINAÇÃO DE NI(II) UTILIZANDO UM NOVO REAGENTE DERIVADO DE L-DOPA
AUTORES: PROENçA, M.V.B-UEL; SOARES, M. F.-UEL; SCARMINIO, I.S.-UEL; BARRETO, S. R. G.-UEL; BARRETO, W. J.-UEL
DEPARTAMENTO DE QUíMICA, UNIVERSIDADE ESTADUAL DE LONDRINA, 86061-061, LONDRINA, PR. (BARRETO@UEL.BR)
RESUMO: RESUMO: A oxidação da L-Dopa em meio aquoso na presença de Na2S2O3 produziu um composto com absorção em 290 e 330 nm. O composto complexa-se rapidamente com Ni(II) presente em solução aquosa, pH 7,5, temperatura de 25º C e no tempo de 30 minutos, com aparecimento de coloração azul intensa com máximo de absorção em 590 nm. A melhor condição de reação foi estabelecida com o auxílio de planejamento fatorial de 2*4 (temperatura, pH, tempo de reação e concentração de níquel) e depois refinado com 2*3 (concentração de niquel, pH e tempo de reação). A curva de calibração mostrou que a lei de Beer é obedecida no intervalo de concentração de 3,53 10-5 mol.L-1 a 1,80 10-4 mol.L-1 de Ni(II), com R=0,9951.
PALAVRAS CHAVES: palavras chaves: l-dopa, níquel, espectrofotometria uv-vis
INTRODUÇÃO: INTRODUÇÃO: O níquel é liberado no meio ambiente por fontes naturais que são as poeiras sopradas pelos ventos, vulcões, vegetação e o spray marinho, e as antropogênicas destacando-se as aplicações industriais, como a produção de aço, incineração de resíduos, mineração e refino do níquel e vários processos de combustão. Devido a essas utilizações industriais, a quantidade de metais pesados no meio ambiente vêm aumentando, sendo necessário o desenvolvimento de métodos confiáveis, rápidos e sensíveis para a determinação deles em amostras ambientais e biológicas. Os complexos de níquel podem ser encontrados nas geometrias quadrado-planar, octaédrica e tetraédrica, apresentando a variação de seu número de oxidação de (1-) a (4+) e sua química sendo predominada pelo estado de oxidação (2+). O produto da oxidação da L-Dopa com oxigênio é um composto do tipo dioxoleno, que pode se coordenar com um metal em três tipos de estados de oxidação; catecolato (2-), semiquinona (1-) e quinona (0) (BARRETO et al., 1999, 2005). O objetivo deste trabalho foi desenvolver um método espectrofotométrico para a determinação de Ni(II) utilizando L-Dopa oxidada como reagente cromóforo.
MATERIAL E MÉTODOS: MATERIAIS E MÉTODOS: A solução de L-Dopa oxidada (reagente cromóforo) foi produzida a partir da dissolução de 0,313g de Na2S2O3 seguida pela adição de 0,100 g de L-Dopa em 500 mL de água ultrapura, mantida sob agitação constante e fluxo de O2 (0,5 L.min-1) por 48h. O tempo de oxidação da L-dopa foi otimizado medindo as absorvâncias de soluções contendo 5 mL da solução de L-Dopa oxidada e 5 mL de solução de NiCl2 1,11.10-4 mol.L-1 à 25° C e pH 7,0 em tampão KH2PO4/NaOH. As medidas foram realizadas em um espectrofotômetro Milton Roy modelo Genesys II. Para determinar as melhores condições da reação de complexação entre níquel e L-Dopa oxidada, foram utilizados dois planejamentos fatoriais, um preliminar de 24 (temperatura, pH, tempo de reação e concentração de níquel) e em seguida um de ajuste final de 23 (tempo de reação, pH e concentração de níquel) (BARROS NETO et al. 1995; BRUNS et al. 2006). Os pH foram ajustados com soluções tampões de KH2PO4 / NaOH de pH 5,8; 6,0; 6,5; 7,0; 7,5; 8,0; e pH 8,5 e 9,2 a partir de soluções de H3BO3 0,1 Mol.L-1, KCl 0,1 Mol.L-1 e NaOH 0,1 Mol.L-1. A solução contendo o reagente se manteve estável por pelo menos 10 dias a 4 °C .
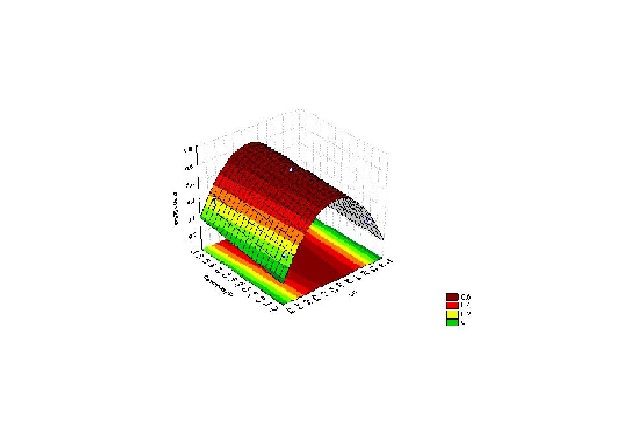
RESULTADOS E DISCUSSÃO: RESULTADOS E DISCUSSÃO: O reagente cromofórico preparado através da oxidação da L-dopa em meio aquoso neutro foi estabilizado devido à presença do tiossulfato de sódio presente na solução. O composto formado é uma semiquinona que apresenta bandas em 290 e 332 nm, não apresentando bandas na região do visível. Quando este composto reagiu com Ni(II) em solução aquosa apareceu uma banda intensa de transferência de carga em 590 nm. Verificou-se através dos planejamentos fatoriais (Figura 1) que a reação é fortemente dependente do pH e concentração de Ni(II) e em menor grau do tempo e temperatura de reação. Deste modo a condição ótima para determinação de Ni(II) em solução aquosa, foi conseguida em pH 7,5, 25 °C e 30 minutos de reação. O intervalo de concentração para obtenção da curva de calibração foi de 3,53. 10-5 mol.L-1 à 1,80. 10-4 mol. L-1. A curva de calibração média (n= 4) obtida foi Y= -0,09507 + 3927,37 X com R= 0,9951.
CONCLUSÕES: CONCLUSÃO: Foi obtido um novo composto reagente para determinação de níquel espectrofotometricamente. Foi caracterizado como uma semiquinona e obtido através da oxidação de L-dopa por O2 durante 48 horas em meio aquoso com tiossulfato de sódio em pH neutro. O método não necessitou de processos de extração com solvente, desenvolvendo coloração à temperatura ambiente após 30 minutos de reação e determinou níquel até 2 ppm.
AGRADECIMENTOS:AGRADECIMENTOS: Os autores agradecem ao CNPq, Fundação Araucária e FAEPE-UEL pelos auxílios financeiros recebidos.
REFERÊNCIAS BIBLIOGRÁFICA:REFERÊNCIAS BIBLIOGRÁFICAS:
1- BARRETO, W. J.; PONZONI, S. A Raman and UV-Vis study os catecholamines oxidized with Mn(III). Spectrochimica Acta, Holanda, 55, 65-72, 1999.
2- BARRETO, W. J. ; BARRETO, S. R.G.; PONZONI, S.; KAWANO, Y.; Di MAURO, E.; MAGOSSO, H. A.; SILVA, W. P. Preparation and characterization of a stable semiquinone-iron complex. Monatshefte Für Chemie, Vienna, 136, 5, 701-712, 2005.
3- BARROS NETO, B. ; SCARMINIO, I. S., I ; BRUNS, R. E. . Planejamento e Otimização de Experimentos. 2. ed. UNICAMP - Campinas: UNICAMP, 1995. v. 1. 299 p.
4-BRUNS, Roy e ; SCARMINIO, I. S.; B NETO, Benício de . Statiscal Design - Chemometrics. Amsterdam: Elsevier, 2006. 412 p.
