ÁREA: Iniciação Científica
TÍTULO: SÍNTESE E CARACTERIZAÇÃO DE SILICATOS DE CÁLCIO
AUTORES: SOARES, J. L. (UMC) ; RODRIGUES, F. A. (UMC)
RESUMO: Silicatos de cálcio apresentam grande interesse do ponto de vista científico e tecnológico devido à sua ampla utilização, podendo variar desde cimentos a catalisadores. Diversos aspectos ligados ao polimorfismo e a natureza das fases e transições de silicatos de cálcio ainda não estão suficientemente esclarecidos. Nossa proposta é o estudo das condições de síntese de Ca2SiO4, silicato dicálcico. Um método de síntese foi desenvolvido com o objetivo de preparar este material; a síntese foi acompanhada por análise térmica diferencial e espectroscopia vibracional na região do infravermelho.
PALAVRAS CHAVES: materiais, síntese, dopagem.
INTRODUÇÃO: A ocorrência de compostos do silício na natureza (LIEBAU, 1985) se estende desde a poeira cósmica, meteoritos, planetas do nosso sistema solar e nas estruturas geológicas da Terra até os seres vivos como nas bactérias, nas cadeias alimentares e no homem. A identificação do silício na natureza permite descrever a evolução do sistema solar, dos planetas e da Terra. Embora ocupe o mesmo grupo do carbono na Tabela Periódica, o silício apresenta diferenças com relação às ligações que estabelece entre os demais elementos. Métodos tradicionais de obtenção de silicatos são baseados em reações no estado sólido, envolvendo temperaturas da ordem de 1400-1500ºC. A adição de estabilizantes de fase, como cloreto de bário pode-se reduzir a temperatura da síntese. Outro aspecto relevante ligado à estrutura dos silicatos é a utilização de dopantes, que podem alterar de forma expressiva sua reatividade e propriedades físicas. Neste trabalho foi estudada a síntese de β-Ca2SiO4 utilizando os respectivos óxidos como materiais de partida. Comparativamente foram estudados silicatos de cálcio dopados com cobre, cádmio e zinco. O efeito da adição de dopantes pode ser avaliado através de métodos termoanalíticos (MACKENZIE, 1970). Também foram descritos aspectos termodinâmicos ligados ao processo de síntese (SELBY et al., 1966; DEHOFF, 1993).
MATERIAL E MÉTODOS: Foram utilizados sílica gel 60 (70-230 Mesh) (Aldrich Chemical) e óxido de cálcio P.A. 95% (Nuclear). Os sólidos foram pesados estequiometricamente de forma a manter uma relação Ca/Si =2. A estes sólidos foi adicionada água deionizada, de forma a obter dispersões com relação água: sólidos de 116:1 [m/m]. As dispersões foram mantidas em agitação magnética por 60 minutos e depois tratadas em banho de ultra-som (Thornton, 25 kHz) por 60 minutos, à temperatura ambiente. Durante a agitação magnética foi medido o pH das soluções. As soluções foram transferidas para placas de Petri e secas em estufa. Os sólidos obtidos desta maneira foram moídos de forma a se obter partículas com tamanho máximo de 90 m. A seguir os sólidos foram analisados por análise térmica diferencial (DTA, Perkin-Elmer, Pyris 7), sob atmosfera inerte e taxa de aquecimento de 40oC por minuto. O método de dopagem seguiu o mesmo feito para a preparação do silicato de cálcio tendo como diferença as massas dos reagentes pesados não sendo medido o pH das soluções. Foram utilizados para a dopagem os seguintes reagentes: óxido de cádmio PA (Vetec), óxido de cobre PA (Merck) e óxido de zinco PA (Acros Organics).
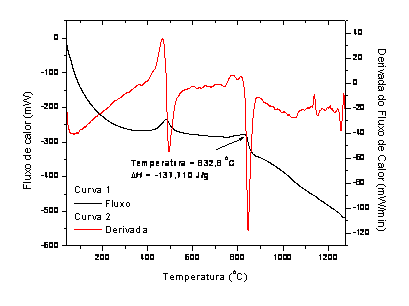
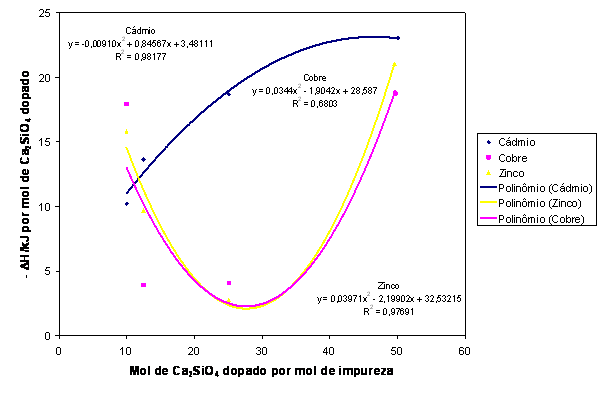
RESULTADOS E DISCUSSÃO: Os termogramas de DTA indicam que a etapa final da síntese de β-Ca2SiO4 ocorre por volta de 830-835oC e envolve uma variação de entalpia da ordem de -137,710 J/g, de acordo com o Gráfico 1. Em relação à síntese de óxido de cálcio com sílica gel, os valores médios de entalpia apresentaram valores inferiores para os casos dessa síntese dopada com cobre, zinco e cádmio. Dopagens de 1, 2, 4 e 5% para o cádmio apresentaram padrões de curva semelhantes (termogramas) enquanto que para o cobre e zinco, as dopagens 1 e 5% apresentaram padrões de curva diferentes das dopagens 2 e 4%, mas semelhantes ao cádmio. As curvas de derivada que se seguem nos termogramas são as derivadas das curvas de fluxo de calor em relação ao tempo e não à temperatura. O fato é que a taxa de aquecimento não é constante, isto é, a variação do tempo de aquecimento não é linear com a variação de temperatura. O Gráfico 2 é o calor integral de formação, isto é, quando um soluto como CdO, CuO ou ZnO é dissolvido em silicato de cálcio por substituição de átomos de cálcio por impureza o calor de formação tende a um valor limite, supondo que a reação foi completa.
CONCLUSÕES: A temperatura e a variação de entalpia de síntese são influenciadas pelo grau de substituição de átomos de cálcio por impurezas e também pela diferença entre os raios iônicos dos hetero-átomos. Todas as sínteses são reações exotérmicas.
AGRADECIMENTOS: FAPESP (2006/00792-0) e UMC
REFERÊNCIAS BIBLIOGRÁFICA: LIEBAU, F. Structural Chemistry of Silicates Structure, Bonding and Classification. 1985. Springer-Verlag: 1-6, 14.
MACKENZIE, R. C. Differential Themal Analysis Volume 1: Fundamental Aspects. 1970. Academic Press: 587.
SELBY, S. M; WEAST, R. C. Handbook of Chemistry and Physics. 1966. The Chemical Rubber: D-32.
DEHOFF, R. T. Thermodynamics in Materials Science. 1993. McGraw Hill series in materiais science and engineering: 40.
