ÁREA: Produtos Naturais
TÍTULO: Estudo Fitoquímico dos Frutos de Byrsonima crassifolia (L.) Kunth (murici)
AUTORES: ALMEIDA, M.M.B. (UFC) ; TAVARES, L. C. (UFC) ; BEZERRA, F. S. (UFC) ; SOUZA, J. S. N. (UFC) ; MACHADO, L. L. (UFC) ; LEMOS, T.L.G. (UFC)
RESUMO: Byrsonima crassifolia (Malpighiaceae), conhecida popularmente como murici é encontrado nas regiões norte e nordeste brasileiro. Este trabalho descreve os resultados de estudos fitoquímicos dos frutos de B. crassifolia do Ceará. O fracionamento cromatográfico do extrato etanólico da polpa dos frutos de murici permitiu a identificação de mistura com 23% de ácidos graxos (ácidos palmítico e linoléico) e 77% de ésteres (palmitato, linoleato e oleato de metila), bem como de uma mistura de ácido ursólico e oleanólico; enquanto que o extrato metanólico levou ao isolamento da quercetina. Embora essas substâncias sejam comuns no gênero Byrsonima, esse é o primeiro registro de isolamento de metabólitos secundários na porção comestível da espécie frutífera Byrsonima crassifolia (L.) Kunth.
PALAVRAS CHAVES: byrsonima crassifolia, frutas tropicais, quercetina
INTRODUÇÃO: O Brasil tem uma grande variedade de frutas que apresentam o sabor exótico, tendo assim um grande potencial econômico. Byrsonima crassifolia, L. (murici) é encontrado nas regiões norte e nordeste brasileiro, tendo fruto de forma arredondada, coloração alaranjada, e sendo consumido principalmente na forma de sucos, doces e licores (SANNOMIYA et al., 2005). Pertence a família Malpighiaceae que compreende 60 gêneros e 1200 espécies (JOLY, 1977). Várias espécies do gênero Byrsonima são conhecidas pela utilização de seus frutos na alimentação, como também pelo seu uso com fins medicinais (FIGUEIREDO et al, 2005). Estudos dos extratos das raízes e troncos da espécie B.crassifolia tem demonstrado possuir atividades antimicrobiana, tripanomicida e antiespasmódica (SANNOMIYA et al., 2005). No entanto, poucas espécies pertencentes a esse gênero foram quimicamente estudadas. Investigações fitoquímicas de B. verbascifolia, B. microphylla e B. crassa revelaram a ocorrência, em troncos e folhas, de triterpenos, flavanóides, éster aromático, naftoquinonas e amentoflavona (GOTTLIEB et al., 1975; MENDES et al., 1999; SANNOMIYA et al., 2004). Estudos sobre B. crassifolia relataram o isolamento de glicolipídeos, triterpenos, ácidos triterpênicos, catequinas e flavonóides das folhas (RASTRELLI et al., 1997, BEJAR, et al.,1995) e, proantocianidinas e taninos do tronco (GEISS et al., 1995), enquanto que dos frutos (polpa) não há nenhum registro de substâncias isoladas, exceto de compostos voláteis responsáveis pelo seu aroma (REZENDE e FRAGA, 2003; ALVES e FRANCO, 2003). Dando continuidade ao estudo fitoquímico de espécies frutíferas do estado do Ceará, este trabalho descreve os resultados obtidos com o isolamento de substâncias da polpa de Byrsonima crassifolia.
MATERIAL E MÉTODOS: Os frutos frescos de Byrsonima crassifolia (L.) Kunth (murici) foram coletados nas proximidades da cidade de Fortaleza Ceará em outubro de 2006 e processados para separação da polpa. A espécie foi taxonomicamente identificada pelo Prof. Dr. Edson Paula Nunes e sua exicata encontra-se depositada no Herbário Prisco Beserra da Universidade Federal do Ceará.
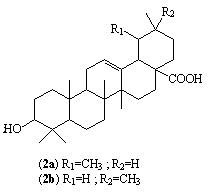
O extrato etanólico da polpa do murici foi submetido a uma partição líquido-líquido com hexano, diclorometano, acetato de etila e n-butanol. A fração hexânica resultante (500 mg) foi submetida à coluna cromatográfica sobre gel de sílica, usando como eluentes hexano, misturas hexano/diclorometano, diclorometano/acetato e acetato/metanol com aumento da polaridade. As frações obtidas foram comparadas por CCD e aquelas que apresentavam comportamentos semelhantes foram reunidas. As frações eluídas com hexano/diclorometano (6:4) foram reagrupadas e submetidas a sucessivas cromatografias em gel de sílica, levando ao isolamento de 17 mg de uma mistura de ésteres e ácidos graxos (MUR-1). Da fração obtida com diclorometano/acetato na proporção 9:1 resultou uma mistura binária de ácido ursólico (2a) e ácido oleanólico (2b), denominada MUR-2 (77 mg). Para melhor identificação dessa mistura, realizou-se uma derivatização através de reação de acetilação, na qual o MUR-2 foi misturado com anidrido acético e piridina, na proporção 2:1 e traços de DMAP (dimetilaminopiridina), obtendo-se o seu derivado acetilado.
O extrato metanólico, após evaporação do solvente, foi particionado em uma mistura de acetato de etila e água (1:1, v/v). Da fração acetato de etila, após cromatografia em sílica gel e consecutivas colunas sephadex LH-20, empregando metanol como eluente, obteve-se 6 mg da substância pura denominada MUR-3.
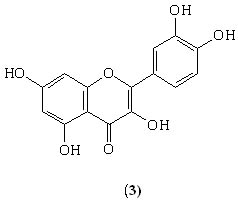
RESULTADOS E DISCUSSÃO: O fracionamento da porção hexânica do extrato etanólico da polpa de B. crassifolia resultou no isolamento de MUR-1, solúvel em CHCl3 e que, embora apresentasse uma única mancha em CCD, constatou-se tratar-se de uma mistura de 5 constituintes: palmitato de metila, linoleato de metila, oleato de metila, ácido palmítico e ácido linoléico. Sua identificação foi realizada por meio de RMN e principalmente CG-MS, através da comparação dos tempos de retenção com dados disponíveis na espectroteca, comparação dos espectros de massa com o dos padrões da Supelco® e dados da literatura. MUR-2 solúvel em piridina foi identificado como uma mistura de ácido ursólico (2a) e oleanólico (2b). A fração AcOEt do extrato metanólico levou ao isolamento de MUR -3, cristais amarelos, solúveis em MeOH e identificado como a quercetina (3). Para a elucidação estrutural dessas substâncias foram utilizadas técnicas de IV, EM, RMN e comparação com dados da literatura.
Estes resultados corroboram com estudos já realizados de B. crassifólia (BEJAR, et al.,1995) e com outras espécies de Byrsonima, onde foram detectadas essas mesmas classes de metabólitos secundários em folhas (SANNOMIYA et al., 2004 e FIGUEIREDO et al, 2005).
Vários estudos têm atribuído aos flavonóides efeitos benéficos a saúde. A quercetina, conhecida como antioxidante, possui várias outras atividades como inibição do crescimento de muitas células neoplásicas (MIDDLETON et al., 2000), atividade espasmogênica (BEJAR et al.,1995), antidiarréica ( FIGUEIREDO et al, 2005), etc.
Os ácido ursólico e oleanólico são reportados como detentores de interessantes bioatividades como anti-HIV, citotóxica (MA et al., 2005), agente tripanossomicida (LEITE et al., 2001), antiinflamatória e hapatoprotetora (LIU, 1995).
CONCLUSÕES: Investigações fitoquímicas da polpa de murici do Ceará apresentaram constituintes pertencentes à classe dos triterpenos (mistura de ácido ursólico e ácido oleanólico) e a dos flavonóides (quercetina), importantes por apresentarem diversas atividades biológicas. Foi isolado também uma mistura com 23% de ácidos graxos (ácido palmítico e linoléico) e 77% de ésteres (palmitato, linoleato e oleato de metila). Embora essas substâncias sejam comuns no gênero Byrsonima, esse é o primeiro registro de isolamento de metabólitos secundários na porção comestível da espécie frutífera Byrsonima crassifólia
AGRADECIMENTOS: Aos órgãos de fomento CNPq, CAPES e FUNCAP.
REFERÊNCIAS BIBLIOGRÁFICA: ALVES, G. L.; FRANCO, M. R. B. 2003. Headspace gas chromatographymass spectrometry of volatile compounds in murici (Byrsonima crassifolia L. Rich). Journal of Chromatography A, 985: 297301.
BEJAR, E.; AMARQUAYE, A.; CHE, C. T.; MALONE, M. H.; FONG, H. H. S. 1995. Constituents of Byrsonima crassifolia and their spasmogenic activity. International Journal of Pharmacognosy, 33: 25-32.
FIGUEIREDO, M. E.; MICHELIN, D. C.; SANNOMIYA, M.; SILVA, M. A.; SANTOS, L.; ALMEIDA, L. F. R.; BRITO, A. R. M. S.; SALGADO, H. R. N.; VILEGAS, W. 2005. Avaliação química e da atividade antidiarréica das folhas de Byrsonima cinera DC. (Malpighiaceae). Revista Brasileira de Ciências Farmacêuticas, 41: 79 -83.
GEISS, F.; HEINRICH, M.; HUNKLER, D.; RIMPLER, H. 1995. Proanthocyanidins with (+)- epicatechin units from Byrsonima crassifolia bark. Phytochemistry, 39: 635-643.
GOTTLIEB, O. R.; HENRIQUES MENDES, P.; TAVEIRA MAGALHÃES, M. 1975. Triterpenoids from Byrsonima verbascifolia. Phytochemistry, 14: 1456-1456.
JOLY, A. B. 1977. Botânica Introdução à taxonomia vegetal. 4 ed. São Paulo: Cia Editora Nacional, 777 p.
LEITE, J. P. V.; LOMBARDI, J. A.; CHIARI, E.; OLIVEIRA, A. B. 2001. Isolamento biomonitorado de uma substância tripanossomicida de Arrabidaea triplinervia (Bignoniaceae), o ácido ursólico. Revista Brasileira de Farmacognosia, 11: 77-87.
LIU, J. 1995. Pharmacology of oleanolic acid and ursolic acid (Review article). Journal of Ethnopharmacology, 49: 57-68.
MA, C-M.; CAI, S-Q.; CUI, J-R.; WANG, R-Q.; TU, P-F.; HATORRI, M.; DANESHTALAB, M. 2005. The cytotoxic activity of ursolic acid derivatives. European Journal of Medicinal Chemistry, 40: 582-589.
MENDES, C. C.; CRUZ, F. G.; DAVID, J. M.; NASCIMENTO, I. P.; DAVID, J. P. 1999. Triterpenes esterified with fatty acid and triterpene acids isolated from Byrsonima microphylla. Química Nova, 22: 185- 188.
MIDDLETON JR, E.; KANDASWAMI, C.; THEOHARIDES, T. C. 2000. The effects of plant flavonoids on mammalian cells: Implications for inflammation, heart disease and cancer. Pharmacological Reviews, 52: 673-751.
RASTRELLI, L.; DETOMMASI, N.; BERGER, I.; CACERES, A.; SARAVIA, A.; DE SIMONE, F. 1997. Glycolipids from Byrsonima crassifolia. Phytochemistry, 45: 647-650.
REZENDE, C. M.; FRAGA, S. R. G.. 2003. Chemical and Aroma Determination of the Pulp and Seeds of Murici (Byrsonima crassifolia L.). Journal of the Brazilian Chemical Society, 14: 425-428.
SANNOMIYA, M.; RODRIGUES, C. M.; COELHO, R.G.; SANTOS, L. C.; HIRUMA-LIMA, C.A.; BRITO, A.R. M. S.; VILEGAS, W. 2004. Application of preparative high-speed counter-current chromatography for the separation of flavonoids from the leaves of Byrsonima crassa Niedenzu (IK). Journal of Chromatography A, 1035: 4751.
SANNOMIYA, M.; FONSECA, V. B.; SILVA, M .A.; ROCHA, L.R.M.; SANTOS, L. C.; HIRUMA-LIMA, C.A.; BRITO, A. R. M. S.; VILEGAS, W. 2005. Flavonoids and antiulcerogenic activity from Byrsonima crassa leaves extracts. Journal of Chromatography A, 985: 297301.
