ÁREA: Iniciação Científica
TÍTULO: Estudo da estabilização das antocianinas presentes no jambolão utilizando biopolímeros
AUTORES: CARVALHO,R.R.V. (UFBA) ; FALCÃO,T.M.B. (UFBA) ; SILVA,C.P. (UFBA) ; BAHIA,M.V. (UFBA) ; MIRANDA,J.A. (UFBA)
RESUMO: O presente trabalho teve por objetivo avaliar a estabilidade de antocianinas do extrato bruto purificado do jambolão na presença de soluções de carboximetilcelulose e de amilopectina em diferentes proporções do biopolímero. A extração das antocianinas foi realizada em meio aquoso, utilizando a proporção 1:3 de massa em gramas de casca da fruta por volume em mL de água, por 12 horas a 25ºC. O teor de antocianinas foi determinado espectrofotometricamente pelo método do pH diferencial. Os testes de estabilidade basearam-se no acompanhamento das variações nas absorvâncias nos máximos de absorção das antocianinas por um período de 72 horas, sob diferentes condições: pH, e presença de luz. Os resultados obtidos evidenciaram uma significativa estabilização das antocianinas em soluções
PALAVRAS CHAVES: antocianinas; jambolão; biopolímeros
INTRODUÇÃO: Antocianinas são pigmentos naturais responsáveis pelas colorações vermelha, azul e púrpura de uma grande variedade de flores e frutos [1]. Pertencem à família dos flavonóides, compostos polifenólicos cujas propriedades biológicas vêm sendo extensamente descritas na literatura [2]. Campos e colaboradores [3] extraíram e identificaram antocianinas do jambolão (Syzygium cuminii), planta tipicamente brasileira, com interesse no estudo de suas propriedades biológicas. Este trabalho teve como objetivo avaliar a capacidade de estabilização de antocianinas extraídas de jambolão, em soluções de biopolímeros derivados de amido e celulose.
MATERIAL E MÉTODOS: Os extratos obtidos emergindo as casca das frutas, por 12 horas a 25 ºC, em água na proporção 1:3 (massa de casca / volume de solvente). Em seguida, o teor de antocianinas foi quantificado pelo método do pH diferencial descrito por Fuleki e Francis [4]. Alíquotas de 50 mL de extrato aquoso contendo antocianinas foram diluídas em balões volumétricos de 10 mL contendo soluções de pH 1,0 e pH 4,5. A seguir, foram feitas medidas espectrofotométricas a 510 e 700 nm. Em seguida, o extrato bruto foi purificado por meio da técnica de extração em fase sólida com cartucho C18. A estabilidade das antocianinas do extrato purificado foi avaliada para soluções preparadas na presença de carboximetilcelulose de grau alimentício/Plury Química e em soluções contendo amilopectina de batata, em diferentes concentrações de biopolímero (0,1%; 0,5%; 1,0%; 1,5%, 2,0% m/v), a pH 4,0; 7,0 e 9,0, na presença e ausência de luz.A absorvância nos máximos de absorção foram monitoradas durante um período de 72 horas, foi estipulado um tempo de meia vida correspondente a redução do valor de absorvância inicial como referência da estabilidade do composto.
RESULTADOS E DISCUSSÃO: Os extratos com concentração de antocianinas totais igual a 0,6±0,2 g L-1 (1,3±0,4 mmol L-1), foram obtidos por imersão das cascas de jambolão em água na proporção 1:3 (m/v), sendo possível confirmar a presença de pelo menos quatro compostos: delfinifina-3-glicosídeo, cianidina-3-galactosídeo, petunidina-3-galactosídeo e pelargonidina-3- arabinosídeo, seguindo o mesmo procedimento descrito por Campos e colaboradores [3]. Neste trabalho, não houve a preocupação em separar as antocianinas, uma vez que o interesse inicial foi verificar a eficiência de sua estabilização na presença dos biopolímeros.
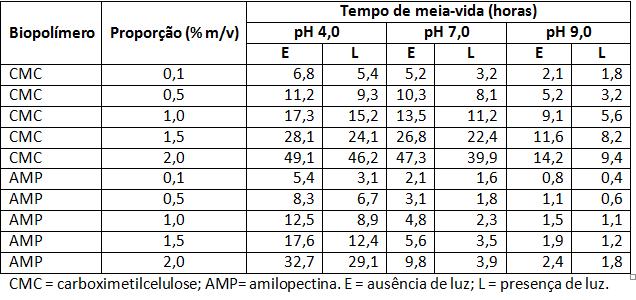
As soluções de biopolímero mostraram-se eficientes quanto à estabilização das antocianinas. Os resultados podem ser acompanhados na tabela 1.
Tabela 1 Tempo de meia-vida das soluções das antocianinas na presença de biopolímeros, em diferentes condições experimentais.
Os maiores tempos de meia-vida foram obtidos para as soluções em carboximetilcelulose. É possível verificar a dependência da estabilidade das antocianinas em relação ao pH do meio, condição já bastante discutida na literatura. Contudo, pode notar que há uma significativa estabilização dos compostos mesmo em pH neutro. Ensaios baseados na utilização de matrizes sólidas serão testados, sobretudo aqueles relacionados à preparação de microesferas poliméricas baseadas nestes biopolímeros, visando a estabilização destas antocianinas. Apesar da estabilidade ainda ser consideravelmente baixa em relação às necessidades da indústria de alimentos, os biopolímeros mostraram-se promissores.
CONCLUSÕES: Os melhores resultados para a estabilização das antocianinas foram obtidos para as soluções de carboximetilcelulose. A boa estabilização obtida em pH neutro, sugere possibilidades quanto a sua utilização pela indústria alimentícia.
AGRADECIMENTOS:
REFERÊNCIAS BIBLIOGRÁFICA: 1 - CLIFFORD, M. N. Chlorogenic acids and other cinnamates-nature, occurrence. J. Sc. Food and Agriculture 80,1033, 2000.
2 - KONG, J. M.; CHIA, L.; GOH, N.; CHIA, T.; BROUILLARD, R. Analysis and biological activities of anthocyanins. Phytochemistry. 64, 923, 2003.
3 - Campos, D. D. P. Extração, purificação e isolamento de antocianinas de jambolão e avaliação dos seus efeitos biológicos (Syzygium cuminii). Dissertação de Mestrado, Instituto de Química, Universidade Estadual de Campinas, SP, 2006.
4 - Terci, D.B.L. Aspectos analíticos e didáticos de antocianinas extraídas de frutas. Tese de Doutorado, Instituto de Química, Universidade Estadual de Campinas, SP, 2004.
