ÁREA: Química Analítica
TÍTULO: COMPORTAMENTO VOLTAMÉTRICO DO OCTA(3-AMINOPROPIL)OCTASILSESQUIOXANO ANCORADO NA SUPERFÍCIE DA SÍLICA GEL MODIFICADA COM HEXACIANOFERRATO DE COBRE
AUTORES: GABRIEL JUNIOR, S. (UNESP) ; SÁ, A. C. (UNESP) ; DO CARMO, D. R. (UNESP)
RESUMO: O silsesquioxano octa(3-aminopropil)octasilsesquioxano foi ancorado na superfície da 3-cloropropil sílica gel e modificado com hexacianoferato de cobre. Os espectros de FTIR e a voltametria cíclica comprovaram o sucesso na formação do complexo binuclear. O voltamograma do CuHCFAPS exibiu dois pares redox com potenciais médios (Em); (Em)1= 0,29 V e (Em)2= 0,72 V vs Ag/AgCl, atribuídos aos processos redox Cu(I)/Cu(II) e Fe(II)(CN)5NO / Fe(III)(CN)5NO, respectivamente. Observou-se que em diferentes concentrações do eletrólito de suporte os Em1 e Em2 foram deslocados para regiões mais anódicas. A performance voltamétrica não foi alterada com a variação de pH (8,0 - 2,0). O eletrodo modificado com pasta de grafite apresentou uma boa estabilidade eletroquímica e uma excelente reprodutibilidade.
PALAVRAS CHAVES: hexacianoferrato de cobre, (3-aminopropil)octasilsesquioxano, voltametria cíclica.
INTRODUÇÃO: Eletroquimicamente, o hexacianoferrato de cobre (CuHCF) apresenta características especiais devido a capacidade de exibir reações redox em diferentes eletrólitos de suporte como K+, Na+, Li+, NH4+. Podem-se aumentar as atividades eletrocatalíticas deste composto quando reagido com materiais nanoestruturados, visto que estes apresentam uma elevada área superficial, podendo aumentar a sensibilidade do eletrodo modificado (BAIONI et al., 2008). Uma das principais vantagens dos eletrodos quimicamente modificados (EQMs) é a sua capacidade em mediar a oxidação de algumas espécies que exibem elevado potencial em eletrodos convencionais, aumentando assim sua sensibilidade e seletividade de resposta no que se refere ao substrato investigado (CARMO, 2003). O objetivo deste trabalho foi preparar o material nanoestruturado (3-aminopropil)octasilsesquioxano, ancorá-lo na superfície da 3-cloropropil sílica gel para depois reagir este material primeiro com íons cúpricos e depois com hexacianoferrato de potássio, formando assim, o complexo binuclear hexacianoferrato de cobre na superfície da 3-cloropropil sílica gel. A substância supracitada foi escolhida por apresentar uma boa estabilidade eletroquímica e habilidades para funcionar como mediadores de elétrons na eletrocatálise de algumas substâncias de interesse biológico como, por exemplo, ácido ascórbico, n-acetilcisteína, dopamina estabelecendo assim, um sistema eletroanalítico para detecção destas importantes substâncias.
MATERIAL E MÉTODOS: para o ancoramento do (3-aminopropil)octasilses- quioxano cerca de 5,0 g de 3-cloropropil sílica gel foi adicionada em 1,0 g do silsesquioxano dissolvido em 25 mL de metanol. A suspensão foi mantida em refluxo por 48h. A fase sólida obtida foi separada, devidamente empacotada e lavada com metanol por 48 h em um sistema de Soxhlet. Em seguida o material foi seco a 80 ºC e, por questão de brevidade, foi chamado de APS. Após a secagem, 1,0 g do APS obtido foi imerso em 25 mL de uma solução de íons Cu2+ 1,0x10-3 molL-1 onde foram agitados por 30 minutos à temperatura ambiente. A fase sólida foi então filtrada e lavada com água bidestilada. Após exaustiva lavagem, o material foi adicionado a uma solução de ferrocianeto de potássio 1,0x10-3 molL-1. Lavou-se o material resultante com bastante água bidestilada. O composto obtido, descrito como CuHCFAPS, foi seco a 80°C e estocado em dessecador à vacuo. O CuHCFAPS foi caracterizado por espectroscopia vibracional utilizando-se um espectrofotômetro Nicolet 5DXB FTIR (Nicolet Instruments, Madison, WI) com um mínimo de 64 "varreduras" para cada amostra numa resolução de ± 4 cm-1. A técnica eletroquímica utilizada nestes estudos foi a voltametria cíclica. Os voltamogramas cíclicos foram realizados em um potenciostato da Microquímica (MQPG-01) em uma escala variando de -0,1 a 1,2 V (vs Ag/AgCl). Para estas medidas, utilizou-se um sistema contendo três eletrodos: eletrodo de pasta de grafite modificada (diâmetro interno de 0,5 mm) 20% m/m com 50 microlitros de Nujol como eletrodo de trabalho, eletrodo de referência (Ag/AgCl) e eletrodo auxiliar de platina.
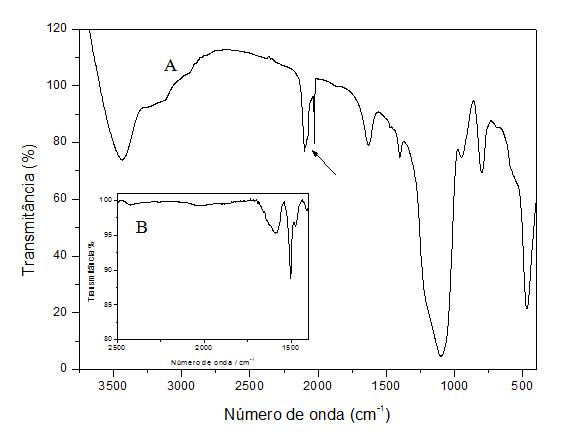
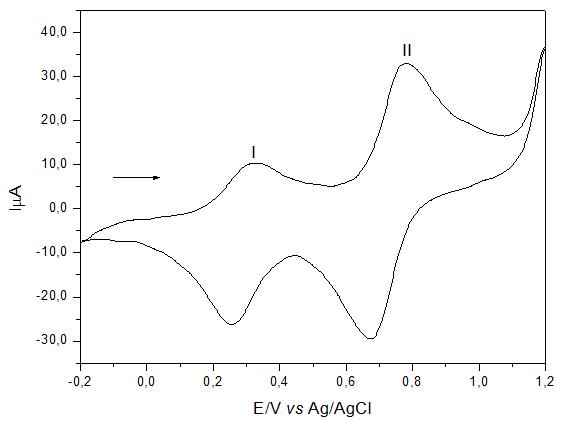
RESULTADOS E DISCUSSÃO: O espectro na região do infravermelho do compósito obtido (CuHCFAPS ) exibiu uma freqüência em 2090 cm-1, apresentado pela seta na Figura 1A, atribuído ao estiramento simétrico(C tripla N) característico do hexacianoferrato de cobre (LOOS-NESKOVIC et al., 2004) quando comparado com o espectro do APS ilustrado na Figura 1B. O voltamograma cíclico do CuHCFAPS exibiu dois pares redox (Figura 2) com potenciais médios (Em); (Em)1= 0,29 V e (Em)2= 0,72 V vs Ag/AgCl, atribuídos aos processos redox Cu(I)/Cu(II) e Fe(II)(CN)5NO / Fe(III)(CN)5NO, respectivamente. Quando o material é submetido a diferentes velocidades de varredura (10 a 100 mVs-1) observou-se para o processo redox Fe(II)/Fe(III), uma dependência linear entre a corrente do pico anódico/catódico e a raiz quadrada da velocidade de varredura, o que caracteriza um processo adsortivo (BARD, 1980). A natureza dos cátions afetou os Em e as intensidades de corrente, deslocando os potenciais médios (Em)2 para potenciais mais positivos, seguindo a ordem: NH4+>K+>Na+>Li+, pois o tamanho do raio dos cátions hidratados são fatores que governam a seletividade deste processo redox (BAIONI, 2008). Já a natureza dos ânions (Cl-, NO3-, SO42-, ClO4-), praticamente não afetam o processo redox dos picos I e II. Os experimentos realizados em diferentes concentrações de KCl (0,01 2,0 mol L-1) resultaram em um deslocamento dos potenciais (Em)1 e (Em)2 para regiões mais positivas (anódicas) à medida que a concentração do eletrólito foi aumentada. Foi verificado, também, que com a variação da concentração hidrogeniônica pH( 8,0 a 2,0), os dois processos redox permaneceram praticamente inalterados.
CONCLUSÕES: O complexo binuclear CuHCFAPS pode ser preparado na superfície da 3-cloropropil sílica gel em duas etapas. O material formado (CuHCFAPS), foi caracterizado por infravermelho(FTIR) que indicou a presença do estiramento simétrico(C tripla N) característico do hexacianoferrato de cobre (CuHCF) . O voltamograma cíclico do CuHCFAPS exibiu dois pares redox com potenciais médios (Em); (Em)1= 0,29 V e (Em)2= 0,72 V vs Ag/AgCl, atribuídos aos processos redox Cu(I)/Cu(II) e Fe(II)(CN)5NO / Fe(III)(CN)5NO, respectivamente. A natureza dos cátions e os pH afetam o Em e as intensidades de corrente.
AGRADECIMENTOS: Fapesp
REFERÊNCIAS BIBLIOGRÁFICA: BAIONI, A. P.; VIDOTTI, M.; FIORITO, P. A.; TORRESI, S. I. C. 2008. Copper hexacyanoferrate nanoparticles modified electrodes: A versatile tool for biosensors. Journal Electroanalytical Chemistry,622: 219-224.
BARD, A. J.; FAULKNER, L. R. Electrochemical Methods, New York: Wiley, 1980. p.196.
CARMO, D. R. DO; SILVA, R. M. DA; STRADIOTTO, N. R. 2003. Electrocatalytic and voltammetric determination of sulfhydryl compounds through iron nitroprusside modified graphite paste electrode. Journal Brazilian Chemistry Society,14: 616-620.
LOOS-NESKOVIC, C.; AYRAULT, S.; BADILLO, V.; JIMENEZ, B.; GARNIER, E.; FEDOROFF, M.; JONES, D. J.; MERINOV, B. 2004. Structure of copper-potassium hexacyanoferrate (II) and sorption mechanisms of cesium. Journal of Solid State Chemistry,177: 1817-1828.
