ÁREA: Química Orgânica
TÍTULO: Estudos sobre a ciclização espontânea de aciltiossemicarbazidas potencialmente bioativas
AUTORES: DE QUEIROZ, A. P. A. (UNICAP) ; ALVES, T. H. O. (UFPE) ; DE ALMEIDA, Y. M. B. (UFPE) ; MALVESTITI, I. (UFPE) ; DOS SANTOS FILHO, J. M. (UFPE)
RESUMO: Anéis heterocíclicos e cadeias heterogêneas têm sido identificados como grupos farmacofóricos essenciais à resposta biológica. Sendo o anel 1,2,4-oxadiazólico um dos heterociclos de maior interesse no planejamento de novas substâncias potencialmente bioativas, estudos anteriores nesse grupo de pesquisa utilizaram a abordagem bioisostérica de hibridação molecular para associá-lo à cadeia da aciltiossemicarbazida por meio de ligação direta entre eles. Os derivados 1,2,4-oxadiazol-aciltiossemicarbazida obtidos sofreram ciclização espontânea, dando o anel 1,3,4-oxadiazol. Novos análogos dessa classe foram planejados, introduzindo um espaçador etilênico entre os grupos farmacofóricos, a fim de estabelecer a natureza dessa reação e sua dependência da ligação direta entre os grupos envolvidos.
PALAVRAS CHAVES: 1,2,4-oxadiazol, ciclização espontânea de tiossemicarbazida, atividade biológica
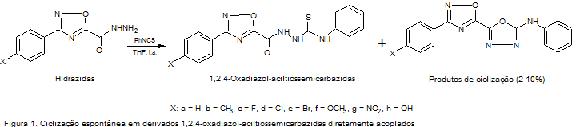
INTRODUÇÃO: Drogas anti-inflamatórias não-estereoidais (NSAIDs) têm sido amplamente empregadas no tratamento de dor, febre e doenças inflamatórias, em especial artrite reumatóide, sendo a busca por elas um campo de pesquisa intenso. Com base no planejamento bioisostérico por hibridação molecular, nosso grupo tem estudado o efeito da associação das porções 1,2,4-oxadiazol e aciltiossemicarbazida na síntese de compostos potencialmente bioativos e recentemente identificou que a ligação direta entre esses dois farmacóforos leva à reação de ciclização espontânea da aciltiossemicarbazida acoplada ao anel 1,2,4-oxadiazólico. Durante a adição de isotiocianato de fenila às hidrazidas de partida, tetarciclicos com anéis 1,2,4- e 1,3,4-oxadiazólicos diretamente ligados entre si foram obtidos como produtos secundários (Fig. 1). Esses resultados foram publicados recentemente[1], sendo proposto um mecanismo de ciclização dependente de fatores eletrônicos exercidos pelo anel 1,2,4-oxadiazol-5-aril-substituído sobre a carbonila da cadeia aciltiossemicarbazida dos derivados estudados. Estudos teóricos usando cálculos de QTAIM e B3LYP/6-31G no programa GAUSSIAN 98W foram realizados para dar suporte a essa proposta[2].
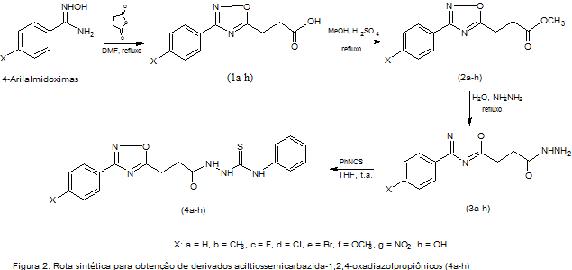
A fim de comprovar experimentalmente as causas da ciclização, planejamos uma série de compostos na qual o anel 1,2,4-oxadiazol e a cadeia aciltiossemicarbazida foram espaçados por um grupo etilênico e conduzimos sua síntese em condições semelhantes às empregadas na obtenção da série original. A rota sintética para a obtenção dos derivados-chave 1,2,4-oxadiazol-5-aril-propionil-hidrazida (1a-h) partiu de aril-amidoximas obtidas rotineiramente em nosso laboratório (Fig. 2). Os novos produtos terão seus perfis de atividade anti-inflamatória e antinociceptiva posteriormente traçados.
MATERIAL E MÉTODOS: Os produtos foram caracterizados por infravermelho (IV) da Perkin Elmer. Análises de ressonância magnética de próton (1H-RMN) foram realizadas a 300 MHz. Os espectrogramas de massa (MS) foram obtidos em equipamento acoplado a espectrógrafo a gás (GC) da Shimadzu. Análises de LCMS (cromatografia líquida acoplada a espectrometria de massas) foram feitas em LCMS-IP-TOF da Shimadzu.
Segundo a Fig. 2, os ácidos 1,2,4-oxadiazolpropiônicos (1a-h) foram obtidos por reação entre 4-arilamidoximas e anidrido succínico sob refluxo em DMF por 3 h e caracterizados por ponto de fusão e TLC. O derivado com X=OH foi caracterizado por técnicas espectroscópicas.
Os ácidos 1,2,4-oxadizolpropiônicos foram convertidos a ésteres metílicos por refluxo em metanol com quantidade catalítica de ácido sulfúrico concentrado. Os derivados 1,2,4-oxadiazolpropianato de metila (2a-h) foram obtidos puros após tratamento da mistura reacional e remoção da fase orgânica em rota-evaporador e devidamente caracterizados. Estes ésteres foram, então, suspendidos em água e uma solução 55% em peso de hidrazina hidrato foi adicionada ao meio reacional. Após refluxo, as hidrazidas (3a-h) formadas permaneceram insolúveis no meio reacional e foram filtradas. Análises de TLC e espectroscópicas indicaram produtos puros.
A síntese das aciltiossemicarbazida-1,2,4-oxadiazolpropiônicas (4a-h) foi realizada inicialmente a temperatura ambiente, sendo as hidrazidas dissolvidas em THF sob nitrogênio. Após a adição de isotiocianato de fenila, controle de TLC indicou a conclusão da reação após 10 min. O solvente foi removido e a mistura reacional bruta foi seca sob vácuo antes de ser analisada por LCMS e 1H-RMN. As aciltiossemicarbazida-1,2,4-oxadiazolpropiônicas foram recristalizadas em etanol e devidamente caracterizadas.
RESULTADOS E DISCUSSÃO: Os resultados da série contendo o anel 1,2,4-oxadiazol diretamente acoplado à aciltiossemicarbazida indicaram o produto ciclizado com rendimentos de 2-10%[1], conforme Fig.1.
A rota sintética para a obtenção dos compostos aciltiossemicarbazida-1,2,4-oxadiazolpropiônicos (4a-h) foi executada com sucesso, sendo as etapas de síntese descritas na Fig.2.
Os derivados 1a-h foram obtidos com redimentos modestos de 38-45%, suscitando estudos para sua otimização. Entre eles, o ácido 1h (X=OH) é produto inédito, sendo completamente caracterizado. A esterificação do grupo ácido, por outro lado, ocorreu sob condições clássicas, levando à série 2a-h com rendimentos excelentes (80-95%), na qual o éster 2h não foi citado na literatura até o momento. O intermediários-chave 1,2,4-oxadiazolpropionil-hidrazida (3a-h) constituem um grupo inédito de substâncias, tendo suas estruturas caracterizadas por técnicas espectroscópicas. Seus rendimentos variaram entre 60 e 85% após isolados por recristalização com etanol-água.
Por fim, a síntese-alvo desse trabalho, sob as condições reacionais empregadas, confirmou a importância do acoplamento direto entre a porção 1,2,4-oxadiazol e a aciltiossemicarbazida. Os produtos brutos das reações de fomação da série aciltiossemicarbazida-1,2,4-oxadiazolpropiônica (4a-h) foram submetidos a análises de LCMS e 1H-RMN e nenhum sinal de derivados oriundos da ciclização do grupo aciltiossemicarbazida foi observado. Também os resultados de TLC foram compatíveis com essa observação, pois a presença do anel 1,3,4-oxadiazol na estrutura levaria a um produto fluorescente ao UV, o que não ocorreu. A purificação dos derivados 4a-h foi realizada por recristalização em etanol, fornecendo os produtos puros como sólidos amorfos brancos e rendimentos entre 65 e 78%.
CONCLUSÕES: A série aciltiossemicarbazida-1,2,4-oxadiazolpropiônica (4a-h), planejada para estudos das propriedades químicas do grupo aciltiossemicarbazida, foi obtida com sucesso, confirmando que o mecanismo de ciclização espontânea da cadeia aberta a 1,3,4-oxadiazol é dependente dos efeitos eletrônicos do anel 1,2,4-oxadiazol. O espaçador etilênico entre os dois grupos farmacofóricos inibiu o processo, de modo que a série 4a-h foi o único produto identificado.
Os novos derivados 3a-h e 4a-h foram caracterizados e devem ser submetidos à avaliação de suas atividades anti-inflamatória e antinociceptiva.
AGRADECIMENTOS: Os autores são gratos à equipe da Central Analítica do Departamento de Química Fundamental da UFPE pelas análises espectroscópicas.
REFERÊNCIAS BIBLIOGRÁFICA: [1] dos Santos Filho, J. M.; de Lima, J. G.; Leite, L. F. C. C. J. Heterocyclic Chem.. 2009, 46, 722.
[2] Oliveira, B. G.; dos Santos Filho, J. M.; de Lima, J. G.; Leite, L. F. C. C., XV Simpósio Brasileiro de Química Teórica, 2009, Poços de Caldas.
