ÁREA: Materiais
TÍTULO: Caracterização de atapulgita de origem amazônica e aplicação em processo de adsorção com chumbo Cinética e termodinâmica de adsorção
AUTORES: SILVA, W.L.L. (UFMT) ; OLIVEIRA, S.P. (UFMT) ; GUERRA, D.J.L. (UFMT) ; VIANA, R.R. (UFMT)
RESUMO: A habilidade deste silicato para remover chumbo (II) em soluções aquosas foi investigada por um série de isotermas de adsorção ajustadas pelos modelos de Langmuir, Temkin, Freundlich e Sips em temperatura ambiente e pH 4,0, considerando a função do erro estatístico, os dados experimentais foram melhor modelados pelo modelo de Langmuir. Os efeitos como pH, concentração do metal e tempo de contato foram estudos usando procedimento de adsorção por batelada. Três modelos cinéticos foram testados, o melhor modelo foi o modelo de Lagergren pseudo-segunda ordem para o sistema estudado. O número máximo de mols adsorvidos foi determinado em 9,90 mmol g-1. Os efeitos energéticos causados pela adsorção do cátion chumbo (II) foram determinados através de metodologia calorimétrica.
PALAVRAS CHAVES: atapulgita, adsorção, chumbo
INTRODUÇÃO: Nos últimos anos, tem-se aumentado consideravelmente a preocupação da sociedade com o meio ambiente. No passado, as indústrias tratavam seus efluentes visando apenas atender a legislação, e atualmente buscam além de reduzir custos diminuindo desperdícios, assegurar uma boa imagem perante os consumidores. As indústrias lançam diariamente ao meio ambiente milhões de toneladas de resíduos sólidos, líquidos e gasosos que são provenientes de seus processos produtivos, onde em sua grande maioria se apresentam nocivos ao ecossistema. Em meio a esses compostos os mais prejudiciais são os de origem química, como os metais pesados (AHARONI, 1991; MARTIN et al., 1999; FONSECA & AIROLDI, 2000; GOSSET et al., 1986 e GUERRA et al., 2006). A adsorção de metais por superfícies minerais é um processo reconhecidamente importante que controla a biodisponibilidade dos metais em ambientes aquáticos (FROST et al., 1997; MING-YUAN et al., 1998; FROST et al., 1999 e MOUSTY, 2004). O tratamento de efluentes contendo metais abrange processos físico-químicos de precipitação, troca iônica, adsorção e extração por solventes, onde o de precipitação é o mais utilizado, no entanto é inadequado para o tratamento de grandes volumes de efluentes. Assim sendo é mais indicado o uso de recursos naturais sem tratamento prévio, como solos argilosos ferruginosos com grande abundancia de substâncias húmicas, e submetidos a tratamentos, como por exemplo, as zeólitas naturais impregnadas com materiais magnéticos e esmectitas pilarizadas com polihidroxicátions de Al, Ti, Si e etc., que se enquadram no grupo de materiais com ampla aplicação em catálise heterogênea e como adsorventes (PEREIRA et 1994; GÁBOR et al., 1995; PADILHA et al., 1997).
MATERIAL E MÉTODOS: A amostra de atapulgita é oriunda da região do estado do Pará (Rio Capim), onde as reservas naturais deste argilomineral são bastante significativas, principalmente devido a fatores climáticos que atuam diretamente em sua formação geológica. A amostra estudada neste trabalho foram provenientes desse depósito que localiza-se a NE do Estado do Pará, entre a rodovia Belém-Brasília (trecho entre Ipixuna do Pará e Mãe do Rio) e o médio curso do Rio Capim. Os estudos de adsorção utilizando o mineral para a remoção do metal divalente de soluções aquosas foram realizados utilizando processo de adsorção em batelada, tendo como variáveis o pH, concentração e tempo. As investigações calorimétricas foram realizadas utilizando um calorímetro isotérmico de marca Thermometric, modelo LKB 2277.
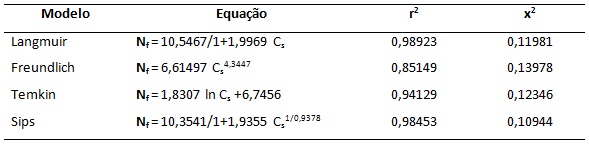
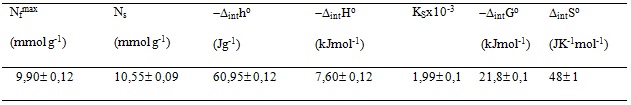
RESULTADOS E DISCUSSÃO: Nos processos de adsorção normalmente prima-se por escolher equações que tenham a característica de ser facilmente linearizáveis e conseqüentemente estimar os parâmetros graficamente (KLUG et al., 1998). Os modelos empregados foram: Langmuir, Freundlich, Temkin e Sips. Os resultados obtidos experimentalmente com o sistema de adsorção ATP/Pb(II), calculados pelo método não-linear são apresentados na Figura- 1, em que é possível observar altos valores de coeficiente de determinação (r2) e coerência nos valores do coeficiente (x2) para os valores teóricos em relação aos valores experimentais. Entre os modelos estudados Langmuir apresentou valor maior do coeficiente de determinação, este dado indica a maior afinidade entre o modelo de Langmuir e o sistema estudado. Com o experimento da variação de concentração foi obtido o valor máximo de adsorção (Nfmax = 9,90 mmol g-1) que na concentração 5,98 mmol dm-3 é estabelecido o equilíbrio da reação de adsorção. Sugerindo que todos os sítios adsortivos presentes na superfície da atapulgita foram preenchidos pelo chumbo.Os valores apresentados conferem características energeticamente favoráveis para as interações da matriz com íons chumbo, de modo que os valores de energia livre e entalpia apresentem-se negativos e os valores do termo entrópico são positivos. Os valores apresentados na Figura-2 mostram que as interações entre os íons chumbo e os centros básicos da atapulgita apresentam-se com valores próximos com a variação de pH. Com isso, os resultados termodinâmicos mostraram que o processo de adsorção pela atapulgita do íon chumbo foi espontâneo. O processo adsortivo foi exotérmico e também foi endoergônico . Assim, este processo adsortivo foi entalpicamente e entropicamente favorável.
CONCLUSÕES: O argilomineral atapulgita utilizado neste trabalho apresentou uma boa capacidade de adsorção do metal divalente chumbo.Em comparação com outros adsorventes naturais e sintéticos, foram obtidos resultados próximos, mas visto que é uma matéria prima natural e de fácil obtenção, apresenta um beneficio significativo do ponto de vista operacional e econômico. As interações com íon chumbo revelaram-se energeticamente favoráveis.Portanto, a discussão sobre os fenômenos envolvidos nas reações e aplicações dos sistemas aqui apresentados, infere na utilização deste mineral no tratamento de efluentes.
AGRADECIMENTOS:
REFERÊNCIAS BIBLIOGRÁFICA: AHARONI C. 1991. Kinetics of soil chemical reactions A theoretical treatment. In: D.L. Sparks, D.L. Suarez (Eds), Rates of soil Chemical Process, Soil of America, Madison, WI, 1:1-18.
FONSECA M.G., AIROLDI C. 2000. New Layered inorganic Organic nanocomposites containing n-propylmercapto copper phyllosilicates. J. Mater. Chem., 10:1457.
FROST R. L., VAN DER GAAST S. J. 1997c. Kaolinite hydroxyls a Raman microscopy study. Clay Minerals, 32:471-484.
FROST R. L., KRISTOF J., PAROZ, G. N., KLOPROGGE, J. T. 1999. Modification of kaolinite surfaces through intercalation with potassium acetate, II. Phys. Chem. Miner., 26:257.
GÁBOR M., TÓTH M., KRISTÓF J., Komáromi-Hiller G. 1995. Synthesis and characterization of silver nanoparticle/kaolinite composites. Clays Clay Miner., 43:223.
GOSSET T., TRANCART J.L., Thevenot D.R. 1986. Batch metal removal by peat: Kinetics and thermodynamics. Water Research, 20:21-26.
GUERRA D.L., LEMOS V.P., ANGÉLICA R.S., AIROLDI C. 2006. Influência da basicidade no processo de pilarização de esmectitas da região amazônica com íon de Keggin, Rev. da Soc. Portuguesa de Materiais, 17:75.
KLUG M., SANCHES M.N.M., LARANJEIRA M.C.M., FÁVERE V.T. 1998. Análise das isotermas de adsorção de Cu(II), Cd(II),Ni(II) e Zi(II) pela N-(3,4-dihidroxibenzil)quitosana empregando o método da regressão não-linear. Química Nova., 21:410-413.
MARTIN A.I., SANCHEZ-CHAVES M., ARRANZ F. 1999. Characterization and controlled release behaviour of adducts from chloroacetylated cellulose and α naphthylacetic acid. React Funct.Polym., 39:179-187.
MING-YUAN H., ZHONGHUI L., ENZE M. 1988. Acidic and hydrocarbon catalytic properties of pillared clay. Catal. Today, 2:321-338.
MOUSTY C. 2004. Sensors and biosensors based on clay-modified electrodes new trends. Applied Clay Science, 27:159-177.
PADILHA P.D., ROCHA J.C., MOREIRA. C., CAMPOS J.T.D. FEDERICI C.D. 1997. Synthesis, Preconcentration of heavy-metals ions from aqueous solutions by means of cellulose phosphate an application in water analysis. Talanta, 45:317.
PEREIRA M.R.FTIR ATR. 1994 Studies on polymer /polymer and polymer/liquid interfaces. Tese de Doutorado. University of Durham.
