ÁREA: Iniciação Científica
TÍTULO: SÍNTESE E CARACTERIZAÇÃO DE NOVOS 3-ARIL-5-PENTIL-1,2,4-OXADIAZÓIS MEDIADA POR FORNO DE MICROONDAS DOMÉSTICO
AUTORES: SOUZA, Z.C (UAG/UFRPE) ; BARROS, C.J.P (DQ/UFRPE) ; FREITAS, J.J.R (DQ/UFRPE) ; FREITAS FILHO, J.R (UAG/UFRPE)
RESUMO: 1,2,4-oxadiazóis são compostos que têm atraído a atenção de muitos pesquisadores devido
à sua ampla gama de atividades biológicas. Além disso, alguns 1,2,4-oxadiazóis também
têm sido utilizados como fungicidas e inseticidas. Neste trabalho descreve-se uma
metodologia potencialmente adaptáveis para a síntese de seis novos 3-aril-5-pentil-
1,2,4-oxadiazóis. A reação foi realizada em forno de microondas doméstico, sem uso de
solvente, com tempo reduzido e em rendimentos de entre 55-73%. As estruturas dos
compostos foram caracterizadas por ressonância magnética nuclear (RMN 1H e 13C),
espectroscópia de infravermelho e análise elementar. Os parâmetros teóricos foram
obtidos por AM1 e ab initio (Hartree-Fock) métodos semi-empíricos.
PALAVRAS CHAVES: 1,2,4-oxadiazol, forno microonda, caracterização, atividade biológica
INTRODUÇÃO: Os 1,2,4 oxadiazóis são compostos cíclicos que apresentam dois heteroátomos de
nitrogênio e um de oxigênio em sua estrutura. Estes heterociclos são bastante
relatados na literatura. Desde os primeiros trabalhos tratando da síntese e das
propriedades biológicas dos oxadiazóis, oito trabalhos de revisão já foram publicados
(CLAPP, 1976). Esses compostos apresentam várias propriedades biológicas entre elas
propriedades farmacológicas. Estes compostos são conhecidos desde 1884 quando os
pesquisadores alemães sintetizaram (TIEMANN e KRÜGER, 1984) o primeiro composto desta
série. As duas revisões das literaturas descritas por CLAPP (1976, 1984) descrevem as
sínteses, a química, as reações, os estudos espectroscópicos e as atividades
biológicas dos 1,2,4-oxadiazóis e 4,5-dihidro-1,2,4-oxadiazóis. Na década de 60,
pelos menos três oxadiazóis, ganharam popularidades como drogas terapêuticas:
oxolamina (BOYER, 1962) e a libexina (ELOY, F.; LENAERS,1966) que apresentam ação
antitussígena, e o irrigor (BOYER, 1962), que tem ações vasodilatadoras das artérias
coronárias e anestésico local. Devido a importância biológica dos 1,2,4-oxadiazóis,
descrita acima o presente trabalho tem como objetivo sintetizar seis novos 3-aril-5-
pentil-1,2,4-oxadiazóis (Ar: fenil, p-toluil, p-metoxifenil, p-clorofenil, p-
bromofenil, p-nitrofenil) mediada por forno de microonda doméstico.
MATERIAL E MÉTODOS: Nas reações, utilizou-se reagentes e solventes, na sua forma comercial, p.a. O
acompanhamento das reações foi feito através de cromatografia em camada delgada
(ccd), onde o solvente usado para correr a placa foi CH2Cl2/AcOEt (9:1). Para
visualização dos compostos usamos lâmpada de ultravioleta e / ou cuba contendo
vapores de iodo. Para cromatografia em coluna utilizamos sílica-gel 60 (Merck, 70
230 mesh). Os espectros de RMN 1H e RMN 13C foram obtidos em espectrofotômetro VARIAN
modelo Unity Plus (300 MHz e 75 MHz), usando CDCl3 como solvente e tetrametilsilano
como padrão interno. Espectros de infravermelho (IV) foram obtidos em
espectrofotômetro de IV com Transformada de Fourier no instrumento BRUKER Modelo IFS
66, em pastilha de KBr. As reações de microondas foram realizadas em forno de
microondas domésticos, marca PANASONIC, modelo NN-5SSBK (220; 900W/2450 MHz). Para
concentrar as soluções orgânicas foram utilizados evaporadores rotatórios do modelo
IKA-WERK operando a pressão reduzida. As estruturas moleculares dos 3-aril-5-pentil-
1,2,4-oxadiazóis (3a-f) foram calculadas ao nível HF usando a basis 6-31G.
Comprimentos e ângulos de ligação bem como os ângulos de torção foram otimizados
inicialmente pelo método semi-empírico AM1[12]. Posteriormente estes resultados foram
utilizados como imput ao método HF/6-31G. Destes cálculos resultaram a energia e o
momento de dipolo para cada composto.
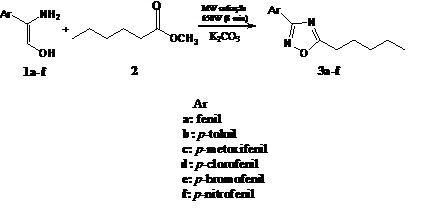
RESULTADOS E DISCUSSÃO: A síntese dos 3-aril-5-pentil-1,2,4-oxadiazóis (3a-f), foi mediada por forno de
microonda doméstico e consistiu em reagir as arilamidoximas (Ar: fenil, p-toluil, p-
clorofenil, p-metoxifenil, p-bromofenil, p-nitrofenil), separadamente, com hexanoato
de metila e K2CO3, sem utilização de solvente (esquema 1). A metodologia empregada
forneceu os produtos rapidamente, com duração de oito minutos, e uma química
ambientalmente limpa. O mecanismo de formação de 3a-f a partir de arilamidoximas,
éster e também de ácidos foi descrito por Srivastava et al (2007).
Esquema 1. Síntese 3-aril-5-pentil-1,2,4-oxadiazóis
As estruturas destes novos compostos foram comprovadas através dos espectros de
infravermelho, de RMN 13C e RMN 1H e análise elementar. Inicialmente, as moléculas
foram examinadas usando os cálculos semi-empíricos com o método AM1, pelo fato de
economia de tempo. O resultado do método semi-empírico mostrou que o anel aromático
está no mesmo plano que o anel heterociclo, em todos os compostos. Energias totais
(ET) e momentos de dipolo (m) para os seis novos 3-aril-5-pentil-1,2,4-oxadiazóis,
3a-f, foram calculados pelos métodos AM1 e HF/6-31G(*). O composto de menor energia
pelo método de AM1, foi o 3c (E=0,008) e o de maior energia foi 3e (E=0,0774). Pelo
método ab initio com base HF/6-31G, o composto de maior energia, também foi o 3e.
CONCLUSÕES: A metodologia utilizada se constituiu num método simples e eficiente para a síntese de
seis novos 3-aril-5-pentil-1,2,4-oxadiazol a partir de diferentes arilamidoximas e o
hexanoato de metila em presença de carbonato de potássio (K2CO3), sem a presença de
solvente, mediada por forno de microonda doméstico. O tempo de reação foi de 8 min e o
rendimento da reação foi de moderado a bom. As estruturas dos compostos foram
caracterizadas por ressonância magnética nuclear (RMN 1H e RMN 13C), espectroscopia de
infravermelho e análise elementar. Ainda, foram feitos cálculos teóricos de 3a-f.
AGRADECIMENTOS: A CAPES pela bolsa de mestra¬do (C. J. P. Barros) e ao CNPq pela bolsa de iniciação
científica (Z. C. Souza, J. J. R. Freitas).
REFERÊNCIAS BIBLIOGRÁFICA: BOYER, J. H. Heterocyclic Compounds (Elderfield, R. C., Ed), Wiley, New York, 1962, 7, 462.
CLAPP, L.B., Advances In Heterocyclic Chemistry, Katritzky, A.R., Ed., Academic Press, New York, 1976, 20, 65
CLAPP, L.B., In Comprehensive Heterocyclic Chemistry, Katritzky, A.R.; Rees, C. W., Eds., Pergamon Press, Oxford, 1984, 6, 365.
ELOY, F.; LENAERS, R. Helv Chim Acta., 1966, 49,1430.
FREITAS, J. J. R.; DE FREITAS, J. C. R.; DA SILVA, L. P. ; DE FREITAS FILHO, J. R.; KIMURA, G. Y.V.; SRIVASTAVA., R. M., Tetrahedron Lett. 48, 6195-6198, 2007.
TIEMANN, F; KRÜGER, P. Ber., 1984, 17, 1685.
