ÁREA: Química Inorgânica
TÍTULO: INVESTIGAÇÃO TERMOGRAVIMÉTRICA E ESPECTROSCÓPICA DO COMPLEXO DIFENIL-4-AMINA SULFONATO DE ZINCO
AUTORES: GOLDNER, S (UFES) ; MACHADO, L. C. (UFES) ; DALTO, F. (UFES) ; CARVALHO, M. A. (UFES) ; MENDES, R. B. (UFES)
RESUMO: O trabalho apresenta a síntese e caracterização do produto da reação do ligante Difenil-4-Amina Sulfonato de Bário com o Sulfato Hepta-hidratado de Zinco. A análise elementar do metal e de CHNS apresentou resultados experimentais próximos aos obtidos teoricamente para o composto [Zn(C12H10NO3S)2.5H2O]. A caracterização espectroscópica por IV mostrou bandas características do ligante sulfonato. As análises termogravimétricas em atmosfera oxidante e inerte mostraram a decomposição total do produto em diferentes temperaturas, conduzindo a um resíduo atribuído ao ZnO. Esta possibilidade foi confirmada por meio das análises dos difratogramas de Raios X. Assim, foi possível propor a seguinte fórmula para o composto: [Zn(C12H10NO3S)2. 5H2O], a reação apresentou rendimento de 78,1%.
PALAVRAS CHAVES: síntese, zinco, sulfonato.
INTRODUÇÃO: O processo de desidratação de metanossulfonatos de Cobalto (II), Cobre (II) e Zinco (II) já foi estudado em atmosfera de nitrogênio por meio de Calorimetria Exploratória Diferencial (DSC) e por Análise Termogravimétrica (TGA), verificando apenas a presença de água de cristalização nesses compostos (WANG at al., 2006). O ligante difenil-4-amina-sulfonato vem sendo utilizado na preparação de complexos metálicos a partir dos respectivos sais de metais alcalinos e alcalinos-terrosos (MACHADO et al., 2009). Quando o centro metálico complexado por esse ligante foi o Ferro, o estado de oxidação deste também foi alterado: de Ferro (III) para Ferro (II) em solução aquosa, a temperatura ambiente e na forma sulfato. O indicativo da ocorrência das reações tem sido demonstrado pela variação intensa de cor (vermelho para azul) e pela precipitação do sulfato de bário (BaSO4).
MATERIAL E MÉTODOS: Primeiro, preparou-se o ligante através da reação entre a difenil- 4- amina sulfonato de Sódio e nitrato de Bário a aproximadamente 70ºC. Então, realizou-se com o ligante e o sulfato de zinco (II) hepta-hidratado, a síntese da difenil- 4- amina sulfonato de Zinco sob atmosfera inerte, em ausência de luz e a aproximadamente 70ºC. Posteriormente, foram feitas análises do composto sintetizado. Os teores de carbono, hidrogênio, nitrogênio e enxofre dos compostos formados nas reações, foram determinados utilizando o instrumento Flash EA 1112 da Thermo. A porcentagem de Zinco foi determinada utilizando o Espectrômetro de Absorção Atômica ZEEnit 700, marca AnalytiK Jena. A caracterização espectroscópica de infravermelho foi obtida nos instrumentos Bomem MB 100 e ABB FTLA2000-102 (scan number = 16, smooth = 60% e linha de base não corrigida) usando pastilha de KBr. As análises termogravimétricas (TGA/DTGA) foram realizadas através do equipamento de análise térmica Shimadzu TGA-51H, com cela de platina, submetida a um fluxo de ar dinâmico ou de nitrogênio purificado, numa vazão de 50mL/minuto em um intervalo de operação correspondente de 0 a 1000ºC (taxa de aquecimento de 10ºC/min). Os difratogramas de Raios X, para os resíduos das análises termogravimétricas, foram feitos em um difratômetro Rigaku Miniflex II equipado com proporcional contador e discriminador de altura de pulso usando radiação CuKα (λ = 1.5418Å).
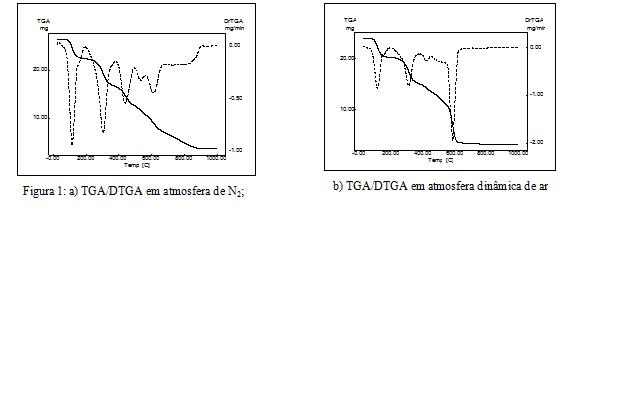
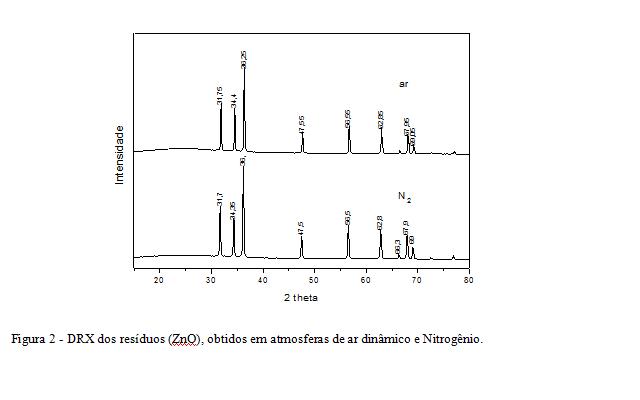
RESULTADOS E DISCUSSÃO: O composto foi caracterizado pela fórmula Zn[(C12H10NO3S)2]5H2O(652,01g/mol): Zn(%)=10,03, Exp.=10,17; C(%)=44,21, Exp.=43,85; H(%)=4,64, Exp.=4,73; N(%)=4,30, Exp.=4,22; S(%)=9,83, Exp.=9,50. O espectro de Infravermelho do produto apresentou bandas características do ligante sulfonato: def. ang. N-H 1591 cm-1, def. axial C-N aromático 1326 cm-1, def. axial M-SO3 [1190, 1128, 1038, 1005] cm-1. As análises termogravimétricas do composto, tanto em atmosfera inerte (figura 1a) quanto oxidante (figura 1b), mostraram a desidratação do produto até uma temperatura de aproximadamente 150 ºC. Em N2, a perda experimental entre 27 e 153 ºC foi de 13,97%; e em atmosfera dinâmica de ar a perda foi de 14,15%, o que corresponde a perda de cinco moléculas de água (13,82%). A partir da desidratação, ocorre a perda da parte orgânica. Em atmosfera inerte a decomposição é mais lenta, ocorrendo em três etapas e terminando apenas a 900ºC. Já em atmosfera oxidante a perda de massa ocorre em duas etapas e se completa a aproximadamente 600 ºC. Nas duas atmosferas, a 1000 ºC, foi encontrado um resíduo branco, com percentual de 13,65% e de 13,01%, para atmosferas inerte e oxidante, respectivamente. Enquanto que o percentual obtido na simulação teórica das perdas, considerando o óxido de zinco (ZnO, 81,38 g/mol) como resíduo, foi de 12,48%. Sendo confirmado pela difratometria de Raios X, figura 2.Portanto, as análises realizadas, confirmaram a fórmula anteriormente sugerida pela análise elementar: [Zn(C12H10NO3S)2.5H2O], ou simplesmente [Zn(DAS)2].5H2O. A reação proposta é a que segue, com rendimento de 78,1%:
1 ZnSO4 . 7H2O (aq) + 1[Ba(DAS)2] (aq) → 1[Zn(DAS)2]. 5H2O (aq) + 1BaSO4 (s)
CONCLUSÕES: O ânion difenil-4-amina sulfonato complexa o íon Zinco (II) e o produto dessa síntese se comporta de maneiras diferentes no tratamento térmico inerte e oxidante. O mesmo resíduo (ZnO) é obtido nas duas atmosferas, porém em uma temperatura mais elevada no primeiro (900 ºC) que no segundo (600 ºC). Isso mostra a estabilidade do complexo, que mesmo sob atmosfera oxidante só é degradado a uma temperatura alta.
AGRADECIMENTOS: LATIG-USP e PRESLAB-UFES.
REFERÊNCIAS BIBLIOGRÁFICA: MACHADO, L. C.; MARINS, A. A. L.; MURI, E. J. B.; BIONDO, A.; MATOS, J. R.; MAZALI, I. O. 2009. Complexation of the Fe(III) and Fe(II) sulphates with diphenyl-4-amine barium sulphonate (DAS): Synthesis, thermogravimetric and spectroscopic studies. Journal of Thermal Analisys Calorimetry: 87, 289-296.
WANG, M.; JIANG, H.; WANG, Z. C. 2006. Dehydration studies of Co (II), Cu (II) e Zn (II) methanesulfonates. Journal of Thermal Analysis and Calorimetry: 85, 751-754.
