ÁREA: Química Analítica
TÍTULO: ESTUDO DA VARIAÇÃO DO pH NA DETERMINAÇÃO DE Mn2+ UTILIZANDO VOLTAMETRIA DE REDISSOLUÇÃO CATÓDICA DE ONDA QUADRADA
AUTORES: SANTOS,V.E. (UFRN) ; Martinez-Huitle, C. A. (UFRN) ; FERNANDES. N.S. (UFRN)
RESUMO: O manganês é um metal abundante presente em diversos minerais. É considerado um elemento estratégico na economia mundial, pois tem amplo uso comercial e distribuição geográfica desigual. Exposições prolongadas a compostos de manganês, por inalação ou oralmente, podem provocar efeitos adversos no sistema nervoso, respiratório e outros. Neste trabalho foi realizado um estudo sobre a variação de pH na determinação da concentração de Mn2+ por voltametria de redissolução catódica, utilizando o eletrodo de trabalho de carbono vítreo, eletrodo de referência de prata cloreto de prata e um eletrodo auxiliar de platina.
PALAVRAS CHAVES: manganês, voltametria de redissolução catódica, carbono vítreo.
INTRODUÇÃO: A indústria química vem apresentando crescimento acentuado nos últimos anos. A questão ambiental que abrange os produtos gerados pelo setor químico vem sendo debatida no Brasil e no mundo nos últimos anos. A resolução 357 de 17 de março de 2005 do CONAMA (Conselho Nacional do Meio Ambiente) que regula os índices máximos de metais em águas para consumo humano limita o teor de manganês em 0,1 mg/L, sendo padrão para água doce. Os íons metálicos possuem alta toxicidade ao ser humano em concentrações inadequadas, podendo causar diversas doenças e distúrbios. Entre as principais aplicações industriais do manganês, destacam-se a fabricação de fósforos de segurança, ligas não-ferrosas (com cobre e níquel), pilhas secas, fertilizantes esmalte porcelanizado, fertilizantes, fungicidas, eletrodos para solda, magnetos, catalisadores, vidros, tintas, cerâmicas, materiais elétricos e produtos farmacêuticos (cloreto, óxido e sulfato de manganês) O excesso de manganês acumulado no fígado e no sistema nervoso central provoca sintomas do tipo Parkinson (doença degenerativa), por esses e outros efeitos prejudiciais é que o manganês é considerado tóxico e está na lista dos metais pesados. Entre as técnicas utilizadas para quantificar cátions e ânions dissolvidos em cada amostra é possível citar: ensaios volumétricos de neutralização, volumétricos de precipitação e volumétricos de complexação. Esse trabalho tem como objetivo determinar a concentração de íons manganês em diferentes pH utilizando a voltametria de redissolução catódica de onda quadrada.
MATERIAL E MÉTODOS: Para a determinação de Mn foi preparado solução estoque de 100 mg/L (5,59x10-4 mol/L de Mn2+), utilizando Mn(NO3)2 preparada com água deionizada. A solução tampão foi preparada com o Na2HPO4/NaH2PO4 pH 4, ajustando o pH com H3PO4 0,1 mol/L e NaOH 0,1 mol/L. As medidas voltamétricas foram realizadas em um Potenciostato/Galvanostato modelo PGSTAT12 da Autolab/Eco Chemie e monitorado pelo software GPES 4.9. Os estudos voltamétricos foram realizados em uma célula eletroquímica com capacidade para 50 mL, contendo um eletrodo de trabalho de carbono vítreo, um eletrodo de referência de prata/cloreto de prata e um eletrodo auxiliar de platina. Inicialmente, estudos de otimização dos parâmetros operacionais dessa técnica, como tempo de duração do pulso (tp), amplitude de potencial de pulso aplicado (DEp) e velocidade de varredura (v). As condições ideais obtidas para estes parâmetros foram: tp = 30 s; DEp 1,2 V e v = 10 mV s-1. Para a quantificação dos íons Mn foi necessário a preparação de uma curva de calibração que foi obtida utilizando a técnica de voltametria de onda quadrada de redissolução catódica (Fig. 1) e variando pH (Fig. 2) para otimizar os resultados com o tempo de deposição.
RESULTADOS E DISCUSSÃO: As análises da solução por voltametria de onda quadrada de redissolução catódica com 100 ppm de íons Mn (5,59x10-4 mol/L), em 30 mL do tampão (pH 4,0), apresentou uma faixa de pico catódico com valor de potencial -0,873 V (Fig. 1) com limite de detecção de 0,1667 ppm de Mn (7,76x10-7 mol/L).
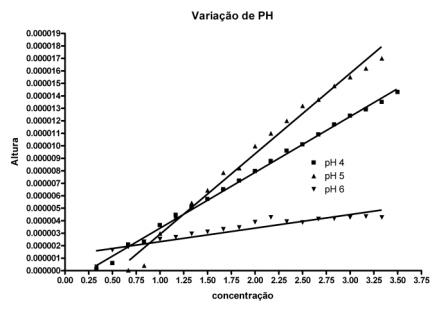
A curva analítica mostrou-se com uma linearidade maior em coeficiente de correlação de 0,9980 em pH 4 e tempo de deposição correspondente a 30 s. No pH 5 e 6 a faixa de trabalho diminui e acima do pH 6 ocorreu a adsorção dos íons manganês na superfície do eletrodo interferindo nos resultados (Fig. 2).
CONCLUSÕES: A partir dos resultados obtidos foi possível perceber que a voltametria de onda quadrada de redissolução catódica é eficiente para a determinação de íons Mn, em pH 4 e que o limite de detecção foi de 7,76x10-7 mol/L. Além disso, foi verificado que com o aumento do pH ocorreu a adsorção dos íons na superfície do eletrodo.
AGRADECIMENTOS: Coordenação e Aperfeiçoamento de pessoal de nível Superior CAPES e PETROBRAS.
REFERÊNCIAS BIBLIOGRÁFICA: CONAMA: Conselho Nacional de Meio Ambiente Disponível em: http://www.mma.gov.br/port/conama: Acesso em 02 de jul. 2010.
SKOOG, D.A., [et al]. Fundamentos de Química Analítica, São Paulo; Editora Thomson, 2006.
OLGA M.S. F., CHRISTOPHER M.A.B. Cathodic stripping voltammetry of trace Mn(II) at carbon film electrodes. Talanta. 2003, 61,643-650.
ROITZ, J.S., BRULAND, K.W. Determination of dissolved manganese (II) in coastal and estuarine waters by differential pulse cathodic stripping voltammetry. Analytica Chimica Acta, 344, 1997.
