ÁREA: Química Analítica
TÍTULO: AVALIAÇÃO DA EFICIÊNCIA DE UM GERADOR DE CLORO PARA ÁGUA POTÁVEL
AUTORES: BARROS, H.C. (UFPA) ; SILVA.C.C.L. (UFPA) ; MORAES, H.H.Q. (UFPA) ; CARVALHO, J. H. S. (UFPA) ; SILVA, J.S. (UFPA) ; LOPES A.S.C. (UFPA)
RESUMO: O presente trabalho detalha o funcionamento do gerador de cloro, equipamento que pode ser utilizado para promover a desinfecção de sistemas de abastecimento de água, o principal objetivo das análises químicas que foram feitas nas amostras coletadas, antes e depois do uso do mesmo, teve o intuito de comprovar a eficiência do mesmo no sistema de abastecimento, no qual ele foi instalado.
Foi necessário o acompanhamento dos parâmetros físicos, químicos e bacteriológicos das amostras de água, os quais permitem medir os fatores de qualidade e julgar a potabilidade da água e sua adequabilidade ao seu uso, tornando possível o diagnóstico de qualquer desvio nos padrões de qualidade impostos pela legislação.
PALAVRAS CHAVES: água; gerador de cloro; potabilidade; sistema de abastecimento.
INTRODUÇÃO: Nas últimas décadas, a humanidade vem se defrontando com uma série de problemas ambientais, financeiros, econômicos e sociais. Neste quadro, as preocupações ambientais e em particular com a água, adquirem especial importância, pois as demandas estão se tornando cada vez maiores, não só devido ao crescimento acelerado da população, mas, sobretudo por seu maior consumo (Rebouças et al., 2002). O monitoramento da água garante um conhecimento abrangente das condições em que a mesma se encontra, e serve para detectar qualquer índice de poluição ou contaminação presente na água e aplicar o tratamento especifico e adequado para cada caso.
O presente trabalho pode ser tratado como um passo a frente no sentido da gestão da qualidade da água, pois tem o intuito de comprovar que apesar de ao longo do tempo o avanço tecnológico tenha sido utilizado para acelerar o processo de contaminação e destruição do meio ambiente
MATERIAL E MÉTODOS: 2.1 Material: Os equipamentos e utensílios usados durante a execução desse trabalho são os que comumente se utiliza em laboratório de análises químicas quantitativa.
2.2 Métodos e procedimentos analíticos:
2.2.1: Amostragem:As amostras foram coletadas em duplicata utilizando-se frascos de polipropileno.
2.2.2 -Análises Físico-Química:DETERMINAÇÃO DE CONDUTIVIDADE MÉTODO CONDUTOMÉTRICO O condutivímetro antes de ser utilizado foi calibrado e configurado, para que a leitura fosse feita corretamente.
DETERMINAÇÃO DE ACIDEZ - MÉTODO ÁCIDO-BASE:A determinação da acidez é realizada adicionando-se à solução problema quantidade estequiométrica de NaOH.O ponto final da titulação é indicado pela mudança de cor do indicador
DETERMINAÇÃO DE CLORETOS - MÉTODO MOHR:Tranferiu-se 50 mL das amostras para erlenmayer de 125 mL, acrescentou-se aos mesmo 0,05 g de bicarbonato de sódio, logo em seguida adicionou-se 0,5 ml da solução de cromato de potássio a 5%, que é usada como indicador nesta determinação. Titulou-se as amostras com a solução de nitrato de prata, até a mudança da coloração.
DETERMINAÇÃO DE CLORO RESIDUAL Transferiu-se 100 mL das amostras para erlenmayer de 250 mL adicionou-se 4 mL da solução de ácido acético a 4%, acrescentou-se 1 g de iodeto de potássio, A solução adquiriu coloração amarela, acrescentou-se 0,5 mL da solução de amido, a solução passou a ter coloração azul violeta e tilou- se com a solução padrão de tiossulfato de sódio.
ANÁLISE BACTERIOLÓGICA : As amostras continham a solução de tiossulfato a 10%, as mesmas foram colocada em um frasco esterilizado e já flambado, até a marca de aferição de 90 mL, para completa os 100 mL da amostra, usou-se uma pipeta de 10 mL esterilizada e já flambada,em seguida foi colocado na amostra 1 envelope de meio de cultura.
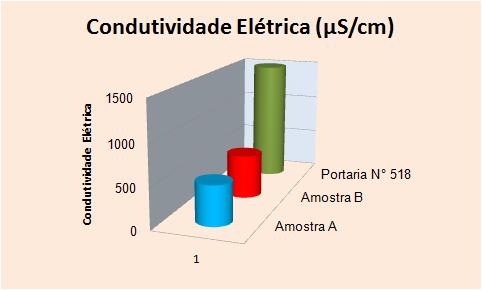
RESULTADOS E DISCUSSÃO: Os resultados obtidos nas análises químicas referente às amostras A e B, foram representados na tabela abaixo, possibilitando o entendimento e comparação dos dados como os valores padrões aceitos pela Portaria N° 518 MS-2004, referentes aos parâmetros indicadores da qualidade da água.Deve-se levar em conta que as coletas foram feita fora do período chuvoso, então não ocorrem mudanças bruscas na composição química dos aqüíferos dos lençóis freáticos. Os valores de alcalinidade e acidez encontram-se interligados observa-se que, a AMOSTRA A têm um pH mais baixo, isto implica em dizer que ela apresenta maior acidez, e menor alcalinidade e vise-versa com relação a AMOSTRA B, através da faixa de pH (4,5-8,3), também pode-se chegar a conclusão de que a alcalinidade da água é devido a presença de bicarbonato em quanto que a acidez é de origem carbônica. A condutividade elétrica em águas subterrâneas geralmente é alta, assim com os sólidos totais dissolvidos, isto se deve a concentração de íons presentes na mesma e que possuem uma diferença de potencial elevando a condutividade, isto é comum ocorre quando apresenta dureza, pois é considerada como uma boa condutora de elétrons devido à presença de íons Ca2+ e Mg2+. O aumento da concentração de cloretos na AMOSTA B, deve-se a presença do cloro residual na água resultante das reações de dissociação que ocorre do ácido hipocloroso (HClO) e do hipoclorito de sódio (NaClO), produzidos na reação eletrolítica. E ausência de coliformes totais e fecais indicam que água analisada pode ser considerada potável.
CONCLUSÕES: As análises químicas quantitativas, que foram feitas durante o andamento deste trabalho tinham o objetivo de comprovar a eficiência do uso do gerador de cloro.
Com base nestes dados chegou-se a conclusão de que este trabalho obteve o resultado esperado, pois os valores obtidos durante os experimentos encontram-se de acordo com Portaria 518.A presença do hipoclorito de sódio no abastecimento de água contribuiu para uma maior qualidade e potabilidade da mesma, podendo ser concluído que a instalação do gerador de cloro foi bem sucedida.
AGRADECIMENTOS: Ao Prof.Msc. Afonso Silva Mendes, pela participação desse trabalho. E pelos docentes e discente que também fizeram parte desse projeto.
REFERÊNCIAS BIBLIOGRÁFICA: BASSET, J; DENNEM, R.C; JEFFERY, G.H; MENDHAM, J. Química Analítica Quantitativa-Vogel, Ed. Guanabara dois, 5°Ed. Rio de Janeiro, 1998.
BABITT, H. E; DOLAND, J. J; CLEASBY, J. L. Abastecimento de Água, Tradução: Zadir Castelo Branco, São Paulo, Edgard Bluncher, 1976.
BACCAN, NIVALDO; ANDRADE, J.C.; GODINHO, OSAWALDO E.S; BARONE, J.S. Química analítica quantitativa elementar, Campinas-SP, Universidade Estadual de Campinas. Editora Edgard Blucher, 2°Ed, 1979.
BOSCARDIN BORGHETTI, N. R.; BORGHETTI, J. R.; ROSA FILHO, E. F. da. Aqüífero Guarani: a verdadeira integração dos países do Mercosul. 1ª ed.. Rio de Janeiro, P.214, Fundação Roberto Marinho, 2004.
BRASIL. FUNDAÇÃO NACIONAL DE SAÚDE. Manual prático de análise de água. 1ª ed. Brasília-DF, 2004.
CETESB - Companhia de Tecnologia e Saneamento Ambiental de São Paulo. E .coli Teste de Fluorescência, baseado na detecção da enzima β-D glucoronidase, para diferenciação de colônias de outros coliformes (técnica de membrana filtrante). São Paulo, p.13, dez. 1992. [Método de ensaio L5.531].
FÖRSTNER, U. & WITTMANN, G. T. W. Metal pollution in the aquatic environment. Berlin: Springer-Verlag, 1983. 486p.
MACÊDO, J. A. B.. Águas & Águas. Belo Horizonte MG: CRQ-MG, 2004.
ROSSIN, A. C. Desinfecção. In: CETESB. Técnica de Abastecimento e Tratamento de Água (Tratamento de Água), 2 ed., São Paulo: CETESB/ASCETESB, 1987.
WELTE, D. Organic geochemistry of carbon. In: WEDEPOHL, K. H. (ed.) Handbook of: Springer-Verlag, 1969.
WORLD HEALTH ORGANIZATION. Guidelines for Drinking Water Quality - vol 2 Recomendations.Geneve: WHO, p.8-29, 1998.
