ÁREA: Iniciação Científica
TÍTULO: NANOCOMPÓSITOS ELETROATIVOS A BASE DE POLIANILINA E ÁGAR EXTRAÍDO DA ALGA VERMELHA GRACILARIA BIRDIAE OBTIDA NO LITORAL DO PIAUÍ
AUTORES: DOS SANTOS, M. C. (UFPI) ; FARIAS, E. A. O. (UFPI) ; DOS SANTOS, R. C. S (UFPI) ; LEITE, J. R. S. A. (UFPI) ; DA SILVA, D. A. (UFPI) ; EIRAS, C. (UFPI)
RESUMO: Filmes finos nanoestruturados formados a partir da técnica de automontagem do tipo LbL (layer-by layer) de polianilina (PANI), um polímero condutor, e Ágar, um polissacarídeo natural extraído da alga vermelha Gracilaria birdiae, abundante no litoral do Piauí foram preparados e caracterizados por medidas de voltametria cíclica (VC) e espectroscopia de UV-VIS. Os filmes foram formados em duas arquiteturas distintas e usando o Agar extraído pelo método artesanal e químico. Os resultados obtidos mostraram que a arquitetura usada para a montagem dos filmes afeta a quantidade de material adsorvido em cada etapa de deposição e os maiores valores de absorbância encontrados referem-se a sequência PANI/ágar.
PALAVRAS CHAVES: ágar, polianilina e automontagem.
INTRODUÇÃO: Nos últimos anos, polissacarídeos bioativos isolados de fontes naturais como as algas, têm atraído a atenção da comunidade científica em áreas como a bioquímica e a farmacologia (WAN et al., 2001). O interesse no Ágar surge devido a abundância de algas vermelhas encontradas no litoral do Piauí e pelas propriedades biológicas apresentadas por este polissacarídeo (CUNHA et al., 2009).
A preparação de filmes finos formados a partir da técnica de automontagem do tipo layer-by-layer (LbL) permite a caracterização in situ dos materiais formadores do filmes dispostos em multicamadas, além de possibilitar o controle da espessura, ordenamento em nível molecular e obtenção de um pequeno tempo de resposta induzido pela camada LbL ultrafina (HOU et al., 2002).
Neste trabalho foram obtidos filmes finos nanoestruturados formados a partir da técnica de automontagem do tipo LbL (layer-by layer) de polianilina (PANI), um polímero condutor, e Ágar. Estes filmes foram caracterizados por medidas de voltametria cíclica (VC) e espectroscopia na região do UV-VIS. Os filmes foram formados em duas arquiteturas distintas (PANI/Agar e Agar/PANI) além de terem sido confeccionados com o Agar obtido tanto pelo método artesanal quanto químico de extração.
MATERIAL E MÉTODOS: A polianilina, na forma de base esmeraldina, foi obtida pela síntese química proposta por Mattoso (1996). Já o Agar foi extraído da alga Gracilaria birdiae coletada na praia do Coqueiro, litoral do Piauí, em junho de 2011, pelos métodos artesanal, realizado em meio aquoso a quente (80°C por 2h), ou químico realizado pelo mesmo procedimento no entanto, em meio de NaOH 5%. A solução de Agar foi filtrada e estocada sob refrigeração até o momento de sua utilização no preparo dos filmes finos.
Os filmes LbL foram preparados através imersão alternada do substrato sólido, (ITO ou vidro), nas soluções do policátion (PANI) e do poliânion (Agar). As caracterizações foram realizadas por voltametria cíclica (VC) e espectroscopia de UV-VIS. Nas medidas de VC utilizou-se uma célula eletroquímica com capacidade para 10 mL e encaixe para três eletrodos: O eletrodo de referência, calomelano saturado (ECS), o contra-eletrodo, uma placa de platina com área de 1,0 cm2 e, eletrodo de trabalho constituído pelo filme LbL sobre ITO. As medidas foram obtidas em um potenciostato/galvanostato PGSTAT 128N da AUTOLAB. Para as medidas espectroscópicas os filmes foram depositados sobre eletrodo de vidro comum e a formação das multicamadas foi monitorada empregando-se um espectrofotômetro SHIMADZU modelo UV-
1800.
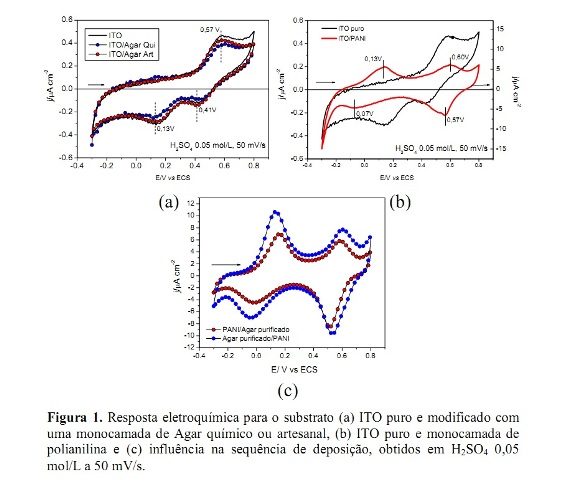
RESULTADOS E DISCUSSÃO: A figura 1a mostra o perfil eletroquímico para o eletrodo de ITO puro e modificado com uma monocamada de Agar obtido pelos métodos de extração; artesanal e químico. A presença do Ágar sobre o ITO não altera a resposta eletroquímica característica do substrato, uma vez que para todos os casos estudados foram observados um processo de oxidação (0,57V) e dois processos de redução (0,41V e 0,13V). No entanto, ao modificar o ITO com uma monocamada de PANI, figura 1b, observa-se um novo perfil eletroquímico agora característico do polímero condutor em meio ácido. A polianilina apresenta dois pares redox intrínsecos claramente descritos na literatura (MATTOSO, 1996).
Após o estudo do comportamento eletroquímico individual do Agar e da PANI, fez-se a deposição das bicamadas com objetivo de analisar o efeito sinérgico resultante destes materiais. Os resultados preliminares obtidos Agar químico, estimularam seu emprego após ter sido submetido a uma etapa posterior de purificação (chamado Agar purificado). Duas seqüências de deposição foram estudadas, ITO/PANI/Agar e ITO/Agar/PANI e são mostradas na figura 1c. Os maiores valores de densidade de corrente foram obtidos para o sistema bicamada em que a PANI foi depositada sobre o ITO modificado com o Agar.
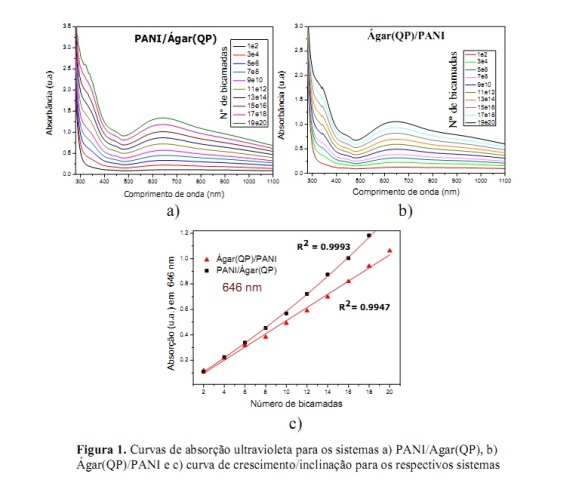
O crescimento dos filmes LbL foi monitorado por UV-VIS a cada duas bicamadas depositadas, figura 2a e 2b. A variação da absorbância em função do número de bicamadas, figura 2c, mostra que a espessura do filme é controlada pelo número de bicamadas depositadas em ambos os sistemas e que a seqüência de deposição define as propriedades finais dos filmes. Os maiores valores de absorção foram obtidos para o sistema PANI/Agar(QP).
CONCLUSÕES: Nanocompósitos eletroativos a base de PANI e Agar foram preparados pela técnica de automontagem do tipo LbL. O Agar extraído pelo método químico e submetido a uma etapa adicional de purificação foi utilizado na formação das bicamadas onde a seqüência de deposição PANI/Agar(QP) mostrou os maiores valores de absorbância e um comportamento exponencial. Os resultados eletroquímicos e espectroscópicos obtidos impulsionam o uso de filme de PANI/Agar(QP) como um novo material com vistas a aplicações como camada ativa para sensores eletroquímicos.
AGRADECIMENTOS: Rede NanoBioMed/CAPES, CNPq pela bolsa concedida, FAPEPI.
REFERÊNCIAS BIBLIOGRÁFICA: CUNHA, P. L. R. da; PAULA, R. C. M. de e FEITOSA, J. P. A.. Polissacarídeos da biodiversidade brasileira: uma oportunidade de transformar conhecimento em valor econômico. Química Nova, n.3, v. 32, 2009.
HOU, Y., JAFFREZIC-RENAULT, N., ZHANG, A. et al. Study of Pure Urease Langmuir-Blodgett Film and Application for Biosensor Development, Sensors and Actuators B: Chemical, v. 86, pp. 143149, 2002.
KERN, W. Purifying Si and SiO2 surfaces with hydrogen peroxide. Semicond. Int., 7:94-98, 1984.
MATTOSO, L. H. Polianilinas: síntese, estrutura e propriedades. Quím. Nova, v. 19, n. 4, p. 388-399, 1996.
WAN, E.; GALEMBECK, E.; GALEMBECK, F.; Polímeros sintéticos. Química Nova na Escola, Edição especial, p. 5-8, 2001.
