ÁREA: Físico-Química
TÍTULO: ESTUDO TEÓRICO DA RELAÇÃO ENTRE ESTRUTURA E ATIVIDADE DO PARACETAMOL E SEUS DERIVADOS ANÁLOGOS
AUTORES: DINIZ, J.E.M. (UEAP) ; MELO, S.S. (UFPA) ; LOBATO, C.C. (UEAP) ; LIMA, M.M.G. (UEAP) ; SANTOS, C.B.R. (UEAP) ; ALVES, C.N. (UFPA)
RESUMO: Neste trabalho foram usados cálculos químicos quânticos do nível da teoria B3LYP, junto com o conjunto de base 6-31G* foram utilizados para obter a energia (E), potencial de ionização (PI), energia da dissociação de ligação (BDE), e distribuição da densidade de spin para o paracetemol (PAR) e seus derivados análogos. Os resultados obtidos com métodos de B3LYP são confrontados com os cálculos Hartree Fock e com os produtos metabólicos formados no sistema biológico. A correlação entre a atividade analgésica, citotoxicidade, e propriedade eletrônica foi obtida através de matriz de correlação.
PALAVRAS CHAVES: análogos do paracetamol. atividade analgésica. dft.
INTRODUÇÃO: O paracetamol (4-hidroxiacetanilida, N-acetil-p-aminolfenol, PAR) é um analgésico largamente utilizado e uma droga antipirética, que em estudos realizados mostrou-se que uma overdose aguda de PAR e seu uso a longo prazo pode levar a um falência renal aguda com risco de doença renal crônica, assim como uma necrose hepática (MITCHELL et al, 1973), além de ser usado por jovens em depressão para cometer suicídio.
Tomando o mecanismo molecular do PAR bem como a hepatotoxidade tem havido vários esforços para melhorar a sua atividade analgésica, evitando sua toxicidade, modificando sua estrutura. Recentemente, sete análogos 3,5-dissubstituído de paracetamol foram sintetizados a fim de comparar suas propriedades físico-químicas, farmacológicas e toxicológicas (BESSEMS et al, 1995).
Este trabalho tem como objetivo estudar uma serie de compostos químicos derivados do paracetamol e também, determinar teoricamente quais propriedades Físico-Químicas seriam de maior relevância para explicar a atividade analgésica de análogos do paracetamol.
MATERIAL E MÉTODOS: O método da Teoria do Funcional de Densidade (DFT) tendo como funcional híbrido B3LYP e o conjunto de funções de base 6-31G* do pacote computacional Gaussview versão 2.1 (GAUSSIAN, 2000) foi empregado para otimização de geometria e determinação dos parâmetros eletrônicos a serem correlacionados com a atividade biológica, tais como: potencial de ionização, energia dos orbitais moleculares HOMO e LUMO, moleza e dureza molecular. O método de regressão linear múltipla (RLM) foi empregado para correlacionar atividade biológica com as propriedades moleculares analisadas, assim como utilizou-se o pacote computacional statistic versão 7.0 (STATSOFT, 2004) para fazer a correlação matricial entre a atividade e as propriedades analisadas, além da análise de regressão linear.
RESULTADOS E DISCUSSÃO: Os análogos do paracetamol, analisados, são mostrados na figura 1. Dos resultados obtidos a partir dos cálculos realizados, ver tabela 1, montou-se uma correlação matricial, onde se observou que dentre as propriedade fisico-químicas analisadas em relação a atividade biológica, a mais relevante, para análise, foi o potencial de ionização (PI). O modelo de regressão obtido pela equação (Log 1/C= 7.8362+1.3352PI) apresenta um grau de explicação de 78 % da variabilidade dos valores observados para a atividade. O teste de significância indicou valor de F= 17,4. Além do mais, apresentou razoável grau de previsibilidade, pois Q2= 0,63 e pequena soma dos erros de previsão SEP = 0,56.
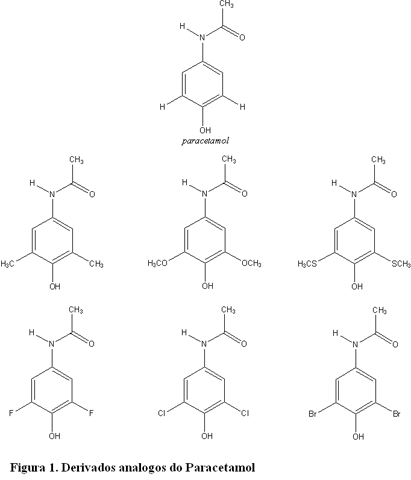
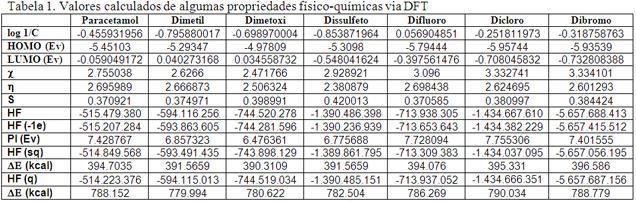
CONCLUSÕES: As variáveis descritoras das propriedades físicas e eletrônicas com potencial relevância para a atividade analgésica foram examinadas para o PAR e análogos 3,5, usando cálculos da mecânica quântica no nível de teoria B3LYP. Os substituintes de elétrons doados na posição 3,5 (-CH3, -OCH3, e -SCH3) diminuídos o potencial de ionização resultante em melhores propriedades inibitórias de cicloxigênese do que o PAR, enquanto que os substituintes de elétrons de halogênio retirados (-F, -Cl, e -Br), aumentaram o potencial de ionização resultante aumentando a capacidade inibitória de cicloxigênese.
AGRADECIMENTOS: CNPq (PNOPG- 55.0822/01-1) - UFPA
REFERÊNCIAS BIBLIOGRÁFICA: BESSEMS, J. G. M.; GAISSER, H. D.; TE KOPPELE, J. M.; VAN BENNEKON, W. P.; COMMANDEUR, J. N. M.; VERMEULEN, N. P. E. 1995, 3,5-Disubstituted analogues of paracetamol. Synthesis, analgesic activity and cytotoxicity. Chemico-Bilogical Interactions, 98, 237-250.
GAUSSIAN, Inc, Gaussview, 2.1, Pittsburgh, PA, 2000.
MITCHELL, J.R.; JOLLOW, D.J.; POTTER, W.Z.; DAVIS D.C.; GILLETTE, J.R., BRODIE, B.B. J. Pharmacol. Exp. Ther. 187 (1973) 185.
STATSOFT, Inc, Statistica 7.0, Tulsa, OK, USA, 2004.
